Cistinosis
Palabras clave
Síndrome de Fanconi, cisteamina, Cis IL, gen CTNS
1. INTRODUCCIÓN
La cistinosis es una enfermedad minoritaria de herencia autosómica recesiva, causada por variantes patogénicas del gen CTNS, que afecta al transporte de cistina en los lisosomas. Se caracteriza por el depósito progresivo y sistémico de cistina intralisosomal principalmente a nivel renal y ocular [1]. Además, la cistinosis nefropática es la primera causa del síndrome de Fanconi hereditario [2]. Sin tratamiento específico evoluciona a fallo renal a los 10-12 años de edad y afecta progresivamente a todos los órganos, con elevada morbimortalidad [3]. Gracias al diagnóstico precoz, tratamiento con cisteamina y éxito de los programas de trasplante renal (TxR) en niños y adolescentes, la historia natural de esta enfermedad se ha transformado [4]. El tratamiento con cisteamina ha conseguido retrasar la edad del fallo renal, disminuir la severidad y frecuencia de la afectación extrarrenal, y paralelamente aumentar la expectativa de vida de los pacientes [5]. En la actualidad hay más pacientes adultos que pediátricos, y la cistinosis ha trascendido del ámbito pediátrico a la medicina del adulto [6].
2. ETIOPATOGENIA
La cistinosis es una enfermedad hereditaria autosómica recesiva causada por mutaciones en el gen CTNS (cromosoma 17p13), que codifica la cistinosina [7], proteína transmembrana del lisosoma con función de cotransportador específico cistina/protón que permite la salida de cistina (dímero del aminoácido cisteína tras un proceso de oxidación) desde el lisosoma al citoplasma celular [1]. En ausencia de cistinosina se produce un depósito progresivo de cistina intralisosomal que constituye el principal marcador diagnóstico, además del estudio genético [3]. La enfermedad tiene una incidencia de 1/100.000-200.000 nacidos y una prevalencia de 1-9/1.000.000. La mutación más común en población occidental es una deleción de 57 Kb que incluye también al gen CARKL que codifica el enzima sedoheptulokinase [8], observándose también en el 34% de la población española [9]. La cistinosis nefropática se suele asociar con dos mutaciones severas o truncantes del gen CTNS, que afectan al promotor, secuencia principal, regiones transmembrana o no-transmembrana, incluyendo pequeñas deleciones/inserciones, o mutaciones de tipo missense o splicing [3].
En el interior del lisosoma, el aminoácido cisteína se oxida y forma cistina, compuesto poco soluble. Se produce un acúmulo de cistina que precipita en forma de cristales en todas las células del organismo, especialmente en tejido renal y ocular [10]. Además del acúmulo de cristales, los defectos del gen CTNS afectan a vías intracelulares, inflamatoria y fibrótica. Aumenta la apoptosis en las células epiteliales del túbulo proximal (PTEC), podocitos y fibroblastos, disminuyen los niveles de ATP y AMPc, y causa disfunción mitocondrial, alterando la autofagia y el anabolismo [7] [11] [12] [13] [14] [15] [16] [17] [18] [19] [20] [21] [22] [23] [24] [25]. Junto con los efectos deletéreos secundarios del depósito de cristales, estos mecanismos contribuyen a la patogenia de la cistinosis.
3. FORMAS CLÍNICAS
La cistinosis es una enfermedad multisistémica [17], siendo el riñón y el ojo los primeros órganos afectados. Se han descrito tres formas clínicas: cistinosis nefropática infantil (OMIM#219800) es el subtipo más grave, de aparición precoz; cistinosis nefropática juvenil (OMIM #219900) que es un subtipo menos severo, de debut juvenil o tardío, de severidad intermedia y la cistinosis no-nefropática o del adulto (OMIM#219750), con afectación ocular exclusiva [19]. No obstante, en la práctica clínica, se diferencian dos subtipos principales: cistinosis nefropática de debut en la primera infancia con síndrome de Fanconi severo que representa el 95% de todos los casos y cistinosis no nefropática de debut tardío, que aparece en el joven o adulto, con afectación renal y/o ocular; representa el < 5% del total de afectos. En algunos pacientes la afectación ocular puede preceder en años a la afectación renal [20].
4. AFECTACIÓN RENAL
Síndrome de Fanconi
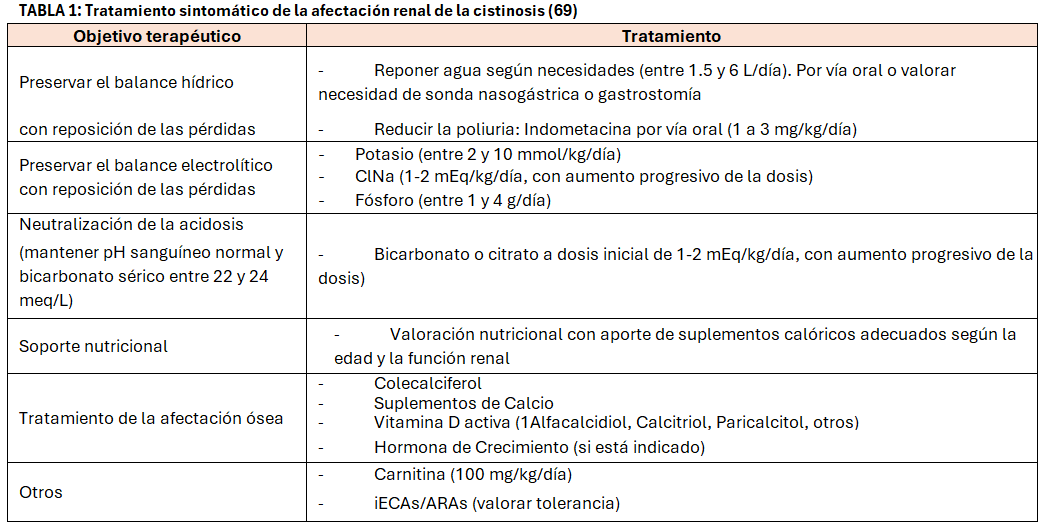
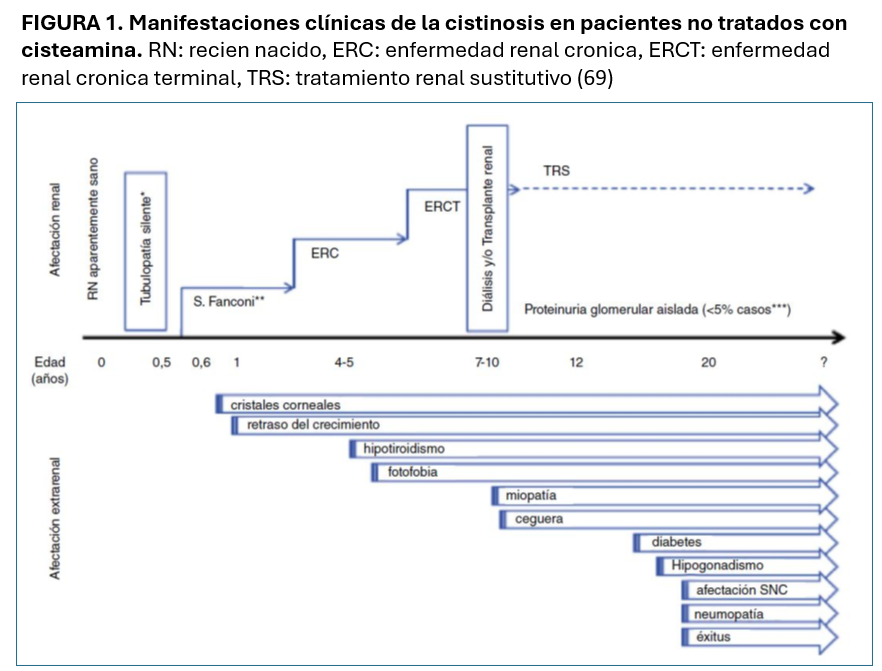
El síndrome de Fanconi severo se considera el cuadro clínico al debut de la enfermedad con progresión a Enfermedad Renal Crónica (ERC) (Figura 1). Se suele manifestar en el segundo semestre de vida, tras un intervalo libre de síntomas [1]. Los recién nacidos afectos son aparentemente normales, si bien es posible detectar alteraciones urinarias muy precoces (orina alcalina con glucosuria y/o proteinuria) precediendo a los síntomas [21]. La cistinosis representa la causa más frecuente de síndrome de Fanconi de etiología genética [19] y debe ser considerada en primer lugar en el diagnóstico diferencial en lactantes. No obstante, se han descrito casos de pacientes con cistinosis con cuadros atípicos de tubulopatía distal, tales como diabetes insípida nefrogénica o síndrome de Bartter. Por tanto, ante cualquier tubulopatía compleja, sobre todo si existe afectación del crecimiento y/o anorexia debemos considerar la cistinosis [3]. Dada la severidad del cuadro requiere de un riguroso tratamiento que debe ser iniciado de modo inmediato [24] (Tabla 1).
Enfermedad Renal Crónica
A partir de los dos años, sin tratamiento específico, se produce una afectación glomerular progresiva con descenso del Filtrado Glomerular (FG) y aumento de la creatinina plasmática a partir de los 4-6 años, con evolución a ERC avanzada [1]. En consecuencia, la edad media de aparición de fallo renal es 9,2 años. En las series contemporáneas que incluyen pacientes tratados precozmente con cisteamina, se observa un retraso en la progresión de ERC, comenzando el Tratamiento Renal Sustitutivo (TRS) alrededor de los 13 años [4], incluso existe un porcentaje creciente que no ha iniciado TRS después de la adolescencia [6].
Existen formas de cistinosis atenuada o de debut tardío que se manifiestan en la adolescencia o en adultos jóvenes como enfermedad glomerular y proteinuria sin síndrome de Fanconi, aunque ocasionalmente con datos sugestivos de tubulopatía proximal. Habitualmente, los pacientes presentan manifestaciones oculares paucisintomáticas [20] (Figura 1).
La biopsia renal, aunque no es necesaria para el diagnóstico, demuestra lesiones inespecíficas de glomeruloesclerosis y otras más características como irregularidades en el «borde en cepillo» de la célula tubular proximal, lesiones en «deformidad en cuello de cisne» y ocasionalmente depósitos de cristales de cistina y podocitos gigantes multinucleados [2] [11]. No obstante, estos hallazgos histológicos pueden ayudar a identificar pacientes con cistinosis juvenil con proteinuria no nefrótica.
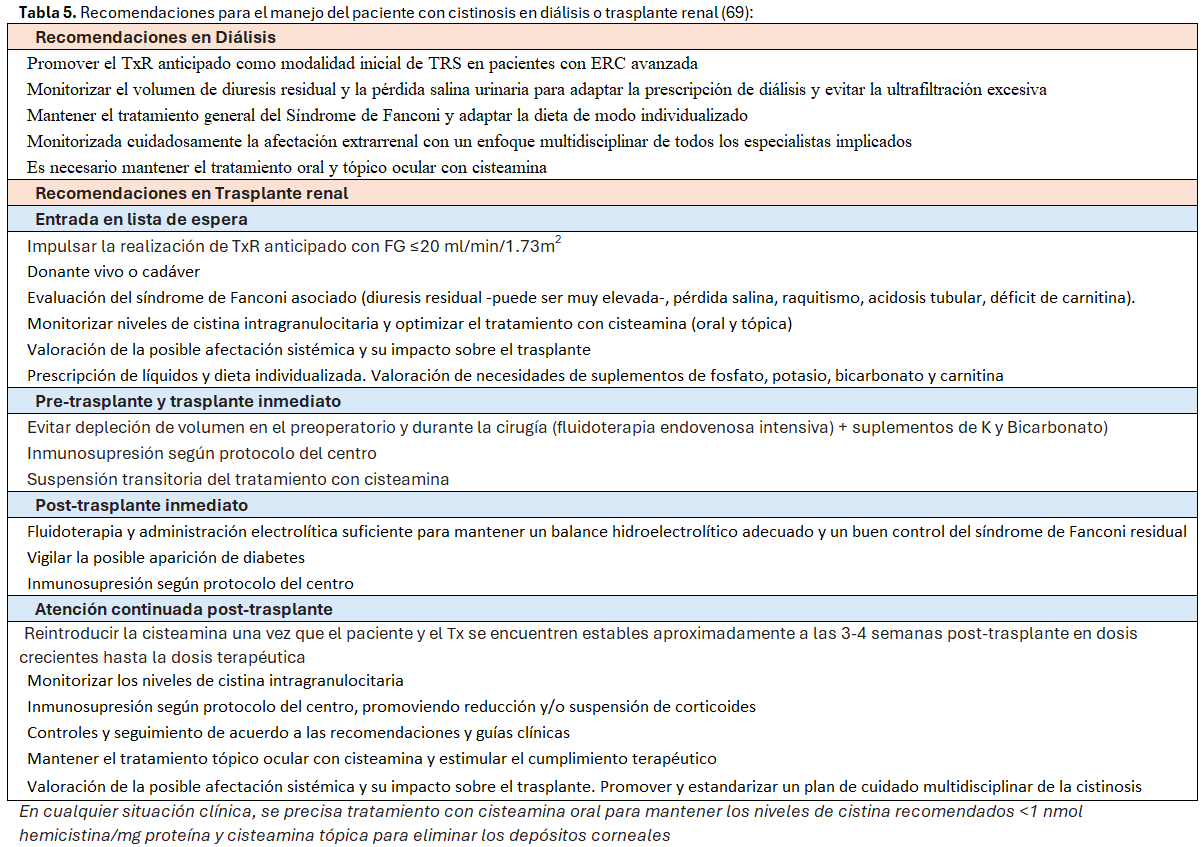
Diálisis (Tabla 2)
Idealmente el TxR es la técnica de elección si bien la limitación de órganos o el diagnóstico tardío condiciona el inicio de diálisis. Según el registro europeo ESPN/ERA-EDTA Registry un 0,9% de los pacientes < 20 años con TRS padecían cistinosis. En Europa, la diálisis peritoneal representó la modalidad inicial más frecuente (39,6%), seguido por el TxR anticipado (35,1%) y hemodiálisis (17,9%) respectivamente [4].
A diferencia de otras enfermedades renales, el síndrome de Fanconi puede persistir tras el inicio de diálisis. Como consecuencia de esto, no suelen precisar restricción en la ingesta hídrica ni uso de quelantes de fósforo. Recientemente se ha descrito que los pacientes con cistinosis y ERC avanzada presentan unos niveles de FGF23 y PTH significativamente inferiores a pacientes con ERC de otra etiología, posiblemente por una afectación ósea primaria característica [26].
Trasplante renal (Tabla 2)
El TxR es la técnica de elección de TRS. Las células del injerto no portan el defecto lisosomal y por ello la enfermedad no recurre en el órgano trasplantado [16].
El trasplante de donante emparentado también es curativo y los portadores heterocigotos de la mutación de CTNS pueden ser donantes adecuados ya que no padecen la enfermedad [6] [27]. Se sugiere realizar un TxR anticipado, sobre todo cuando exista un donante vivo disponible [27]. Así, la indicación de TxR se establece cuando el FG es < 20ml/min/1,73 m2, algo más precoz que en otras patologías renales [3].
Los datos del Registro Europeo (ESPN/ERA-EDTA Registry) muestran un 35,1% de trasplantes anticipados. Del global de pacientes con cistinosis en TRS, un 85% estaban trasplantados. Respecto al tipo de donante, en Europa el 48,9% recibieron un TxR de donante vivo [4].
Es de destacar que la duración del injerto renal funcionante en los pacientes con cistinosis es superior que el observado en otras etiologías de enfermedad renal [4].
La indicación de nefrectomía unilateral o bilateral previa al trasplante puede considerarse en pacientes con poliuria severa, si bien no existe un consenso al respecto y tampoco está bien definido el momento de realizarlo (previo, durante la cirugía del trasplante o después de éste) [28] [29] [30].
5. AFECTACIÓN EXTRARRENAL
La naturaleza sistémica de la enfermedad explica la aparición progresiva de otra sintomatología clínica secundaria al depósito de cristales de cistina en los distintos órganos y sistemas (Figura 1):
Afectación ocular
La afectación ocular es universal. La presencia de cristales de cistina en la córnea es una de las manifestaciones más precoces y criterio diagnóstico de esta enfermedad [3] [31]. Los cristales están ausentes al nacimiento, pero pueden observarse a los pocos meses de vida [3]. Inicialmente se depositan en las capas superficiales de la córnea periférica, pero progresivamente afectan a todas las capas y extensión de la córnea. Su consecuencia es la fotofobia, que puede ser incapacitante, y la alteración en la sensibilidad corneal. Con el tiempo, se producen erosiones corneales recidivantes y edema estromal, que pueden provocar disminución de la agudeza visual. En casos no tratados y con afectación severa, se ha descrito depósito de calcio en la membrana de Bowman o queratopatía en banda [32]. Estos cristales también se depositan en otras estructuras oculares (conjuntiva, cámara anterior, iris, cuerpo ciliar, coroides y retina) [33]. Por otro lado, se observa disminución de la producción de lágrimas y ojo seco, y manifestaciones neuro-oftalmológicas (papiledema y oftalmoplejía) secundarias al aumento de la presión intracraneal [27]. En las formas tardías de la enfermedad la presencia de cristales puede no ser detectada hasta la edad adulta [20].
Crecimiento y desarrollo. Enfermedad mineral-ósea
El retraso de crecimiento es un síntoma clásico y suele ser motivo de consulta precoz [34]. Estos pacientes presentan hasta 11 veces más riesgo de deformidades óseas, cirugía ortopédica y talla baja [1]. La etiología es multifactorial relacionándose con la severidad del síndrome de Fanconi, frecuentemente con hipofosfatemia, hipocalcemia y disminución de hormona paratiroidea. La concurrencia de acidosis metabólica, desnutrición, pérdidas digestivas y renales aumentadas y la ERC conducen a un déficit de crecimiento, en el que se observa una mineralización alterada y aumento en la reabsorción ósea [26] [35].
Históricamente, los pacientes con cistinosis nefropática mal controlados alcanzaban menor estatura [34], con una talla adulta promedio de 144 cm y un peso de 45 kg, 25 cm y 25 kg por debajo de la media [27]. Con un mejor control terapéutico, se observa menor retraso estatural [5]. A pesar de ello, un 44% de los pacientes en diálisis y un 27% de los trasplantados siguen teniendo talla baja y aspecto grácil [4]. La administración temprana de GH mejora la talla, aunque la respuesta es menor que en otros tipos de ERC. La GH es esencial por su efecto anabólico y sobre el crecimiento [26] [36].
Se desarrolla una enfermedad ósea metabólica característica multifactorial no sólo por el depósito de cristales de cistina en el hueso, mineralización deficiente, raquitismo de origen renal [19], la ERC per se [37] y al déficit de cobre (posiblemente secundario al síndrome de Fanconi de larga duración), sino por la propia afectación ósea de la cistinosis [38]. Por ello es frecuente detectar osteopenia, especialmente en trasplantados, también en relación con otras alteraciones endocrinas y con el tratamiento [18]. En algunos casos se detecta fragilidad ósea y mayor riesgo de fracturas [25] [39].
Afectación endocrina
Las manifestaciones endocrinas se producen por destrucción de las glándulas afectas debida a los depósitos de cistina; su incidencia y edad de aparición están asociadas a la instauración del tratamiento con cisteamina [1]. El hipotiroidismo primario es la complicación más frecuente [27], de curso progresivo y requiere tratamiento crónico con levotiroxina [3]. La diabetes mellitus se caracteriza por una alteración progresiva de la secreción de insulina [40], con inmunología negativa y requiere tratamiento con insulina [1]. Se observa en pacientes trasplantados que reciben corticosteroides [18]. Es importante tratar el hipogonadismo hipergonadotrófico que se observa en los varones afectos. Así mismo es frecuente la diabetes mellitus en el paciente adulto [1] [6].
Afectación cardiovascular
La aparición de dislipemia y calcificación vascular por la propia cistinosis y por la ERC per se, aumentan del riesgo cardiovascular [1] [18] [25]. Un 42% de los pacientes desarrollan hipertensión arterial postrasplante. También se han descrito aneurismas aórticos y afectación de vasos coronarios, así como cuadros de miocardiopatía asociados al depósito de cristales de cistina en miocardio [25] [30]. En pacientes adultos se recomienda el despistaje de cardiopatía isquémica [27].
Afectación neurológica
Pueden presentar una miopatía progresiva [27], de predominio distal de inicio en manos; objetivándose pérdida de masa muscular con posterior afectación de la capacidad ventilatoria y dificultades en la deglución. Algunos autores atribuyen la debilidad muscular al déficit de carnitina [23].
La afectación del Sistema Nervioso Central (SNC) [27] sobre todo en pacientes con tratamiento subóptimo con cisteamina puede ser:
1. De presentación aguda: cefaleas, epilepsia, ictus, encefalopatía. [41] [42] [43]
2. De presentación subaguda/progresiva: hipertensión endocraneal, atrofia cerebral, ataxia, piramidalismo, trastornos en la marcha, calcificaciones en los ganglios basales y periventriculares, desmielinización de la sustancia blanca, deterioro mental [44] [45] [46] [47] [48] [49] [50]
Afectación gastrointestinal y hepática
Las náuseas, los vómitos, el dolor epigástrico y la anorexia son frecuentes debidos al aumento de la secreción de gastrina asociado al uso de cisteamina, antiácidos y bloqueadores de los receptores H2. Puede producirse reflujo gastroesofágico, dificultades mecánicas para tragar, retraso en el vaciado gástrico, alteración de la motilidad intestinal, pseudo-obstrucción intestinal y enfermedad inflamatoria intestinal. A nivel hepático, puede observarse hepatomegalia, hipertensión portal no cirrótica con hiperesplenismo, colestasis e hipercolesterolemia [25] [51] [52].
Afectación hematológica
La anemia es de origen multifactorial (déficit nutricional, alteración hormonal, hiperesplenismo, inflamación y asociada a la ERC). Se pueden encontrar depósitos de cristales de cistina en la médula ósea que pueden provocar citopenias [25] [53]. Se ha descrito casos de coagulopatía asociada a la disfunción plaquetaria [17] [25] [53].
Afectación dermatológica
Puede observarse hipopigmentación de la piel y el pelo debido a una melanogénesis alterada, así como alteración de la sudoración e intolerancia al calor [3] [25] [27].
6. DIAGNÓSTICO
El diagnóstico de la cistinosis se establece mediante el diagnóstico clínico y se confirma con el diagnóstico bioquímico y molecular.
Diagnóstico clínico
Los signos guía son el síndrome de Fanconi severo de aparición precoz (retraso del crecimiento, náuseas, vómitos, poliuria-polidipsia, deshidratación y/o raquitismo) y la detección de cristales corneales [20] [25]. En pacientes con formas menos severas, se observa fallo renal y proteinuria. Ocasionalmente la visualización de cristales en córnea, que es patognomónica de la enfermedad, en pacientes adultos con ERC de causa no filiada conduce al diagnóstico [20]. La utilidad de la biopsia renal es limitada, pero puede ser de utilidad en presentaciones atípicas [1] [30] [54], siendo el diagnóstico genético de elección ante una sospecha clínica [1].
Diagnóstico bioquímico
El diagnóstico bioquímico general consiste en la detección de trastornos hidroelectrolíticos, del equilibrio ácido-base y eventualmente de la función renal, característicos del síndrome de Fanconi [1] [17] [27].
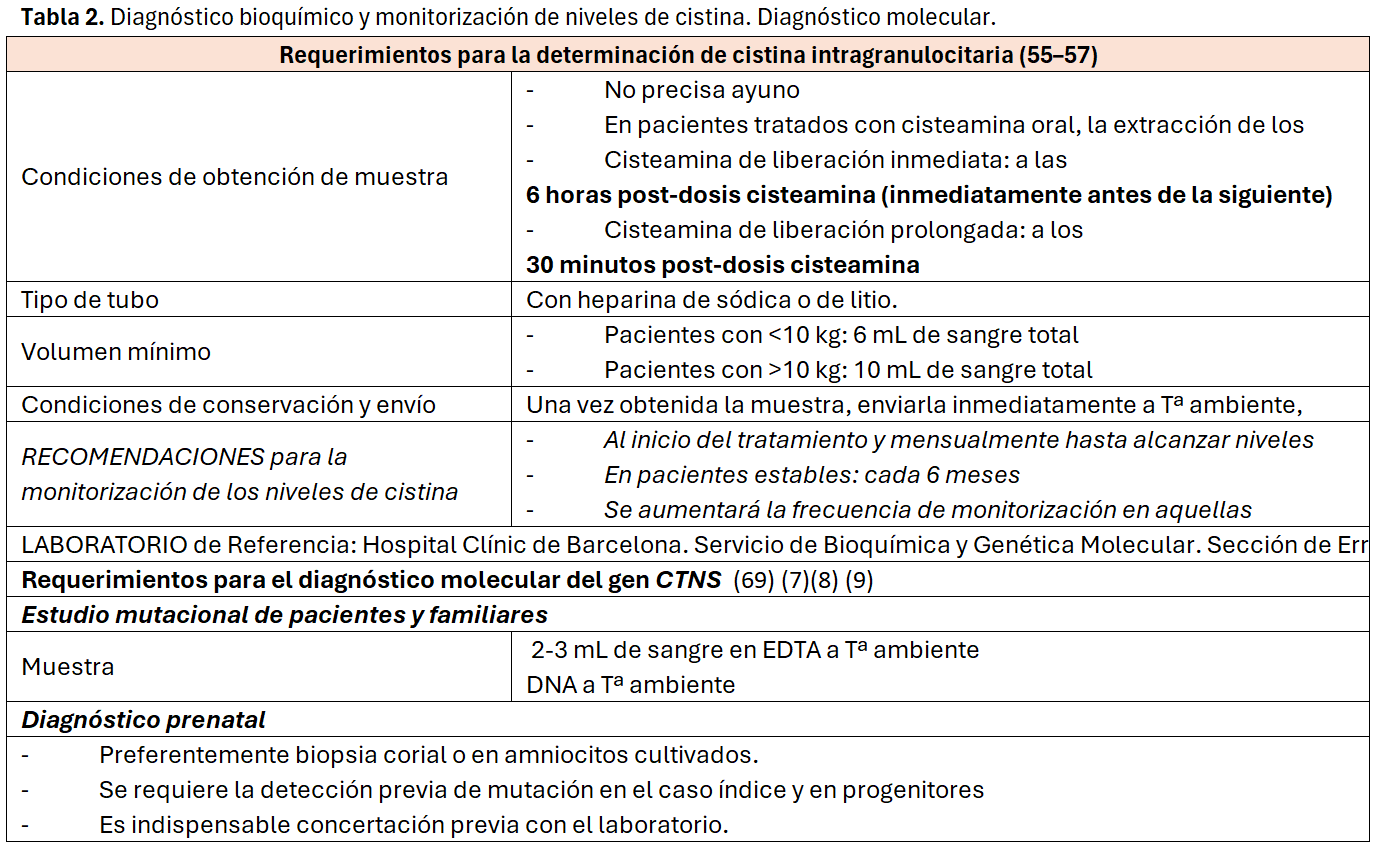
El diagnóstico específico consiste en la detección de niveles elevados de cistina intraleucocitaria en leucocitos totales (CiS IL) [55]. En la actualidad se aplican las técnicas de cromatografía líquida de alta presión-espectrometría de masas en tándem (HPLC-MS/MS) en muestra de granulocitos que es una técnica más sensible [25] [56] [57]. Los valores de referencia son:
* Individuo sano < 0,5 nmol hemicistina/mg de proteína (los valores > 0,5 tienen significación diagnóstica y se recomienda repetir la determinación)
* Individuo afecto sin tratamiento >1 nmol hemicistina/mg de proteína (habitualmente > 2)
* Individuo tratado con buen control terapéutico < 1 nmol hemicistina/mg de proteína. En el caso de que la determinación se realice en granulocitos, el nivel indicativo de buen control terapéutico es >2 nmol hemicistina/mg de proteína
Un valor normal de cistina intragranulocitaria en lactantes de corta edad no excluye el diagnóstico de manera absoluta. De ahí que en casos con alta sospecha de cistinosis, se recomiende realizar una segunda determinación a los 3-6 meses de la primera, cuando esta no sea concluyente [58] (Tabla 3).
Diagnóstico molecular
La cistinosis se confirma con la detección de mutaciones en homocigosis o heterocigosis compuesta en el gen CTNS. Se han descrito > 100 mutaciones diferentes y la más frecuente es la deleción ~57kb de los primeros 10 exones, sobre todo en pacientes con ascendente nor-europeo. Las mutaciones puntuales se traducen en la ausencia de proteína o en una proteína truncada probablemente no funcional [1] [17] [18]. El diagnóstico genético de cistinosis está disponible en muchos centros (Tabla 3).
Screening de cistinosis
El inicio muy precoz de tratamiento con cisteamina retrasa la aparición de complicaciones, incluso previene o aminora el Síndrome de Fanconi, demostrando la utilidad del cribado neonatal [7] [25] [59]. Se ha demostrado que las técnicas de la qPCR (permite detectar la variante patogénica 57-kb en heterocigosis) combinada con la NGS (para confirmar el diagnóstico) puede utilizarse como una herramienta rentable y de alto rendimiento en el cribado neonatal de este tipo de enfermedades [60] [61].
Consejo genético
Al tratarse de una enfermedad autosómica recesiva, la probabilidad de una familia con un hijo afecto, de tener un segundo hijo con cistinosis, es del 25% [1]. Todos los niños nacidos de un progenitor con cistinosis serán portadores obligados [62]. La probabilidad que tiene una mujer con cistinosis de tener un hijo afecto es muy bajo excepto en familias consanguíneas o poblaciones endogámicas [1]. El consejo genético incluye la información referente a las asociaciones de pacientes y las estrategias institucionales en enfermedades minoritarias [63] [64] [65] [66] [67] y sobre las técnicas de diagnóstico prenatal y selección de embriones [63] [68]. Las pruebas de diagnóstico prenatal mediante biopsia de vellosidades coriónicas y amniocentesis son una opción para las parejas de riesgo [61] [62].
7. TRATAMIENTO
Tratamiento sintomático de la afectación renal
Los objetivos del tratamiento incluyen el control del síndrome de Fanconi (Tabla 1) y sus complicaciones (Tablas 4) y (Tabla 5) [1] [27] [69].
La prescripción cautelosa de indometacina en niños pequeños con Síndrome de Fanconi grave consigue reducir el volumen urinario, permitiendo mejorar el estado nutritivo de los pacientes y su tolerancia a los suplementos y medicaciones que precisan. Su uso es más habitual en algunos países europeos, y potencialmente puede conducir a nefrotoxicidad y molestias gastrointestinales, que pueden aumentar la irritación gástrica causada por la cisteamina, por lo que siempre se recomienda ser prudente con su prescripción [35].
Los IECA/ARA-II hipotéticamente contribuirían a retrasar la progresión de la enfermedad glomerular en la cistinosis, pero también pueden causar hipoperfusión renal en sujetos hipovolémicos, por lo que su prescripción debe indicarse con máxima cautela en estos pacientes que suelen ser poliúricos y con frecuencia no toleran estos fármacos [35].
El tratamiento de la ERC seguirá las guías internacionales [70] [71] [72]. En los pacientes trasplantados se recomienda minimizar o evitar los corticoides por la afectación ósea y muscular [18].
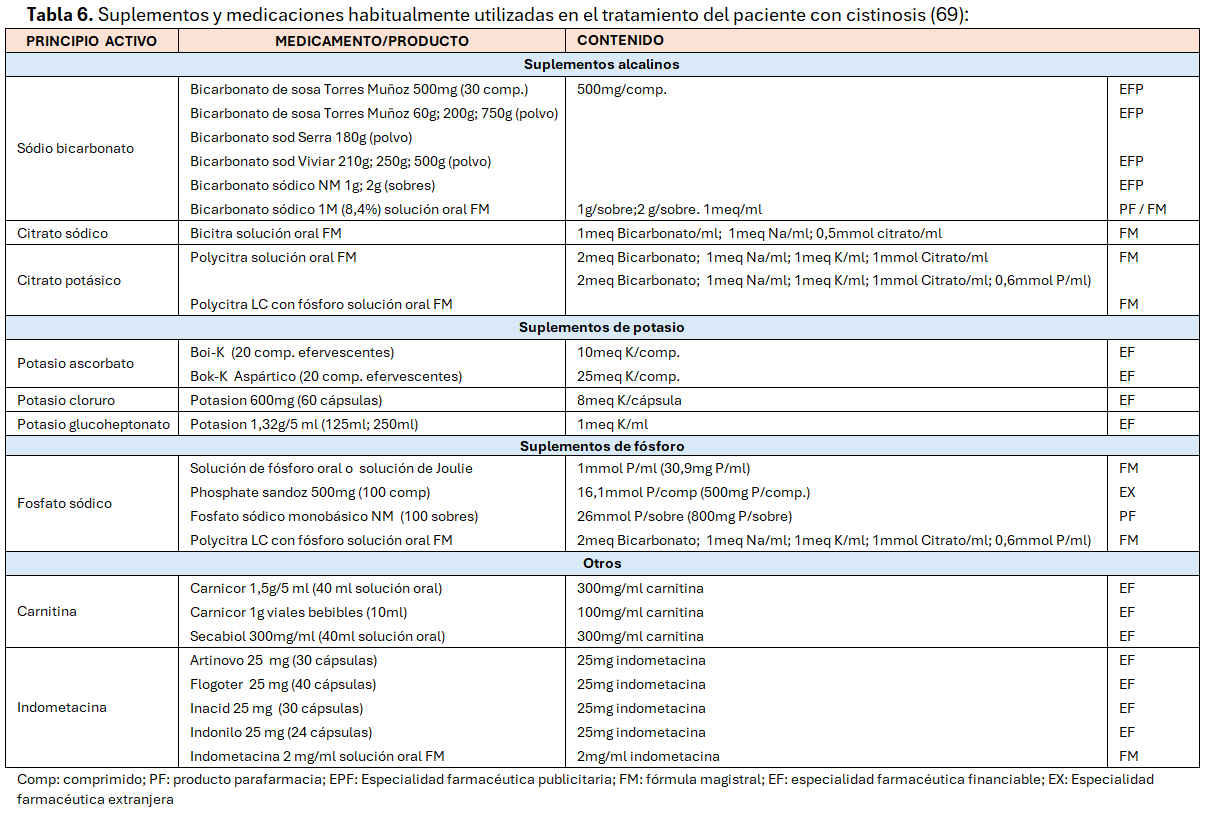
Tratamiento específico con cisteamina (Tabla 6)
A. Cisteamina oral
El único tratamiento específico es la cisteamina oral, que es un quelante de cistina. La cisteamina entra en el lisosoma mediante un transportador desconocido, fragmentando la cistina en cisteína y un compuesto cisteína-cisteamina, que de este modo salen del lisosoma respectivamente a través del transportador de cisteína y del transportador lisina/arginina (PQLC2). La cisteamina ha demostrado de modo indudable su capacidad quelante reduciendo el contenido de cistina de las células, mejorando significativamente el pronóstico de los pacientes [5] [27] [73].
La primera fórmula farmacológica de cisteamina fue Cystagon® (bitartrato de cisteamina oral en cápsulas duras) , autorizado para uso clínico en la década de los 90, y que en la actualidad se conoce como cisteamina de liberación inmediata [5] [74] [75] [76]. En los últimos años se ha desarrollado una fórmula de cisteamina de liberación retardada (Procysbi®), aprobada por la Agencia Europea del Medicamento en el año 2013, y en programa de uso compasivo en nuestro medio [75] [77] [78].
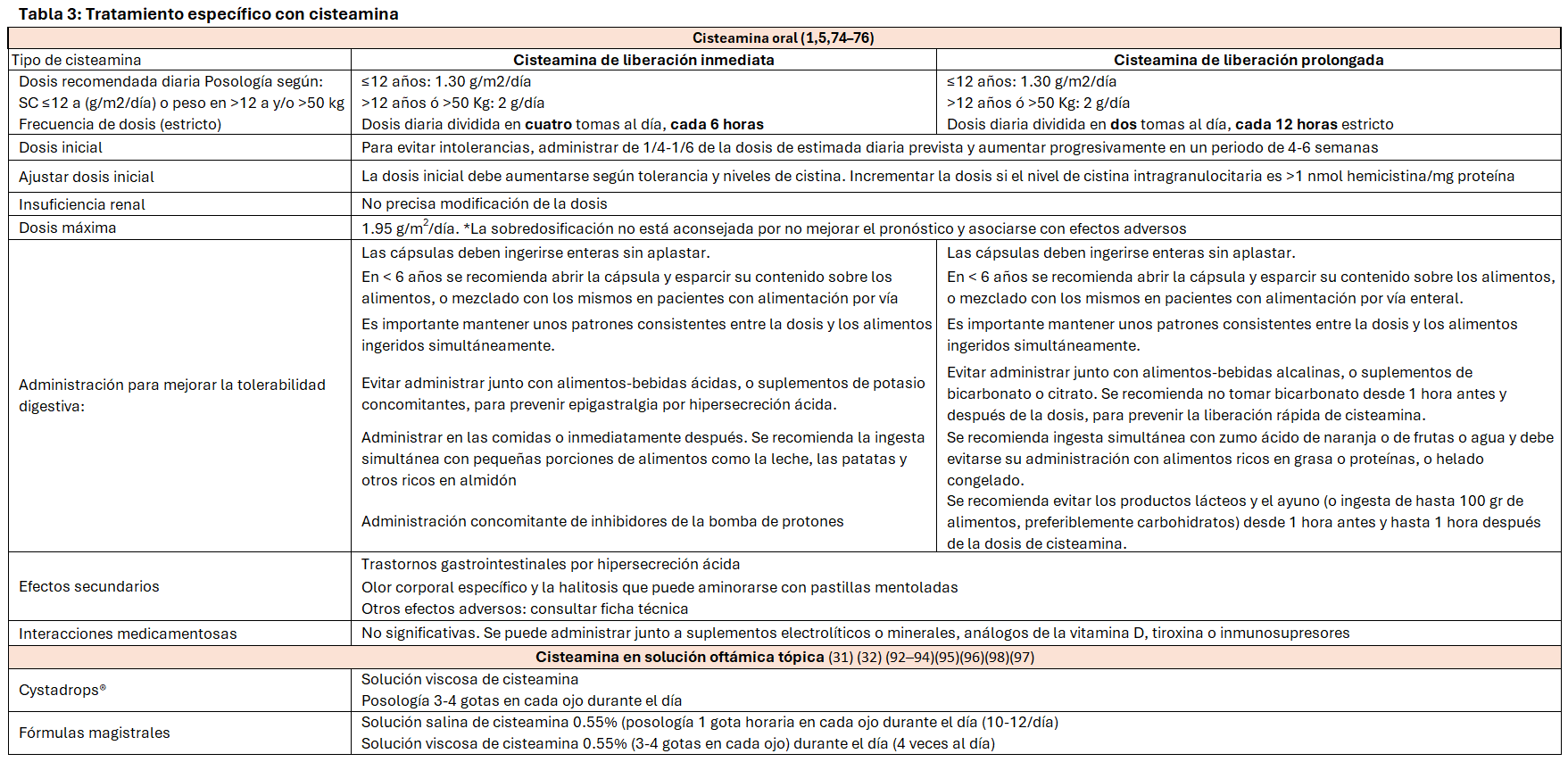
La (Tabla 6), resume la posología y modo de administración de la cisteamina oral. La dosis se calcula con relación a la superficie corporal y se debe alcanzar de modo progresivo hasta una dosis máxima de 1.95 g/m2/día. Dosis más elevadas se relacionan con la aparición de efectos secundarios (dolor óseo, mialgia, estrías y angioendoteliomatosis) [5].
Efectos secundarios
Los efectos secundarios frecuentes de la cisteamina oral son la halitosis producida por los metabolitos de degradación que contienen compuestos sulfúricos volátiles y el mal olor corporal [5] [79], que contribuyen a una pobre adherencia en adolescente y adultos [80]. Otros efectos son la aparición de rash, hipertermia, letargia, neutropenia, convulsiones, y molestias gastrointestinales [52], que pueden aminorarse iniciando el tratamiento de modo gradual [5]. Se ha descrito cuatro casos de colonopatía fibrosante que se asocian al ácido metacrílico (Eudragit L 30D-55), componente del recubrimiento entérico en la cisteamina de liberación retardada [81] [82] [83]. Se ha descrito también un caso encefalopatía aguda y tetraparesis espástica por toxicidad con cisteamina en relación con un déficit de cobre y que se resolvió reduciendo la dosis de cisteamina [84].
Tratamiento en situaciones especiales
Enfermedad renal crónica, diálisis y trasplante: No existe una correlación entre el FG y los niveles de cisteamina en plasma, por lo que no precisa ajuste de dosis por insuficiencia renal, sino que la dosis prescrita se debe ajustar a la cuantificación de los niveles de CiS IL. El trasplante cura las manifestaciones renales de la cistinosis, pero el paciente debe continuar recibiendo cisteamina para la prevención y el tratamiento de la enfermedad sistémica.
Embarazo: El tratamiento con cisteamina debe ser interrumpido por su potencial teratogénico [5].
Beneficios terapéuticos
La cisteamina oral debe introducirse desde el momento del diagnóstico y mantenerse de por vida. Cuando la adherencia es consistente, la cisteamina es capaz de deplecionar hasta un 95% los depósitos celulares de cistina [45]. La reducción de estos depósitos se correlaciona con la gravedad de la cistinosis [5] [27] [30]. Se ha demostrado que la cisteamina prolonga la vida del paciente, retrasa la progresión de la enfermedad renal y el inicio TRS. Así mismo, disminuye la severidad y frecuencia de las manifestaciones extrarrenales [1] [5] [27] [85]. El pronóstico de la enfermedad está directamente relacionado con el inicio precoz y la duración del tratamiento. Incluso cuando el diagnóstico de cistinosis es tardío, la administración de cisteamina ha demostrado beneficios clínicos [5] [27] [61] [85] [86]. Más allá, el inicio del tratamiento con cisteamina antes de los 2 meses de edad ofrece aún mejores resultados observando así una presentación clínica más leve, adecuado crecimiento, preservando la función renal y evitando el síndrome de Fanconi grave y la necesidad de suplementación [21] [35] [59] [87].
Transición de cisteamina de liberación inmediata a prolongada
La cisteamina de liberación prolongada es igual de eficaz (manteniendo un FG y niveles de cistina estables) y ha demostrado varios beneficios como menor tasa de efectos secundarios (olor corporal, halitosis y efectos gastrointestinales), mejora del crecimiento, reducción significativa de los días de hospitalización, favorece la adherencia y mejora la calidad de vida gracias a la dosificación [88] [89] [90].
B. Cisteamina tópica (gotas oftálmicas)
El tratamiento específico de la afectación ocular requiere, además de la cisteamina oral, la administración de cisteamina tópica en forma de gotas oftalmológicas [31] [32] [39].
La cisteamina tópica se utiliza para tratar los depósitos en la córnea, ya que es una estructura avascular [31] [32] [91] [92] [93]. La prescripción recomendada se indica en la (Tabla 6).
Las fórmulas acuosas tradicionales son difíciles de aplicar [94] [95], especialmente en niños, por lo que se han desarrollado formulaciones viscosas para mejorar la adherencia y reducir la frecuencia de instilaciones [96]. Cystadrops® (cysteamine ophthalmic solution 0.37%) fue aprobado en 2017 por la EMA y en 2020 por la FDA [97] [98], mostrando mejoras en la fotofobia y reducción de depósitos tras 3 meses de tratamiento [99].
Para las estructuras oculares no corneales, la cisteamina oral es efectiva y reduce la incidencia de retinopatía. La adherencia al tratamiento oral es clave para evitar la pérdida de visión [27] [31] [32] [39].
Monitorización del tratamiento
En la práctica clínica la monitorización reside en la cuantificación de los niveles de CiS IL en leucocitos totales [55] [56] [57]. Se considera que un nivel ≤1 nmol hemicistina/mg de proteína es indicativo de buen control, aunque es difícil de conseguir. Si la determinación se realiza en granulocitos, el nivel indicativo de buen control terapéutico es >2 nmol hemicistina/mg de proteína [5]. Los requerimientos para la determinación de CiS IL se muestran en la (Tabla 6).
Se recomienda monitorizar los niveles al inicio del tratamiento y mensualmente tras los cambios en la dosis prescrita. En pacientes en seguimiento con niveles estables, se recomienda cada 6 meses. Así mismo, de modo individualizado, se aumentará la frecuencia de monitorización en aquellas situaciones de cambios clínicos (al inicio de diálisis y TxR) [5] [100].
Adherencia al tratamiento
Una mala adherencia al tratamiento implica peor pronóstico con mayor progresión de enfermedad renal y extrarrenal [1] [4] [5] [27].
La monitorización de niveles de CiS IL permite detectar a los pacientes no cumplidores [55] [57]. La adherencia es mayor en niños y disminuye en adolescentes y adultos [5] [27] [80].
Los factores de riesgo de no adherencia incluyen: pauta estricta, problemas de tolerancia, efectos secundarios y la polifarmacia. Otros factores son el conocimiento limitado sobre la enfermedad, la falta de motivación, una transición inadecuada a servicios de adultos y el impacto en la calidad de vida [5] [69] [80] [101].
Se están desarrollando dispositivos electrónicos para mejorar la adherencia [102], y se ha observado mayor adherencia con cisteamina oral de liberación retardada [102] [103].
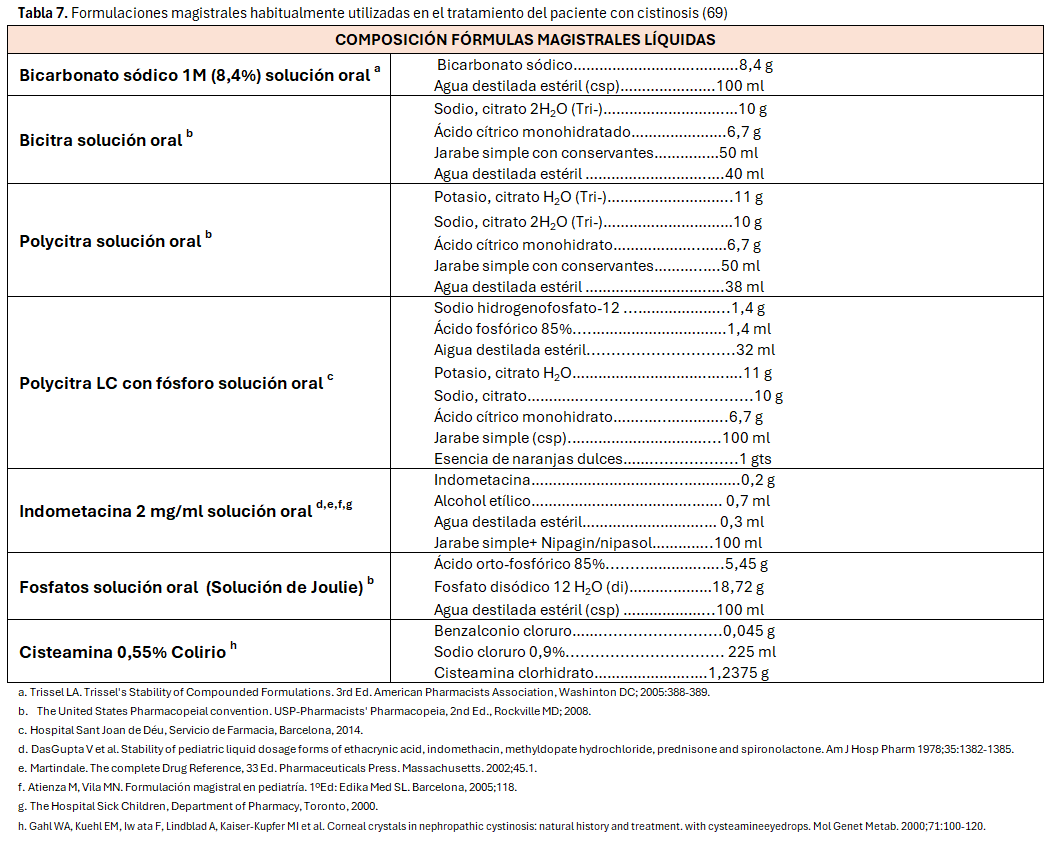
Con el fin de optimizar la adherencia de los pacientes con cistinosis se recomiendan estrategias correctoras de los factores de riesgo y la promoción del autocuidado del paciente (Tabla 7) [104] [105] [106] [107] [108].
Futuros tratamientos
Las limitaciones del tratamiento con cisteamina incluyen la falta de respuesta al Síndrome de Fanconi, la ausencia de curación, los efectos adversos y la complejidad del tratamiento indicado de por vida. Recientemente, se están investigando nuevas moléculas y productos biológicos que actúan sobre la disfunción mitocondrial e inflamación, entre otros mecanismos de disfunción celular tubular, para su uso solo o junto con la cisteamina oral.
Algunos potenciales tratamientos son la molécula ELX-02, un análogo de los aminoglucósidos que permite reparar mutaciones non-sense [109] [110] [111], la terapia génica mediante el trasplante de células madre hematopoyéticas a las que previamente se les ha transferido ex vivo el gen CTNS funcional a través de un lentivirus modificado [112] [113], los inhibidores mTOR [114] o la dieta cetogénica entre otros [115].
8. SALUD REPRODUCTIVA, FERTILIDAD, EMBARAZO Y LACTANCIA
En los varones se produce retraso en la pubertad, hipogonadismo primario y la azoospermia [1] [17] [25] [27]. La espermatogénesis está preservada a nivel testicular en algunos pacientes, lo que ha permitido la paternidad utilizando técnicas de reproducción asistida [25] [114].
En los últimos años, el embarazo se ha convertido en una preocupación importante para las mujeres adultas con cistinosis [115]. Las pacientes en edad fértil deben recibir asesoramiento previo al embarazo [116] [117]. Una serie europea recoge 12 pacientes con 19 embarazos y como resultados, 13 niños nacidos vivos (68,4% de éxito) mostrando así resultados satisfactorios [115], si bien son embarazos de alto riesgo materno por la presencia de preeclampsia, hipertensión, desproporción pelvicocefálica, diabetes gestacional, debilidad muscular respiratoria, parto pretérmino así como el riesgo desconocido de progresión de la cistinosis al interrumpir la cisteamina, y de mayor riesgo fetal (prematuridad, bajo peso y muerte neonatal) [62] [115] [118] [119]. Por este motivo, los embarazos requieren una planificación multidisciplinar previa a la concepción y un seguimiento prenatal [115]. Se han publicado gestaciones en pacientes con ERC, en diálisis o trasplantadas [115] [116].
Aunque los datos son insuficientes, se ha observado toxicidad reproductiva y efecto teratogénico de la cisteamina en animales [115] [116] [117] [120]. La administración de cisteamina está contraindicada durante el embarazo, especialmente durante el primer trimestre, y se recomienda evitarla durante la lactancia [75] [77] [78]. Sin embargo, una reciente publicación ha demostrado que se secretan bajas cantidades de cisteamina en leche materna que probablemente no sean clínicamente significativas [117].
9. MANEJO MULTIDISCIPLINAR Y SEGUIMIENTO DEL PACIENTE ADULTO
Se estima que en España hay diagnosticados ~60 pacientes con cistinosis, la mayoría adolescentes, adultos y/o trasplantados, atendidos en más de 20 centros hospitalarios diferentes [80]. En el 2013, se creó el grupo multidisciplinar T-CiS.bcn para mejorar la atención integral y la transición de adolescentes a servicios de adultos [69] [101].
Es aconsejable la formación de equipos multidisciplinares en el tratamiento de los pacientes adultos con cistinosis, dirigidos por un coordinador (frecuentemente, un nefrólogo o especialista en metabolismo), idealmente en centros especializados, que permita la atención integral y coordinación de los aspectos extrarrenales. Además, se sugieren consultar documentos sobre diagnóstico, tratamiento y seguimiento en diferentes etapas de la vida, abordando temas como fertilidad, planificación familiar y bienestar psicológico [121].
Os dejamos varios documentos publicados para consultar:
- Nephropathic Cystinosis Kidney Disease: Improving Global Outcomes (KDIGO 2016) [17]
- Nephropathic cystinosis: an international consensus document [35]
- Cystinosis in adult and adolescent patients: Recommendations for the comprehensive care of cystinosis [69]
- Expert guidance on the multidisciplinary management of cystinosis in adolescent and adult patients [121]
Aspectos psicosociales
Se recomienda evaluación psicológica durante la adolescencia y transición al adulto, debido a la presencia de dificultades (ansiedad, depresión, baja adherencia al tratamiento, aislamiento social y estrés emocional). Los adolescentes y adultos jóvenes presentan riesgo de desarrollar estas complicaciones, por lo que deben someterse a revisiones periódicas y recibir apoyo psicológico y psicosocial. Sugerimos discutir con el paciente y la familia los objetivos a largo plazo para conseguir una vida independiente, mientras se proporciona un apoyo adecuado durante los cuidados pediátricos. El momento de transferencia a la atención de adultos debe ser individualizado, previamente se habrá realizado una preparación psicosocial que permita la adquisición progresiva de independencia y responsabilidad [122]. Las asociaciones de pacientes brindan un apoyo fundamental al paciente y su familia. En España la asociación de pacientes es el grupo cistinosis (https://www.grupocistinosis.org) [65]
Otras situaciones con alta demanda de soporte psicológico o social son las situaciones médicas críticas (comunicación del diagnóstico, necesidad de inicio de TRS, pérdida del injerto renal y progresión de clínica extrarrenal) o situaciones vitales/sociales (retos de la adolescencia, inicio de educación profesional e incorporación al mundo laboral, relaciones sociales y de pareja, y planificación familiar) [122].
10. CONCEPTOS CLAVE
* La cistinosis es una enfermedad minoritaria autosómica recesiva.
* La cistinosis nefropática es la forma más frecuente y se debe sospechar si existe alteración del crecimiento y/o síndrome de Fanconi.
* El diagnóstico precoz, inicio temprano de cisteamina y la adherencia al tratamiento, condicionan la morbilidad y el pronóstico.
* Es necesario implementar programas de transición al adulto, con el nefrólogo como coordinador principal debido a la naturaleza multisistémica de la enfermedad.
Agradecimientos: Grupo de trabajo T-CiS.bcn y sus documentos de consenso [68] [80]