Técnicas de hemodiálisis
1. INTRODUCCION
Difusión, convección y adsorción son los tres principios físicos que regulan la eliminación de sustancias en la diálisis extracorpórea. Los solutos de pequeño tamaño y gran movilidad se transfieren bien por difusión, en cambio las medianas y grandes moléculas con poca movilidad se eliminan mejor por convección. Las toxinas urémicas unidas a proteínas se eliminan con dificultad por convección y difusión, pero quedan adheridas a las membranas de diálisis, pero la capacidad de adsorción de un dializador es muy limitada y para eliminar toxinas por adsorción hay que recurrir a procedimientos que utilicen cartuchos con sustancias de gran capacidad adsortiva. Las técnicas de diálisis utilizadas en el tratamiento sustitutivo de la insuficiencia renal crónica (IRC) se clasifican en dos grandes grupos según predomine el principio de difusión (HD) o de convección (técnicas convectivas). Más recientemente se han diseñado procedimientos para asociar la adsorción a los principios de difusión y convección.
2. HEMODIALISIS
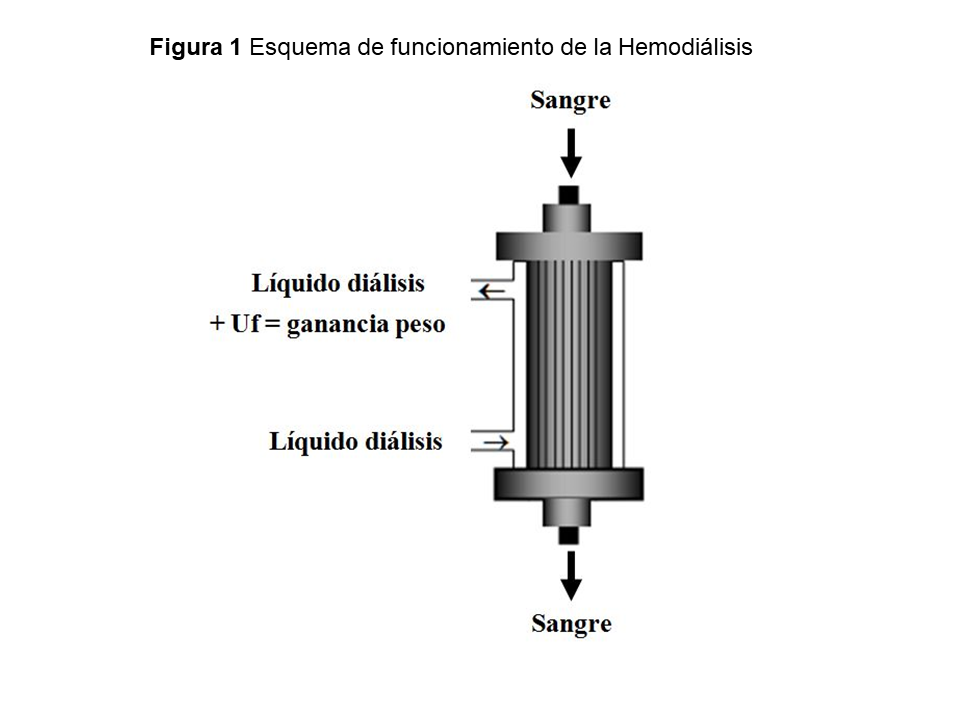
Es el procedimiento de depuración extracorpórea más utilizado en el tratamiento de la IRC. La HD es una técnica fundamentalmente difusiva; la convección queda reservada a la eliminación del agua retenida en el periodo interdiálisis (Figura 1). La superficie del dializador, el flujo de sangre y en menor medida el flujo del baño de diálisis son los factores que regulan la difusión de los pequeños solutos. La eliminación de medianas y grandes moléculas por difusión es menos eficaz y depende fundamentalmente de la permeabilidad de la membrana.
Hay diversas modalidades de HD en función de la eficiencia, permeabilidad y biocompatibilidad del dializador utilizado. La eficiencia del dializador está determinada por la capacidad de eliminación de pequeñas moléculas y se mide por el coeficiente de transferencia de masas para la urea (KoA). El KoA es el aclaramiento máximo teórico de un dializador, dado un flujo infinito tanto de sangre como de líquido de diálisis. Según el KoA del dializador, la HD puede ser de baja (KoA < 500 ml/min), moderada (KoA 500-700) o alta eficiencia (KoA > 700 ml/min) [1]. Esta clasificación, que no tiene en cuenta la biocompatibilidad de la membrana, ha sido muy utilizada en EEUU pero ha tenido poca repercusión en Europa.
La permeabilidad del dializador se mide por su capacidad para la transferencia de agua (coeficiente de ultrafiltración, Kuf) y para la depuración de beta-2-microglobulina. Como ambas suelen ser paralelas, se utiliza el coeficiente de ultrafiltración como índice de permeabilidad. Según el coeficiente de ultrafiltración, la HD pude ser de bajo flujo (Kuf < 20 ml/h/mmHg) o alto flujo (Kuf > 20 ml/h/mmHg) [1], sin embargo, la tendencia actual es considerar la HD de alto flujo cuando el Kuf es superior a 40 ml/h/mmHg. La HD de bajo flujo se subdivide a su vez en la variedad de baja eficacia (Kuf < 10 ml/h/mmHg y KoA < 600 ml/min) y en la variedad de alta eficacia (Kuf 10-20 ml/h/mmHg y KoA > 600ml/min). La HD de bajo flujo, también llamada HD convencional, puede usar dializadores con membrana de derivados de la celulosa de baja biocompatibilidad (actualmente en desuso) o membrana sintética. La HD de alto flujo suele utilizar una membrana sintética biocompatible, y aunque el transporte sigue siendo difusivo, existe más transporte convectivo que en la HD de bajo flujo. Se precisa de baño de diálisis puro por el fenómeno de retrofiltración asociado a los dializadores de alta permeabilidad. Para una mayor eficacia, se recomiendan flujos de sangre elevados.
Comparada con la HD convencional, la de alto flujo se asocia a una mejor depuración de medianas moléculas. Tres ensayos clínicos han analizado la supervivencia como objetivo primario [2][3][4] y aunque globalmente no se demostró una diferencia en la mortalidad entre el grupo de enfermos tratado con HD de alto flujo con respecto al grupo tratado con HD de bajo flujo, sí que se demostró una mayor supervivencia en determinados subgrupos de enfermos como son los enfermos diabéticos o desnutridos [5]. Los resultados favorables observados con la HD de alto flujo, pueden ser atribuidos no solo a la calidad de la membrana (biocompatibilidad y permeabilidad) sino también a la del baño de diálisis. Junto con la hemodiafiltración on line, la HD de alto flujo es la técnica de HD de referencia utilizada actualmente en la mayoría de las unidades de HD.
Recientemente se han introducido unos dializadores con un nuevo tipo de membrana, llamadas de medio cut-off (MCO) con un punto de corte de 65 KDa, que permiten eliminar un mayor número de moléculas de mediano PM pero con menor pérdida de albúmina. Además de presentar poros de mayor diámetro y distribución más homogénea, los capilares de esta membrana presentan un menor diámetro interno que favorece la caída de presión en el compartimento sanguíneo a lo largo del dializador favoreciendo la retrofiltración, asociando un mayor transporte convectivo interno, lo que se ha denominado “hemodiafiltración interna”. Esto se traduce en un mayor coeficiente de cribado para moléculas de medio PM, que se ha calculado cercano a 0.9 para moléculas como la beta-2 microglobulina.
La HD con este tipo de membrana recibe el nombre de HD extendida y los resultados iniciales indican que es una técnica segura que consigue una eliminación de medianas y grandes moléculas similar a la conseguida con el transporte convectivo (hemodiafiltración on line), e incluso podría ser superior en el aclaramiento de moléculas de mayor PM [6]. Hay que esperar a la obtención de más resultados para determinar la utilidad e indicaciones de esta nueva técnica de HD, así como de su impacto en la supervivencia.
3. TECNICAS CONVECTIVAS
Las técnicas convectivas surgen con la finalidad de aumentar la eliminación de las moléculas de mediano y gran tamaño que se transfieren mal por difusión. La transferencia de solutos en la convección se realiza mediante el principio de arrastre por flujo y depende del tamaño del poro de la membrana y de la tasa de ultrafiltración. Las técnicas convectivas usan una membrana sintética biocompatible de alto flujo y realizan una ultrafiltración superior a la necesaria para eliminar el líquido acumulado por el enfermo entre dos sesiones de diálisis. El exceso de volumen extraído debe ser repuesto con un líquido de reposición de composición fisiológica. El volumen convectivo es el equivalente al total de líquido ultrafiltrado, y el volumen de reposición es el volumen convectivo menos el volumen correspondiente a la ganancia de peso del periodo interdiálisis.
Las técnicas convectivas pueden utilizar exclusivamente el principio de convección sin difusión (hemofiltración), o tratarse de técnicas mixtas que combinan el principio de difusión con diversas formas de convección (hemodiafiltración).
Los procedimientos convectivos pueden clasificarse a su vez en dos grupos según que el líquido de sustitución sea una solución de electrolitos contenidos en bolsas (convección clásica) o el propio baño de diálisis convenientemente tratado (convección "on-line").
3. 1. TECNICAS CONVECTIVAS CLASICAS
En la convección clásica, el líquido de reposición es introducido en la línea venosa después del dializador (modo postdilucional). La extracción del agua plasmática produce un aumento progresivo de la viscosidad de la sangre conforme avanza por el dializador. La hemoconcentración junto con la adsorción de proteínas en la membrana del dializador y la acumulación en la vecindad de la membrana de grandes moléculas que no pueden atravesarla (fenómeno de polarización) reducen el transporte por difusión y convección. Estos fenómenos son inversamente proporcionales al flujo de sangre y directamente proporcionales a la tasa de ultrafiltración, al hematocrito y la concentración plasmática de proteínas. En las técnicas convectivas en modo postdilucional, la tasa de ultrafiltración está supeditada al flujo de sangre, en concreto a la fracción de filtración (relación entre la tasa de ultrafiltración y el flujo de sangre, expresado en porcentaje). Se acepta que la fracción de filtración no debe superar el 30%, ya que valores más elevados pueden afectar al rendimiento de dializador con aumento excesivo de la presión transmembrana y activación de las alarmas del sistema.
Las modalidades clásicas de hemofiltración y hemodiafiltración son técnicas complejas que exigen una perfecta sincronización entre las bombas de ultrafiltración y de infusión, y son más costosas por los líquidos de reposición. No llegaron a demostrar unos resultados claramente superiores a la HD y nunca consiguieron convertirse en una alternativa a la misma.
Resumimos a continuación las principales técnicas convectivas clásicas utilizadas.
3.1.1. Hemofiltración
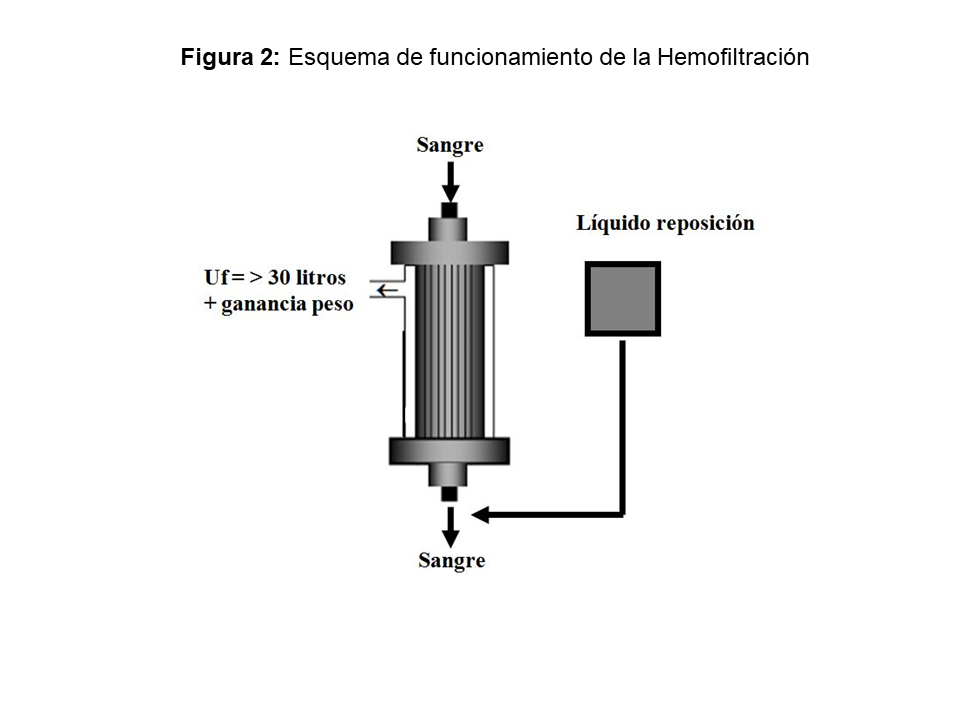
La depuración de solutos se realiza exclusivamente por el principio de convección, sin baño de diálisis, a semejanza del funcionamiento del riñón nativo (Figura 2). La eliminación de solutos en la hemofiltración depende del coeficiente de cribado (cociente entre la concentración del soluto en el ultrafiltrado y en el agua del plasma) y de la tasa de ultrafiltración.
Para conseguir una dosis de diálisis adecuada según los criterios basados en la eliminación de urea, es necesario conseguir en cada enfermo un volumen convectivo equivalente a su volumen de distribución de la urea (un mínimo de 30 litros). Para conseguir una tasa tan alta de ultrafiltración es necesario un flujo de sangre superior a los 400 ml/min. Este requisito y el elevado volumen de líquido de reposición requerido hicieron que esta técnica, tan antigua como la diálisis, tuviera un escaso desarrollo.
3.1.2. Hemodiafiltración convencional
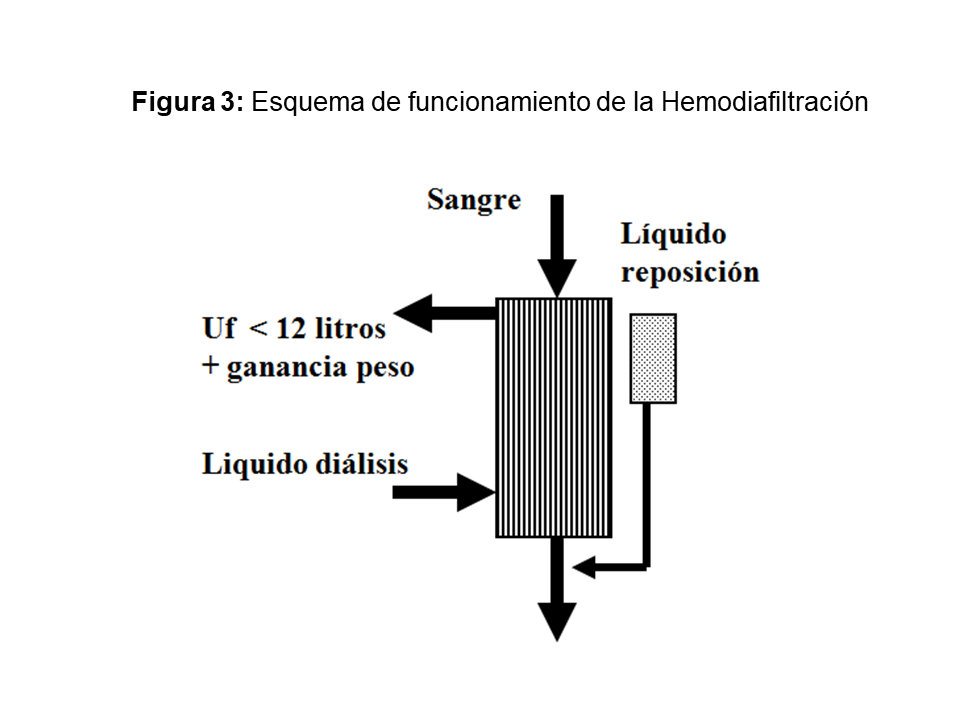
La hemodiafiltración combina los dos principios de difusión y convección. Con flujos arteriales menores y tasas de ultrafiltración de hasta 12 litros por sesión, se consigue un aclaramiento de pequeñas moléculas muy superior a la hemofiltración, con una eliminación de medianas y grandes moléculas intermedia entre la HD y la hemofiltración (Figura 3).
Hay que resaltar que difusión y convección tienen un efecto competitivo en la transferencia de moléculas. La eliminación difusiva de un soluto disminuye su concentración plasmática conforme progresa la sangre por el dializador y reduce su eliminación convectiva que es proporcional a su concentración en el compartimento sanguíneo. Por otra parte la eliminación convectiva aumenta la concentración del soluto en el compartimento del baño de diálisis con disminución del gradiente de concentración transmembrana y de la eliminación difusiva.
Además de la hemodiafiltración convencional, hay otras dos modalidades que utilizan los principios de la hemodiafiltración: la "Acetate Free Biofiltration" (AFB) y la Paired Filtration Dialysis (PFD).
3.1.3. Acetate Free Biofiltration (AFB)
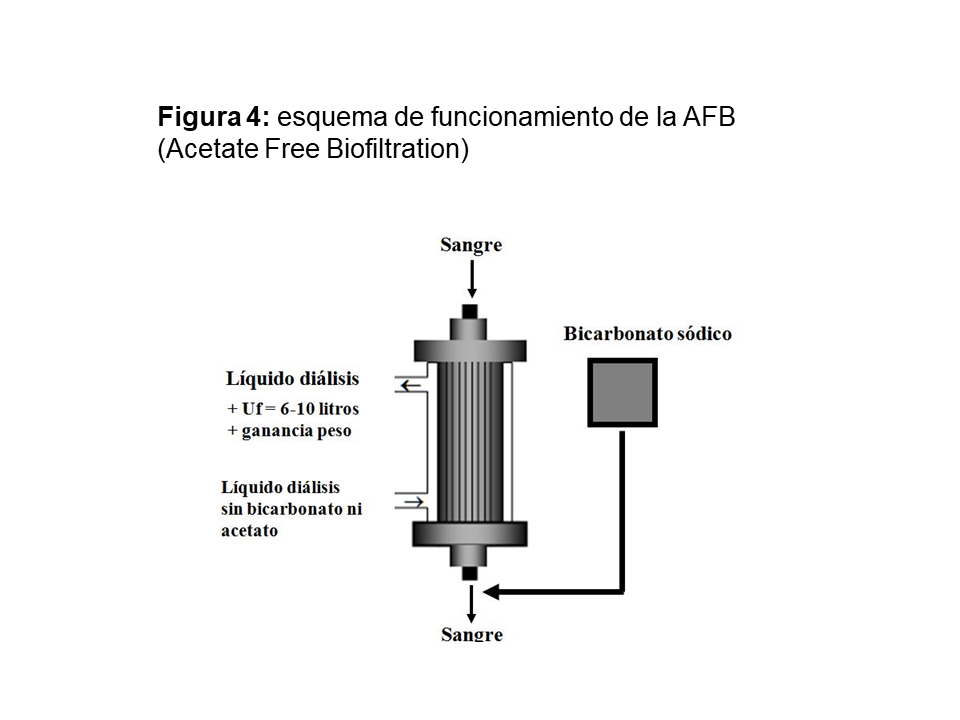
La AFB es una técnica de hemodiafiltración en la que el líquido de diálisis no contiene ninguna base (ni acetato ni bicarbonato) (Figura 4). La tasa de ultrafiltración extra es de 6-12 litros y el líquido de reposición es una solución de bicarbonato sódico. El objetivo de esta técnica es eliminar el acetato del baño de diálisis y controlar el equilibrio ácido-base de una forma individualizada. Para garantizar un correcto ajuste, es preciso realizar controles de las concentraciones de bicarbonato en sangre pre y postdiálisis al inicio de la técnica y siempre que se modifiquen las condiciones de la diálisis (tiempo, flujo arterial, superficie del dializador y volumen del ultrafiltrado), y ajustar la conductividad del baño de diálisis para evitar la sobrecarga de sodio.
Una modalidad de AFB es la AFB-K que utiliza una concentración descendente de potasio en el baño de diálisis para mantener un gradiente constante con su concentración en plasma. El objetivo de esta técnica es reducir la aparición de arritmias durante la diálisis enfermos con propensión a las mismas.
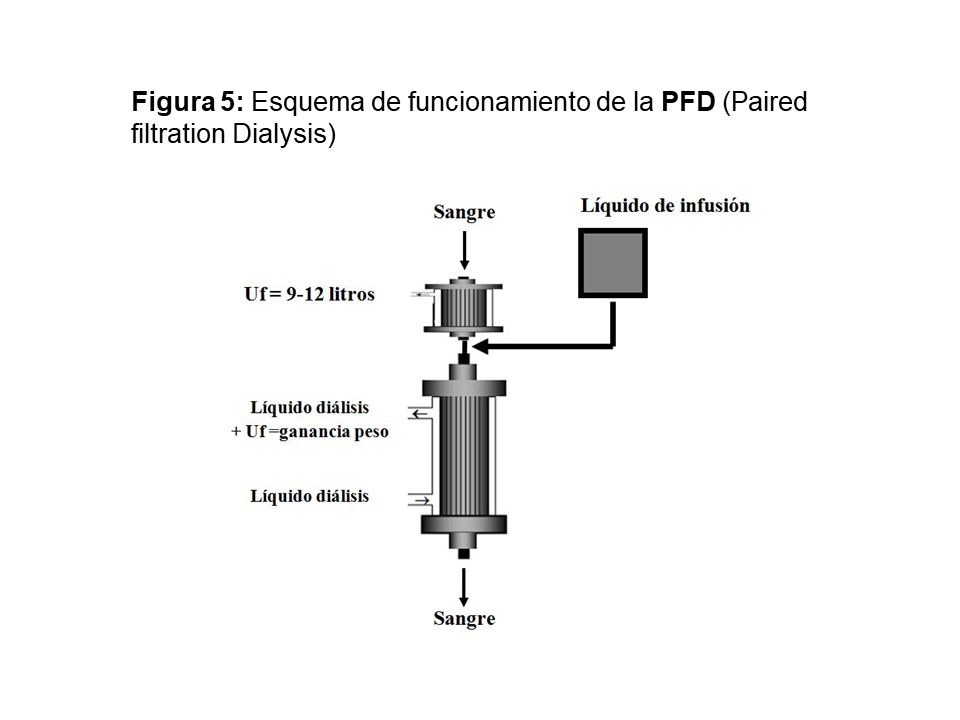
3.1.4. Paired Filtration Dialysis (PFD)
Es una técnica de hemodiafiltración diseñada para evitar la interferencia entre los transportes convectivo y difusivo. Consta de dos dializadores acoplados en serie. En el primero se realiza una ultrafiltración de 9-12 litros y en el segundo una HD tradicional; en la conexión existente entre ambos se efectúa la reinfusión del líquido de reposición (Figura 5).
La PFD con regeneración del ultrafiltrado (PFD-Carbón) es una modalidad derivada de la anterior. El líquido ultrafiltrado en la primera cámara es reinfundido tras ser regenerado en un cartucho que adsorbe toxinas urémicas. Evita la necesidad de líquido de reposición y aumenta la seguridad de la técnica ya que el volumen ultrafiltrado es reinfundido sin posibilidad de desequilibrio entre ultrafiltración y reinfusión.
3.2. CONVECCIÓN "ON-LINE"
La posibilidad de usar el baño de diálisis como líquido de sustitución fue el avance que renovó el interés por las técnicas convectivas. Inicialmente, se utilizó como líquido de reposición un baño de diálisis que previamente había sido esterilizado y almacenado en recipientes cerrados (preparación "off-line" del líquido de reposición). Pero fue la infusión directa del baño de diálisis conforme se va produciendo en el monitor (preparación "on-line"), sin necesidad de almacenamiento externo, el gran avance técnico que permitió la expansión de las técnicas convectivas en el tratamiento de la IRC.
Para poderse usar como líquido de reposición, el baño de diálisis debe ser de alta calidad y reunir las condiciones del denominado baño ultrapuro. Tiene que ser fabricado con un agua de gran pureza obtenida con doble sistema de ósmosis inversa, debe estar en continua recirculación para evitar focos de contaminación por estancamiento y antes de ser infundido en el circuito sanguíneo, debe atravesar al menos dos filtros de endotoxinas intercalados en el circuito del baño de diálisis.
Esta técnica de producción "on-line" permite utilizar grandes volúmenes de reposición sin incremento del coste. Se supera así una de las principales limitaciones de la convección clásica y se consigue un alto rendimiento en la eliminación de sustancias por convección. Un módulo de balance de fluidos o un sistema similar con medidores de flujo, garantiza una exacta equivalencia en el tiempo entre el exceso de volumen plasmático extraído y el volumen repuesto. La hemodiafiltración “on-line” (HDF-OL) precisa la utilización de un dializador de alta permeabilidad con un Kuf superior a 40 ml/h/mmHg y un coeficiente de cribado para la beta-2-microglobulina superior a 0,6.
Aunque la convección "on-line" también se ha aplicado a las técnicas de hemofiltración y PFD, es la HDF-OL la que ha logrado un mayor desarrollo y en la actualidad, es la técnica convectiva por antonomasia.
3.2.1. Hemodiafiltración “on-line”
Ver NAD: Hemodiafiltración on-line
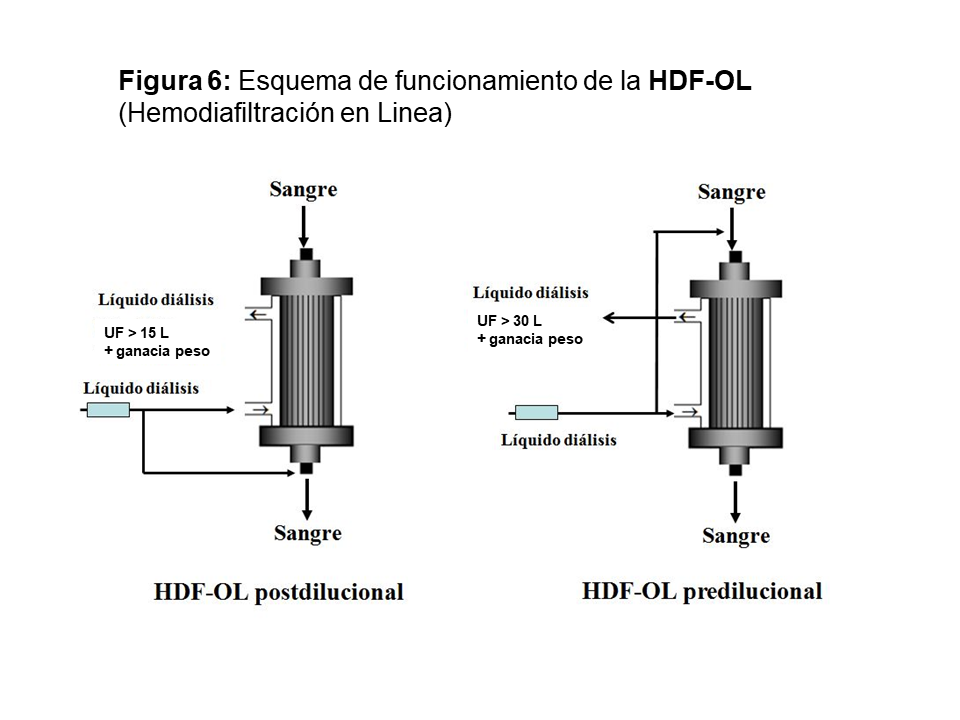
La HDF-OL con infusión del líquido de sustitución en modo postdilucional es el procedimiento que consigue los mejores resultados en la depuración de todo tipo de moléculas (Figura 6). Con los avances tecnológicos, se ha aumentado el volumen ultrafiltrado y de reinfusión. La Guía Clínica para Unidades de HD de la Sociedad Española de Nefrología, en su revisión del año 2020 recomienda un alto volumen de reposición, con el objetivo de alcanzar más de 21 litros por sesión (hemodiafiltración postdilucional de alto volumen) [7].
Como se describió previamente, una fracción de filtración mayor del 30% puede ocasionar problemas de rendimiento de dializador con aumento de la presión transmembrana y aparición de alarmas. Para evitar estos problemas los monitores actuales regulan de forma automática la tasa de ultrafiltración en función de flujo de sangre y de la presión transmembrana. El volumen de líquido conseguido por convección va a depender fundamentalmente de dos variables: el flujo de sangre y la duración de la sesión. Para obtener un volumen convectivo adecuado en una sesión de 4 horas de duración, es necesario un flujo mínimo de sangre de 350 ml/min. Si no es posible alcanzar este flujo de sangre, habría que aumentar la duración de la sesión.
La libre disposición de líquido de reposición ha permitido el desarrollo de diferentes modos de HDF-OL para su empleo en enfermos con hematocrito alto y en los que el flujo arterial no pueda alcanzar las altas tasas requeridas. La infusión del líquido de reposición antes de entrar la sangre en el dializador (modo predilucional) disminuye los problemas derivados de la hemoconcentración y polarización (Figura 6). El descenso de la concentración de solutos en el agua del plasma como consecuencia de la hemodilución reduce su transferencia por difusión y por convección. Aunque se intenta compensar esta pérdida de eficacia aumentando el volumen de recambio (como mínimo debe ser el doble que en el modo postdilucional), el rendimiento del modo predilucional siempre es inferior al postdilucional.
Para mejorar la eficacia del modo predilucional y evitar los problemas derivados del aumento de la presión transmembrana en el postdilucional, han surgido diversas modalidades de hemodiafiltración "on-line". Referimos a continuación las más conocidas.
-Modalidad mixta simultánea: el líquido de reposición es infundido pre y postdializador de forma simultánea.
-Modalidad secuencial: inicio en modo postdilución y paso al predilución cuando la presión transmembrana alcanza un determinado valor.
-Modalidad "mid-dilution": utiliza un dializador especial con dos haces de capilares (central y anillo periférico); la sangre circula sucesivamente por ambos haces en recorrido de ida y vuelta, y entre ambos ser realiza la infusión del líquido de reposición; la primera parte del recorrido se comporta como una hemodiafiltración en modo postdilucional y la segunda como una hemodiafiltración en modo predilucional.
Todas estas modalidades consiguen unos resultados intermedios entre las modalidades pre y postdilucional.
3.2.2. Hemodiafiltración con capacidad adsortiva (HFR)
Las toxinas urémicas unidas a proteínas son difíciles de eliminar con cualquier estrategia de diálisis. En la actualidad se han desarrollado procedimientos, que a la técnica de difusión-convección añaden un proceso de adsorción capaz de retener moléculas unidas a proteínas.
Uno de estos procedimientos es la técnica de HFR. En una primera fase la sangre pasa por un dializador de alta permeabilidad (fase convectiva) generando un ultrafiltrado que se hace pasar por una resina hidrofóbica con gran capacidad de adsorción (fase adsortiva). Posteriormente el ultrafiltrado libre de los solutos adheridos a la resina se devuelve a la sangre, que pasa por un segundo dializador para eliminar las pequeñas moléculas y realizar la ultrafiltración necesaria para conseguir el peso seco (fase difusiva). Algunos estudios han demostrado con esta técnica un descenso en las concentraciones plasmática de p-cresol y de mediadores inflamatorios [8], aunque son necesarios más estudios que avalen estos resultados.
Otra técnica que puede contribuir a eliminar toxinas unidas a proteínas es combinar la adsorción con la hemodiafiltración utilizando membranas con mayor capacidad adsortiva, como el polimetilmetacrilato (PMMA).
RESULTADOS DE LA HEMODIAFILTRACION “ON-LINE”
El estudio DOPPS fue el primero en describir una mejor supervivencia en los pacientes en hemodiafiltración cuando se alcanzara un volumen convectivo mínimo (15–25 L/sesión) [9]. Numerosos estudios observacionales describieron que la hemodiafiltración “on-line” proporcionaba mejores resultados en mortalidad y morbilidad que la HD. Muchos de estos estudios presentaban problemas metodológicos como la selección positiva de enfermos, la ausencia de grupo control, y la comparación de la hemodiafiltración con técnicas de HD de bajo flujo. En estos últimos casos no podía dilucidarse si los beneficios clínicos objetivados con la hemodiafiltración “on-line” eran debidos al empleo de membrana de alto flujo, al baño de diálisis ultrapuro o a la propia convección [10][11][12]. Sin embargo, fueron los resultados de cuatro estudios prospectivos, multicéntricos, con control aleatorizado, realizados en un número importante de enfermos los que pusieron de manifiesto la relevancia clínica de la hemodiafiltración “on-line”. El primero (CONTRAST Study) comparaba la hemodiafiltración “on-line” con la HD de bajo flujo [13], y los tres estudios restantes (Turkish HDF Study, ESHOL Study y French Study) lo hacían con la HD de alto flujo [14][15][16]. En el estudio ESHOL [15] se alcanzó un alto volumen convectivo (≥ 22,9 L/sesión) en el grupo de HDF-OL, demostrando una disminución del 30% del riesgo de mortalidad en el grupo de HDF-OL con respecto el grupo tratado con HD-alto flujo. Los resultados de estos ensayos clínicos y del metaanálisis realizado con los datos de todos ellos [17] demostraron que la HDF-O reduce la mortalidad global y de origen cardiovascular, principalmente cuando se consiguen volúmenes elevados de transporte convectivo, concluyendo que el mejor resultado en cuanto a reducción de la mortalidad se obtienen si se alcanza un volumen convectivo > 23 L/sesión, equivalente a un volumen de infusión de 21 L/sesión en pacientes con una ultrafiltración media de 2 L/sesión [17].
Más recientemente, algunos estudios observacionales han descrito que un transporte convectivo aún superior a 25 litros/sesión podría aumentar la depuración de toxinas unidas a proteínas [18], aunque son necesarios más estudios para demostrar la utilidad clínica de estas observaciones clínicas.
Las técnicas de convección "on-line" pueden ser consideradas seguras si tenemos en cuenta que tras más de 15 años de utilización no se han publicado complicaciones, efectos secundarios o peores resultados de los conseguidos con la HD de alto flujo.
La necesidad de asegurar una alta calidad del agua obliga a aumentar la frecuencia de los controles periódicos del agua y del baño de diálisis.
RESULTADOS DE LA HEMODIALISIS EXTENDIDA
Ver NAD: Hemodiálisis extendida
Desde hace pocos años, disponemos de dializadores de medio punto de corte (medium cut-off, MCO), que permiten eliminar moléculas de hasta 45 kDa, como las cadenas ligeras de las inmunoglobulinas, pero con una menor pérdida de albúmina [18]. Con esta técnica, la depuración de medianas moléculas es superior a la HD de alto flujo, con resultados variables con respecto la HDF-OL [19][20][21]. En el momento actual, los beneficios clínicos de esta técnica con respecto la HDF-OL son inciertos y deben ser avalados en futuros ensayos clínicos que comparen ambas.
RESULTADOS DE LA HEMODIAFILTRACION CON CAPACIDAD ADSORTIVA
Las toxinas urémicas unidas a proteínas se eliminan mal con la HD de alto flujo, la HDF-OL y la HD extendida, habiéndose relacionado el acúmulo de estas toxinas con un aumento de la morbilidad cardiovascular [23]. Aunque se ha postulado la adsorción como un mecanismo para aumentar la eliminación de estas sustancias, en el momento actual es difícil establecer la relevancia clínica de la adsorción sobre la morbi-mortalidad de los pacientes en diálisis.
CONCLUSION
La HD de alto flujo y la HDF-OL son las técnicas de referencia en el tratamiento con HD de la ERC, siendo la HDF-OL la que más se ha generalizado en los últimos años, debido a la facilidad en la preparación del líquido de sustitución y a que no conlleva un mayor coste. Ambas técnicas precisan de membranas de alta permeabilidad y buena calidad del agua de diálisis, que en el caso de la HDF-OL precisa de líquido de diálisis ultrapuro. Los resultados disponibles de los ensayos clínicos han demostrado que la HDF-OL reduce de forma significativa la mortalidad cuando se obtiene un alto volumen convectivo. El reto de esta técnica es conseguir un alto volumen convectivo de forma generalizada.
Más recientemente, ha aparecido la HD extendida que es una técnica de HD que utiliza un dializador con un poro de mayor tamaño, de medio cut-off, y un diámetro interno del capilar menor favoreciendo la retrofiltración. Se ha descrito una eliminación de medianas y grandes moléculas similar a la HDF-OL, pero aún se desconoce el impacto sobre la supervivencia con respecto la HDF-OL.
Finalmente, las toxinas urémicas unidas a proteínas son difíciles de eliminar con las técnicas de diálisis actuales. El alto transporte convectivo y la incorporación de resinas o dializadores con capacidad adsortiva a las técnicas actuales podrían aumentar la eliminación de estas toxinas. Sin embargo, el papel de la adición de estas técnicas adsortivas sobre la supervivencia no está bien establecido y hay que tener presente que para su generalización debería ser de fácil aplicación sin incrementos significativos del coste.