Monitores de Hemodiálisis
Índice:
1. Concepto e introducción
2. Elementos de los monitores de hemodiálisis (HD):
2.a Circuito sanguíneo
2.b Circuito hidráulico. Fabricación del líquido de diálisis (LD).
2.c Sistemas de monitorización:
2.c.1 Ajustes básicos
2.c.2 Monitorización del aclaramiento
2.c.3 Sistemas para mejorar la tolerancia hemodinámica
a. Monitorización del hematocrito y volumen relativo de sangre
b. Balance térmico
c. Medida de saturación de oxígeno
2.c.4 Sistemas de seguimiento del acceso vascular
2.c.5 Monitorización del balance de sodio (sal)
3. Sistemas de retroalimentación o biofeedback
3.a Automatización de la prescripción de sodio
3.b Automatización del volumen relativo sanguíneo (VRS)
3.b.1 Modificación de Uf y concentración de sodio en LD ajustado a VRS
3.b.2 Modificación de Uf ajustado a VRS
3.b.3 Modificación de concentración de sodio en LD ajustado a VRS.
3.b.4 Modificación de la UF en función de la presión arterial (PA) del paciente.
4. Los monitores y la optimización de la hemodiafiltración en línea.
5. Sistema informático. Comunicaciones del monitor.
6. Sistemas de automatización de la preparación, conexión, tratamiento, desconexión y desinfección.
7. Tipos y funcionalidad de los monitores de HD 2025
7.a Comparativa.
7.b La opinión de la enfermería.
7.c Monitores para HD domiciliaria
8. Posibles mejoras.
Anexo 1
1. Concepto e introducción
El monitor de hemodiálisis (HD), también conocido como riñón artificial, es una máquina capaz de realizar algunas de las funciones renales para el tratamiento de los pacientes con insuficiencia renal avanzada. Para llevar a cabo una hemodiálisis (HD), se necesita además del monitor, un dializador, agua purificada, los concentrados (ácido y de bicarbonato), las líneas y conexiones con el acceso vascular. La evolución de estas máquinas ha logrado mejorar la tolerancia a la técnica y la seguridad del paciente.
Este capítulo está dirigido a conocer el monitor de HD. En él podemos distinguir 3 elementos esenciales: el circuito sanguíneo; el circuito hidráulico con un sistema generador de líquido de diálisis (LD) y sistemas de monitorización para que la HD pueda realizarse correctamente y de forma segura.
2.Elementos de los monitores de hemodiálisis (HD):
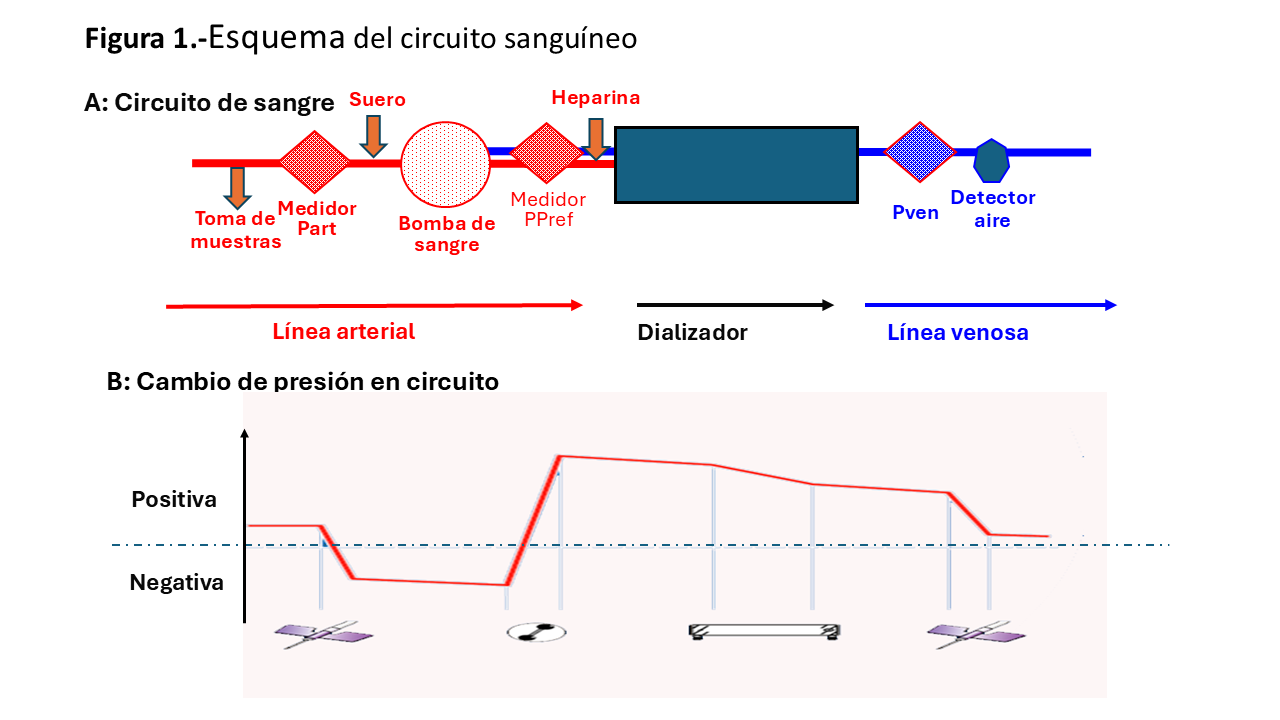
2.a Circuito sanguíneo (Figura 1) [1]
El flujo de sangre necesario para la HD proviene del acceso vascular (AV); la sangre fluye desde la línea arterial hacia el dializador y vuelve al paciente a través de la línea venosa. El elemento que moviliza la sangre en el circuito es una bomba peristáltica de rodillos, que hace que progrese la sangre mediante la compresión de un segmento colapsable denominado segmento de bomba y ubicado en la línea arterial. Dicha compresión genera una presión negativa, de succión, antes de la bomba, que lleva la sangre al interior de la línea. Como la presión prebomba es negativa y la posbomba es positiva, cuando los rodillos pasan por una zona donde no comprimen, la sangre retrocede (cambia su sentido) y ese movimiento se define como pulso. El pulso es mayor cuanta más diferencia hay entre las presiones pre y posbomba y también cuanto mayor sea el número de rodillos. Dos rodillos implican dos pulsos por vuelta, tres rodillos, tres pulsos por vuelta y así, sucesivamente. Cuantos más rodillos, el flujo tendrá más pulsos, pero serán menos intensos. Además, aumentará el riesgo de hemólisis y de lesión por estrés del material del segmento de la bomba. Otro factor que influye en el pulso es la viscosidad de la sangre. A mayor viscosidad del fluido habrá más pulso porque se necesita más presión para movilizarlo. Como consecuencia de la presión negativa de succión, si hay una rotura de línea arterial, antes de la bomba, puede entrar aire rápidamente en el dializador, disminuyendo la eficacia de la diálisis y facilitando su coagulación.
Para que el circuito funcione correctamente, hay una serie de controladores:
Medidor de presión en línea arterial (Part), próximo a la bomba de sangre. Protege de una excesiva succión por la bomba. Es un valor negativo, que dependerá de los flujos de acceso y bomba (Qb), de la viscosidad de la sangre y del diámetro y permeabilidad (ausencia de obstrucción) de la aguja o catéter. Si la medición está fuera de rango se activará la alarma y detendrá la bomba de sangre.
Los monitores de HD calculan el flujo sanguíneo (FS o Qb) mediante un algoritmo teniendo en cuenta la velocidad de la bomba peristáltica de rodillos, el volumen del segmento de bomba de la línea y la Part. Si la Part es muy negativa el cálculo es inexacto y el Qb real inferior al calculado.
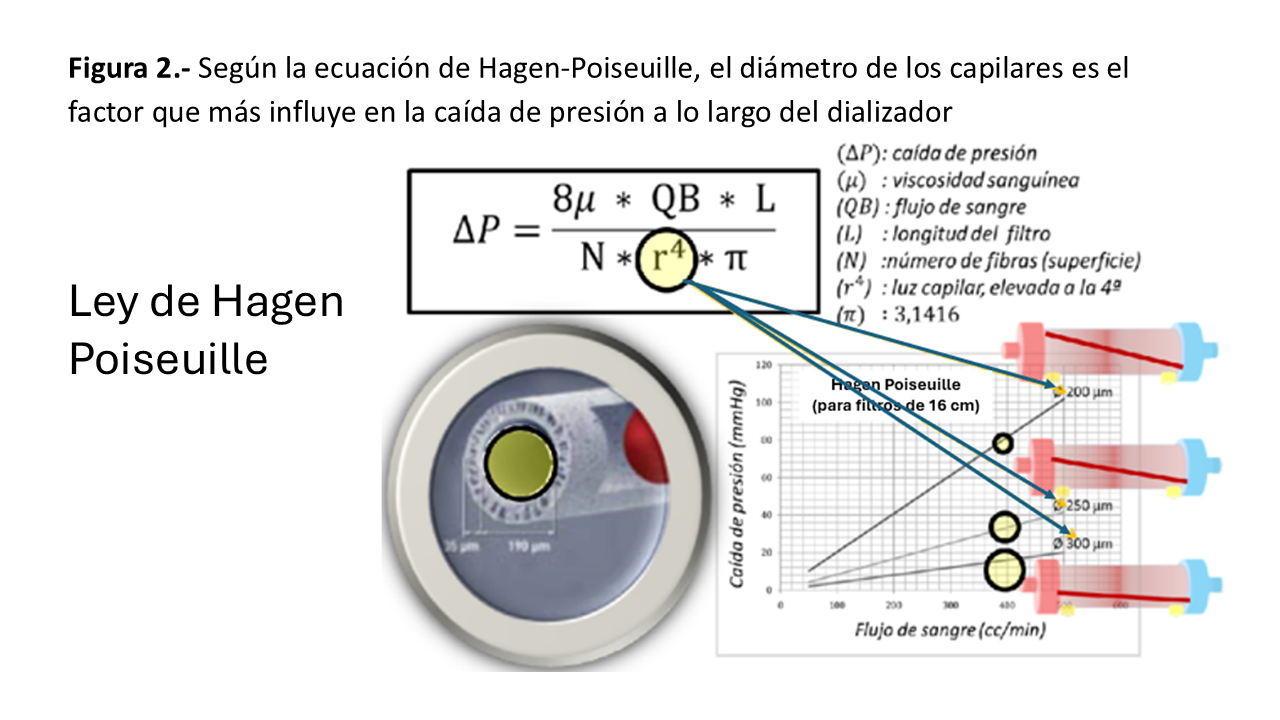
Medidor de presión prefiltro (Ppref), después de la bomba y antes del dializador. Se obtiene una presión positiva que es la más elevada del circuito, no debiendo superar los 700 mmHg. Va a depender del Qb, de la viscosidad de la sangre y de la resistencia en el dializador. El dializador es el elemento determinante de la Ppref y dentro de éste, acorde a la ley de Hagen-Poiseuille (Figura 2), el factor que más influye y de forma inversa, es el diámetro capilar. En la fórmula está elevado a la cuarta potencia el radio interno, siendo menos importantes la longitud y el número de fibras o la superficie del dializador. Se utiliza, junto a otras presiones del circuito sanguíneo y del LD para calcular la presión transmembrana (PTM), que no es visible en todos los monitores. De hecho, no todos los monitores miden la presión prefiltro.
Medidor de presión venosa (Pven), situado después del dializador, mide la resistencia de la sangre que vuelve al acceso vascular. Es positiva y va a depender del Qb, la viscosidad de la sangre y la resistencia del retorno venoso. Es recomendable que no supere los +300 mmHg. Así, cuando se exceda de los límites fijados, igual que ocurría con la Part, se activarán alarmas y se detendrá la bomba. Dado que puede producirse una desconexión accidental de la línea, que puede pasar desapercibida, se han desarrollado sensores adicionales que avisan en caso de que acontezca este problema y que son especialmente útiles en la HD domiciliaria nocturna.
Junto a estos controladores, antes de la bomba, existe, un punto de toma de muestras y un punto en “T” para infusión, por succión, de suero u otro tipo de medicaciones. Posbomba, nos encontramos un punto de infusión para heparina en “T”, cámara venosa y un detector de aire. La cámara venosa de aire es una importante medida de seguridad ya que “atrapa” el aire que pudiera haber en la línea, previniendo su entrada accidental al paciente. Si se detecta la presencia de microburbujas tras la cámara venosa o excesiva espuma en la cámara, se activará un sistema de seguridad, “clamp”, que colapsará la línea venosa y detendrá la bomba sanguínea, salvaguardando así de posibles embolismos aéreos. Además, la cámara venosa estará dotada de una malla atrapa-coágulos y de un control de nivel.
Como norma general, en todos los monitores, las alarmas del circuito sanguíneo paran la bomba de sangre. Las alarmas del circuito del LD, lo derivan al drenaje sin pasar por el dializador, dejando al monitor en bypass.
Finalmente, localizados en el circuito sanguíneo, nos encontramos un módulo de la bomba de heparina, que permite su inyección gradual o en bolo, en la línea arterial, durante la sesión de HD y un módulo de control de la presión arterial (PA), que conecta con el brazalete colocado en el paciente y puede controlar periódicamente la PA sistólica, diastólica, frecuencia del pulso y calcular la PA media. En algún monitor puede funcionar como un sistema de retroalimentación o biofeedback.
Monitores de unipunción.
Una configuración alternativa del sistema de diálisis es el que permite el uso de una sola aguja en el AV o un catéter de una sola luz, es la llamada unipunción. Puede realizarse de dos formas: con doble clamp y una sola bomba (cabezal único) o con doble bomba (cabezal doble). En ambos métodos, tanto la línea arterial como la venosa deben disponer de cámara de expansión para aumentar la capacidad sanguínea del circuito y así conseguir movilizar más sangre en cada ciclo. Los ciclos pueden programarse mediante control de las variaciones de presión producidas entre los dos clamps o entre las dos bombas. Los rendimientos del método de doble cabezal son superiores por la mayor velocidad y menor tiempo utilizado para la devolución de la sangre, además de mínimas recirculaciones, de escasamente un 20%. Como medida de seguridad en caso de problema con el medidor de presión, los monitores llevan incorporado un segundo control, bien de vueltas o de tiempo. Estos controles detienen las bombas cuando han dado las vueltas programadas o sobrepasado el máximo de tiempo de funcionamiento calculado en cada ciclo, respectivamente. De esta forma si las presiones no funcionan, las bombas se detendrán y avisarán de que algo sucede.
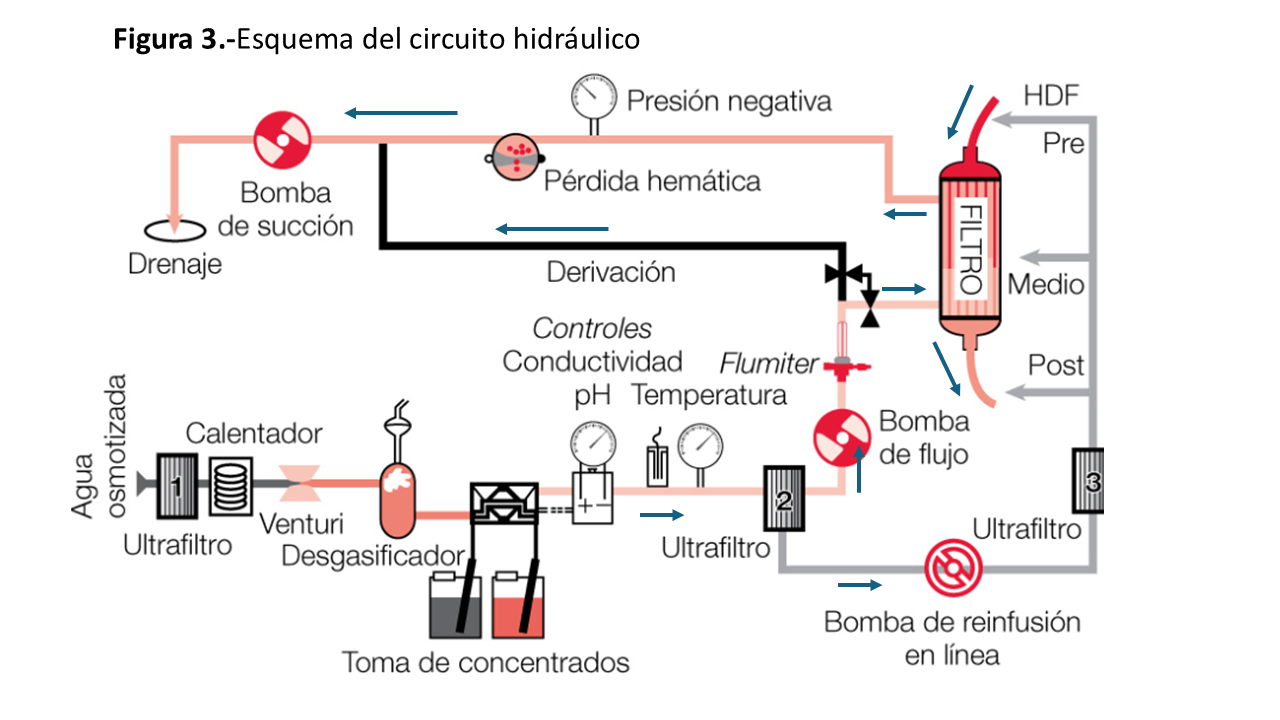
2.b Circuito hidráulico. Fabricación del líquido de HD (LD) (Figura 3).
En el monitor, se prepara el LD de forma constante mediante la mezcla de los concentrados de electrolitos y el agua purificada.
El proceso de fabricación del LD comienza calentando el agua (entre 35 a 37º C) para favorecer tanto la desgasificación como la posterior disolución de las sales. Una vez el agua calentada y desgasificada, se realiza la mezcla con los concentrados ácido y de bicarbonato e inmediatamente después se controlan de forma continua la conductividad y la temperatura. Si ambas son correctas, el LD pasa al dializador. En caso contrario, se desechará mediante una derivación hacia el drenaje. En esta situación, el monitor entra en bypass, interrumpiendo la difusión.
Los mecanismos de seguridad son esenciales ya que una mala desgasificación generaría burbujas de aire, que podrían hacer funcionar mal el detector de fuga de sangre y el detector de conductividad. Por otro lado, un LD con concentraciones de solutos no adecuadas puede producir una grave alteración electrolítica en el paciente. La monitorización de la conductividad evita esta complicación. Los cambios en la temperatura, la presencia de burbujas de aire o el mal funcionamiento del sensor, generalmente un electrodo, pueden alterar la conductividad del dializado.
Existen varios controles que aseguran la composición y pureza del LD. El monitor posee varios ultrafiltros que permiten obtener un LD ultrapuro. Estos están localizados tanto a la entrada del agua tratada, como tras la mezcla del agua con los concentrados (2). El primero de estos ultrafiltros, el localizado a la entrada del agua purificada, es un filtro de partículas, que en algunos monitores también retiene sustancias pirogénicas denominadas endotoxinas. Los otros están localizados después de que se fabrique el LD y en la mayoría de los monitores son dos. En ocasiones usan sólo uno para el LD y los dos si hay reinfusión como en la hemodiafiltración en línea (HDF-OL). En el sistema inicial de Gambro®, el segundo ultrafiltro en hemodiafiltración-OL era externo y desechable.
Después de pasar el dializador, en el circuito del LD, existe otro mecanismo de seguridad que controla las posibles pérdidas hemáticas mediante un sistema óptico de infrarrojos o ultrasonidos. Tiene sensibilidad para detectar pérdidas de 0,5 ml de sangre para un hematocrito del 25% y flujos de LD (Qd) de 500-800 ml/min. Cuando se detecta sangre en el dializado, salta una alarma, que para la bomba sanguínea. La presencia de sangre en el dializado generalmente indica una rotura de la membrana del dializador que puede ser producida, entre otras causas, por una PTM superior a 500 mmHg.
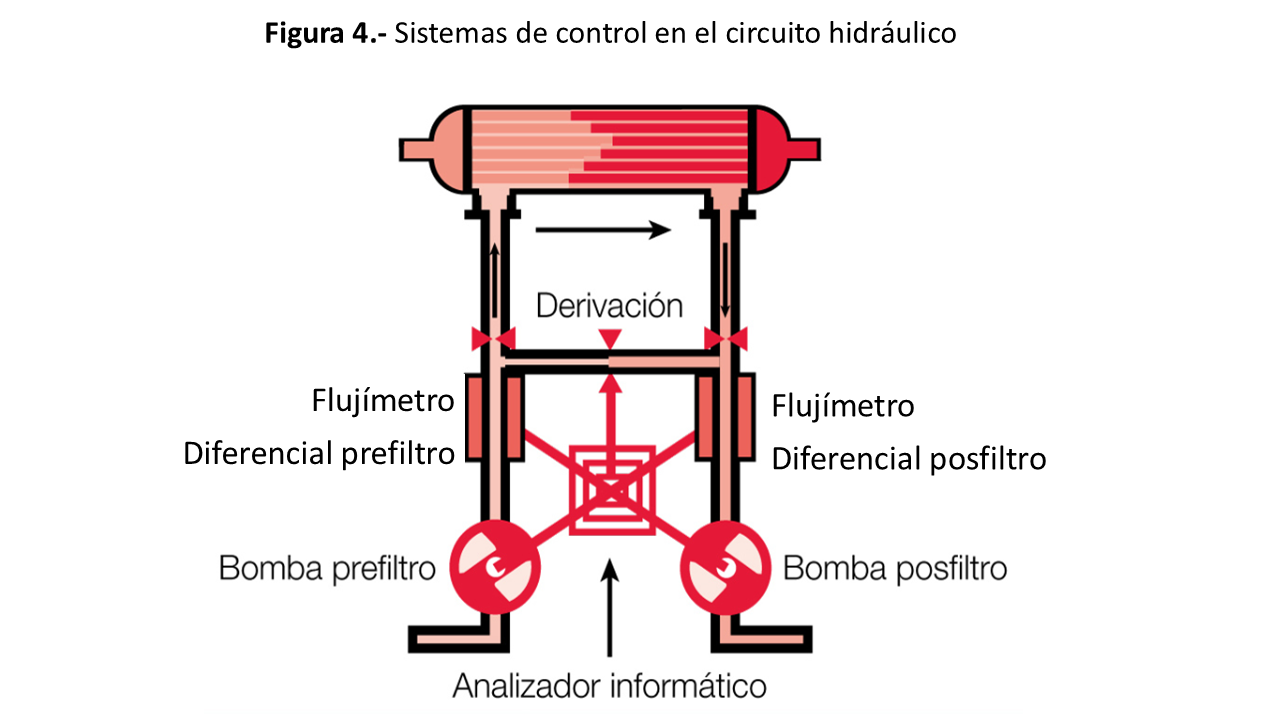
Además de la fabricación del LD, este circuito controla el volumen ultrafiltrado (UF). Actualmente, el método de control de la ultrafiltración utiliza circuitos muy sofisticados (Figura 4) que disponen de bombas de flujo prefiltro y posfiltro (cerrando el circuito) y de controles exactos de flujos, pre y posdializador, mediante flujómetros o flujímetros. Otros sistemas de control son la cámara de balanzas y el sistema Corioli. Estos sistemas usan distintas tecnologías según el monitor y permiten cuantificar, con muchísima exactitud, el volumen de LD que entra y sale del dializador, contabilizándolo de forma continua mediante analizadores informáticos.
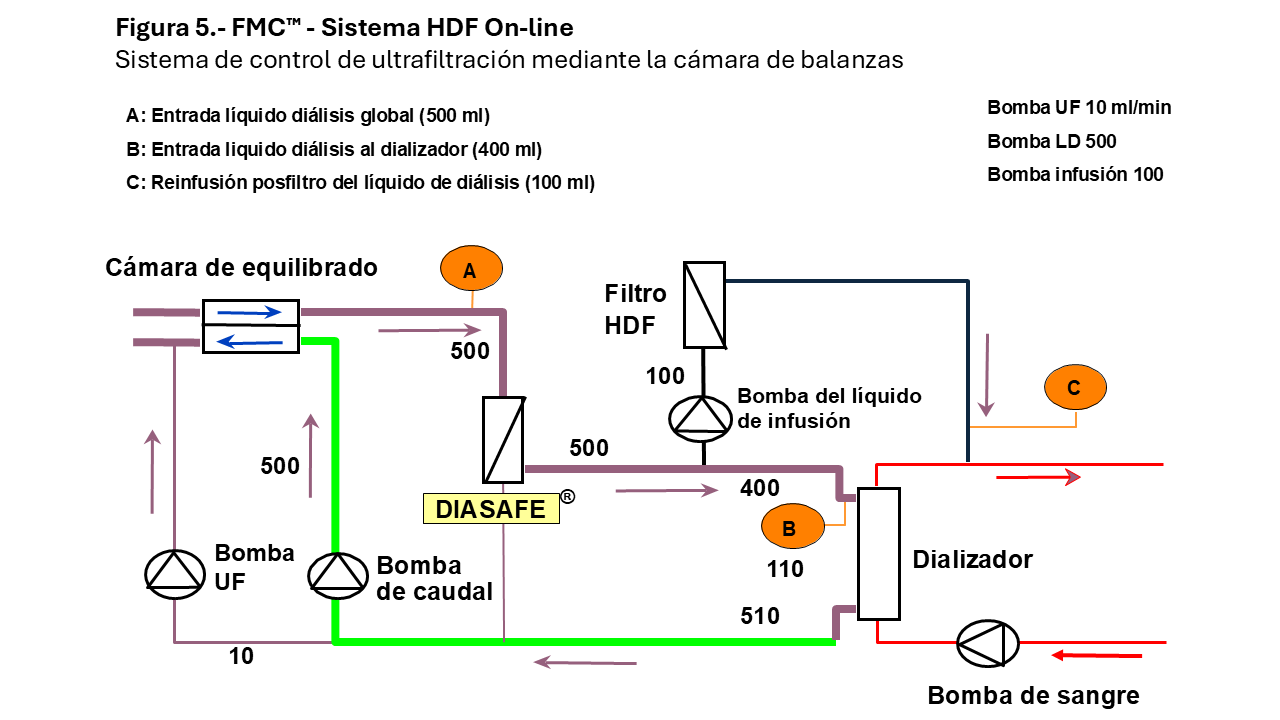
Cuando se realiza HDF-OL, se requieren también sistemas de seguridad para realizar el transporte convectivo correctamente. El sistema de control de ultrafiltración, mediante la cámara de balanzas, permite que el flujo de LD infundido coincida exactamente con el ultrafiltrado (Figura 5).
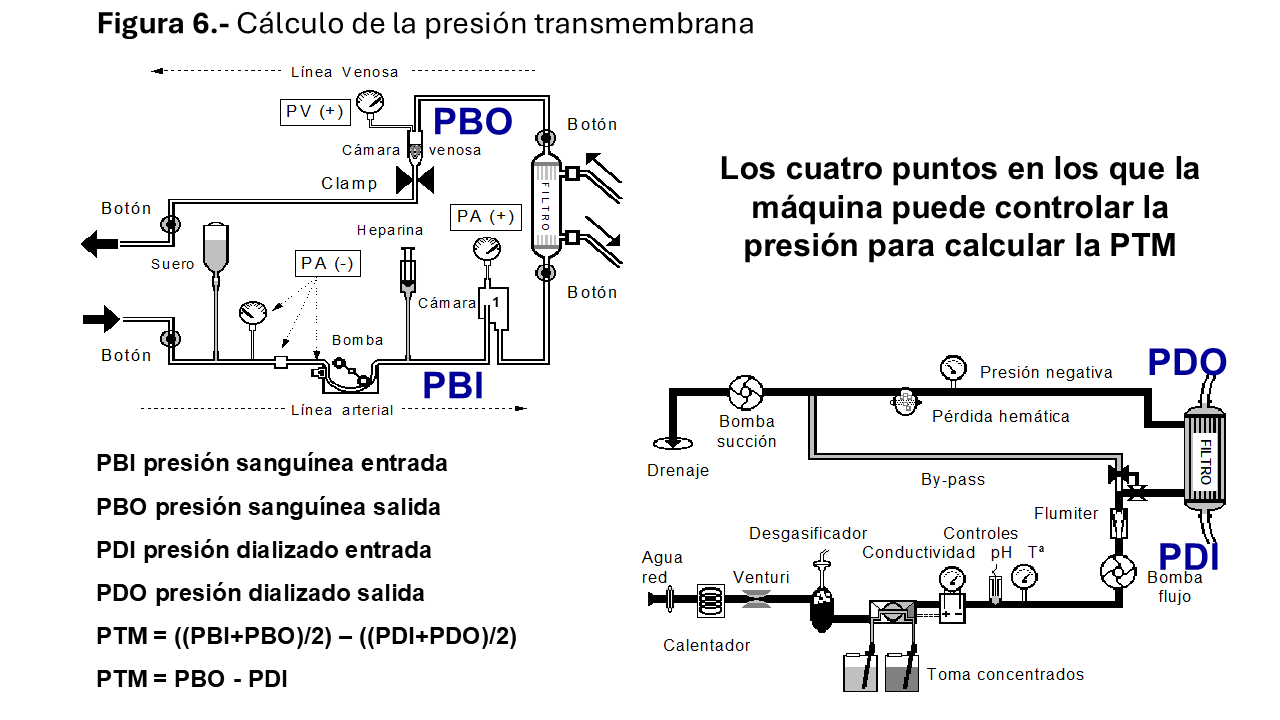
Los monitores de HD son capaces de aportar una estimación de la presión transmembrana (PTM). Con las medidas de presión de ambos circuitos calculan la PTM, que se define como el gradiente teórico de presiones que existe dentro del dializador, entre el compartimento sanguíneo (Pb) y el del LD (Pd). La Pb será la semisuma de presiones de entrada (Pbi) y salida (Pbo) en sangre y la Pd la semisuma de presiones de entrada (Pdi) y salida del baño (Pdo): PTM = [(Pbi + Pbo)/2] – [(Pdi + Pdo)/2]
Los monitores de diálisis utilizan distintas medidas para calcular la PTM, ya sea como [(Pbi + Pbo)/2] – Pdo, 3 puntos o más frecuentemente, de forma más sencilla, como Pbo – Pdo, 2 puntos. Por lo tanto, la PTM que nos suministran los monitores no se corresponde con la realidad y será diferente según el cálculo de cada monitor (2, 3 ó 4 puntos) (Figura 6).
Algunos monitores (Surdial®, Baxter®) utilizan esta medición y se utiliza para optimizar de forma automática el volumen convectivo en la HDFOL. Van aumentando progresivamente la UF y viendo como repercute en el aumento de PTM hasta lograr el punto de máxima eficiencia.
Así, los monitores van a contar con una serie de límites o alarmas de estas presiones, por ejemplo: Ppref < 700 mmHg o PTM < 300 mmHg, que dependerán de la técnica que vayamos a utilizar y que se integrarán en su software.
Los monitores más completos tienen tres bombas: la bomba de sangre, una bomba de unipunción y una bomba de infusión para la HDF-OL.
2.c Sistemas de monitorización:
El monitor de HD se debe programar para la diálisis según las especificaciones del nefrólogo que pueden estar preestablecidas o individualizadas para una sesión en concreto.
Además de enviar la sangre y el LD al dializador, con múltiples sistemas de seguridad, las máquinas de diálisis actuales también son capaces de detectar, calcular y almacenar una gran variedad de datos en tiempo real. Toda la tecnología va dirigida a facilitar la realización de la técnica, medir la dosis de hemodiálisis y mejorar la estabilidad hemodinámica del paciente.
Los primeros biosensores se desarrollaron en las últimas décadas del siglo XX. Controlan y analizan variaciones de determinados parámetros en el circuito de sangre o en el del LD. Cuando responden de forma automática ante un cambio en alguno de estos parámetros, constituyen un sistema más avanzado denominado biofeedback. Por tanto, los biosensores son detectores no invasivos que reciben señales del circuito de sangre o del LD dando información en tiempo real y de forma repetida. Si el parámetro analizado está fuera de los valores deseados el monitor avisa para que se actúe de forma manual. En el caso de un biofeedback, el monitor responde automáticamente, sin lapso entre la señal detectada y el cambio, ya que se diseñan para parecerse a la fisiología con una respuesta inmediata por parte del monitor. Un ejemplo de biofeedback es el sistema que según monitoriza la volemia del paciente, durante la sesión de diálisis, ajusta la tasa de ultrafiltración y la conductividad del LD para prevenir descensos de volumen sanguíneo inferiores a un valor establecido previamente.
El monitor puede registrar la presión arterial del paciente de forma programada mediante un manguito de presión conectado al mismo.
2.c.1 Ajustes básicos
Existen una serie de ajustes que sirven para individualizar la diálisis y que podemos ver reflejados en la pantalla del monitor durante toda la sesión.
- Flujo de sangre (Qb) es clave para llevar a cabo una diálisis adecuada y es uno de los primeros ajustes a realizar. Un Qb alto > 350 ml/min logra un mayor rendimiento de la HD y, en todo caso, debe estar en consonancia con las características del dializador.
El Qb está condicionado por la velocidad de la bomba sanguínea. Sus variaciones cambiarán tanto la Part, la Ppref y la Pven, que a su vez, pueden condicionar el Qb programado: la Part en general no debe ser inferior a – 170/-200 mmHg, la Ppref no debe superar + 500/+ 700 mmHg y la Pven a + 170/+ 200 mmHg.
- Flujo del LD (Qd) es otro ajuste a programar al inicio de la sesión de diálisis. Debe estar en consonancia con el Qb y de hecho, algunas máquinas lo ajustan automáticamente a éste. Con los dializadores modernos, con alta densidad de capilares, utilizar Qd por encima de 500 ml/min aumenta muy poco el aclaramiento de la técnica (K) y consume mayor volumen de agua y LD [3][4] La antigua relación Qd/Qb de 1,4 debería ser actualmente de 1,2.
- La UF se programa en función del control del peso del paciente. En general, se suele utilizar el mismo ritmo de UF a lo largo de toda la sesión de HD. Sin embargo, también puede hacerse perfiles de UF que proporcionan una tasa variable de eliminación de líquido, con modelos de descenso lineal, escalonado o exponencial.
- El ajuste de bicarbonato/conductividad parcial de bicarbonato (de 20 a 40 mM/l). Es útil en pacientes con acidosis o alcalosis metabólicas o con problemas respiratorios o hepáticos. En la mayoría de los monitores, la conductividad de bicarbonato está reflejada en la pantalla del monitor y puede modificarse en función de las necesidades del paciente. Hay que conocer que el monitor no mide la concentración de bicarbonato en el LD, sino que la calcula a partir de la conductividad parcial. También hay que tener en cuenta que los cambios en el bicarbonato van a producir cambios en los otros electrolitos del LD para mantener la electroneutralidad.
- Ajuste de la concentración de Na/conductividad total. [5][6]. La concentración de sodio también se puede individualizar. Su ajuste modifica las proporciones entre el concentrado ácido y el agua, cambiando ligeramente las concentraciones de otros solutos presentes en dicho concentrado. Como en el caso del bicarbonato, el monitor no mide sodio, sino que lo calcula en función de la conductividad y de la composición del LD, que debe estar incluida en la información del monitor y preseleccionada. El sodio del LD se puede mantener fijo durante la sesión de diálisis o bien, se pueden usar los perfiles disponibles en el monitor. Los perfiles cambian la concentración de sodio en el dializado durante la diálisis, generalmente comienzan con 150 o 155 mEq/l y van disminuyendo progresivamente hasta 135- 140 mEq/l casi al final de la diálisis. Estos perfiles ofrecen la ventaja teórica de reducir los síntomas intradiálisis (hipotensión y calambres), minimizar la sed, la ganancia interdiálisis (GID) y la hipertensión, aunque esto no está comprobado en la práctica.
- Ajuste de la temperatura. La temperatura del LD puede también ajustarse y se hace de forma empírica. Dependiendo de la política de la unidad de hemodiálisis se tiende a usar temperaturas bajas para mejorar la tolerancia hemodinámica.
2.c.2 Monitorización del aclaramiento
La monitorización en línea del aclaramiento (K) puede proporcionar el mejor seguimiento de la adecuación de la diálisis. Se puede realizar midiendo: a) la concentración de urea en el dializado de forma continua o periódicamente, b) la dialisancia iónica (DI) y c) la absorción de luz ultravioleta del LD.
Los sensores de urea miden continuamente la concentración de urea en el efluente. Sus problemas de calibración, mantenimiento y costes han condicionado que su uso no se haya extendido [7].
La dialisancia iónica. Los métodos basados en conductividad fueron descritos en 1993 [8]. Provienen de la observación de que el aclaramiento de sodio y urea son casi iguales. La medición se hace elevando la conductividad del LD (dependiendo del monitor sube a 15,5 mS/cm durante 60 a 90 segundos (OCM®) o sube 1 mS/cm (Diascan®) durante 2 minutos) o bajándola si se estuviera dializando con conductividad elevada. Estos cambios modificarán la difusión de sodio entre la sangre y el LD, variando la conductividad a la salida del LD. El cambio se compara con el basal y se aplica un modelo matemático que nos permite conocer la DI. La fórmula utilizada es:
K= [1-((Cdo2 - Cdo1) / (Cdi2- Cdi1))]x (Qd+Qf)
Donde: Cdo2 y Cdo1 son la conductividad a la salida del LD cuando se modifica y en la situación basal, Cdi2 y Cdi1 son la conductividad a la entrada del LD, tras el cambio y en situación basal, y Qd y Qf son las tasas de UF. También se calcula, la conductividad del agua plasmática (Cp), que es cuando la conductividad de entrada al dializador es igual a la de salida.
La DI es equivalente al K de urea. Es importante recordar que la DI del sodio se infiere indirectamente de la conductividad del LD y que, por tanto, K es una medida indirecta. En la práctica, cada monitor realizará la medida de forma programada con una frecuencia determinada, mediante sensores que van colocados a la entrada y la salida del LD y deben calibrarse periódicamente. Los valores de aclaramiento comunicados pueden diferir dependiendo del equipo utilizado y los ajustes aplicados al software, pero múltiples estudios han validado este método. Tiene una magnífica correlación con el Kt/V medido en sangre, con un rango de error menor al 5-6%, siendo la V, que se introduce en el cálculo, lo que más variabilidad induce. Por ello, muchos datos abogan por la medición del Kt, una forma real de medir la dosis de diálisis, expresada en litros, ya que tanto K como el t son reales y medidos por el monitor. Como posible efecto negativo se incluye la sobrecarga de sal, pero se han realizado trabajos in vitro, clínicos y de cálculo matemático, que evidencian que no supone una sobrecarga de sal relevante [9][10][11].
El tercer método es la espectroscopia ultravioleta-visible o espectrofotometría ultravioleta-visible. A partir de estudios de cromatografía líquida se demostró que algunas sustancias urémicas eran activas en el espectro del rango ultravioleta (UV), lo que llevó al desarrollo de sensores espectrofotométricos a la salida del LD que monitorizan el tratamiento. Se utiliza una radiación electromagnética en una longitud de onda, que es absorbida por las moléculas de esta región del espectro y cuantificada (280–100 nm Adimea™ y Dialysis Dose Monitor™). La absorbancia se calcula de forma constante comparándose de forma logarítmica con la inicial (habitualmente cada 3 minutos) creando una curva que reproduce el Kt/V sp, con la ventaja de que no hay que medir la V. La debilidad teórica es que la longitud de onda no es específica para una molécula, aunque longitudes de onda entre 200-285 nm miden moléculas pequeñas (urea, ácido úrico o creatina) y representan el 95% de la absorbancia. Este método ha demostrado también una buena correlación con el Kt/V de urea medido en sangre [12] [13] [14]. Un estudio que compara ambos métodos de medida encuentra medidas similares [15].
En general, la monitorización en línea elimina el gasto y los riesgos de las muestras de sangre, reduce el tiempo de personal, permite determinaciones más frecuentes de la dosis suministrada y da mediciones en tiempo real. Con ello, se consigue un adecuado control y seguimiento de la dosis de diálisis, detectando pacientes que pudieran tener una dosis de diálisis inadecuada. La otra gran ventaja de utilizar estos biosensores es que permiten valorar rápidamente la evolución de la sesión detectando si existe alguna incidencia, como conexión invertida de líneas, disfunción del catéter, tiempos muertos, etc., incidencias que se pueden corregir fácilmente cuando se detectan. Además, el seguimiento en cada sesión de diálisis permite detectar si existe un descenso de la eficacia mantenido, que puede asociarse a disfunción del acceso vascular.
Los inconvenientes de la monitorización en línea del aclaramiento son: 1. necesidad de múltiples mediciones de K para obtener una media de la diálisis completa, 2. monitorización segura del tiempo de tratamiento, 3. se necesitan muestras de urea en sangre para permitir la determinación de la tasa de catabolismo proteico (PCR) y 4. si se quiere medir Kt/V usando DI es necesario medir o estimar V.
2.c.3 Sistemas para mejorar la tolerancia hemodinámica
Conseguir una adecuada tolerancia hemodinámica es uno de los objetivos fundamentales de la diálisis. La inestabilidad hemodinámica, conlleva problemas tanto agudos (durante la sesión de HD) como a largo plazo. Los sistemas de control de la volemia incorporados en los monitores ayudan a mejorar la tolerancia hemodinámica, previniendo las hipotensiones intradiálisis y evitando el desarrollo de hipertensión.
2.c.3.a Monitorización del hematocrito y volumen relativo de sangre
El primero de ellos es la monitorización en línea del hematocrito o la viscosidad sanguínea sustentándose en que el grado de hemoconcentración refleja la magnitud relativa de la depleción del volumen intravascular [16] [17] [18].
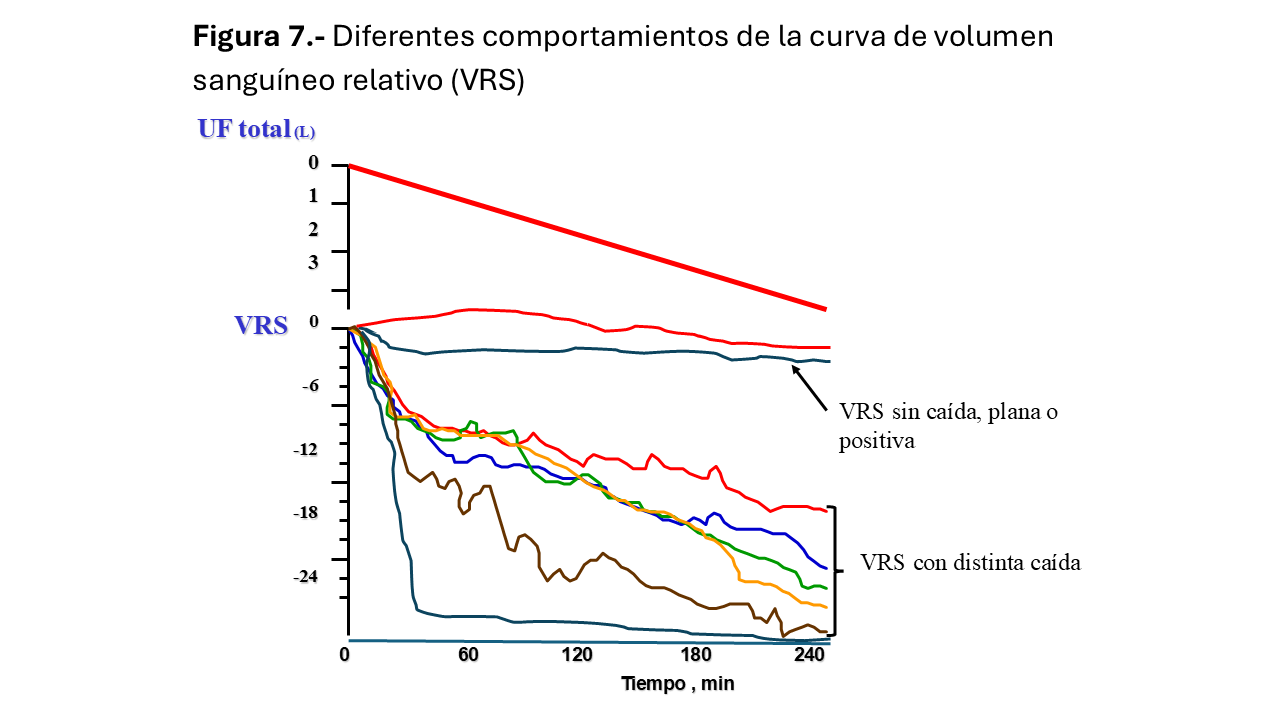
Es un método indirecto de control de las variaciones de la volemia basado en la ley de conservación de masas: si la cantidad de una sustancia X no sufre variación durante la sesión de diálisis, las variaciones en su concentración serán exclusivamente debidas a modificaciones del volumen en el que está disuelta. Teóricamente, durante la HD la masa proteica y eritrocitaria permanece constante, mientras disminuye el volumen de agua plasmática por la UF y esto se registrará como porcentaje de variación del volumen sanguíneo (VS), tras una medida inicial que es 100%. El descenso de VS ocasionado por la ultrafiltración se compensa continuamente por el relleno vascular y según sea la capacidad de relleno la curva de VS cambiará. Así, la interpretación teórica es que la pendiente será más pronunciada si la volemia desciende, indicando que la velocidad de ultrafiltración excede al relleno intravascular desde los espacios intersticial e intracelular y, por lo tanto, puede propiciar hipotensión. Por el contrario, si la volemia crece o se mantiene constante, la curva será plana o la pendiente menor y nos inclinaremos a pensar que podemos hacer mayores balances negativos si los precisamos, sin esperar cambios sustanciales hemodinámicos. Es importante subrayar que los equipos no miden cambios absolutos del volumen sino el porcentaje de cambio o volumen sanguíneo relativo (VRS) que se muestra en un gráfico como porcentaje de cambio de volumen (%VRS/tiempo) pudiendo describirse curvas diferentes en cada paciente con igual UF (Figura 7).
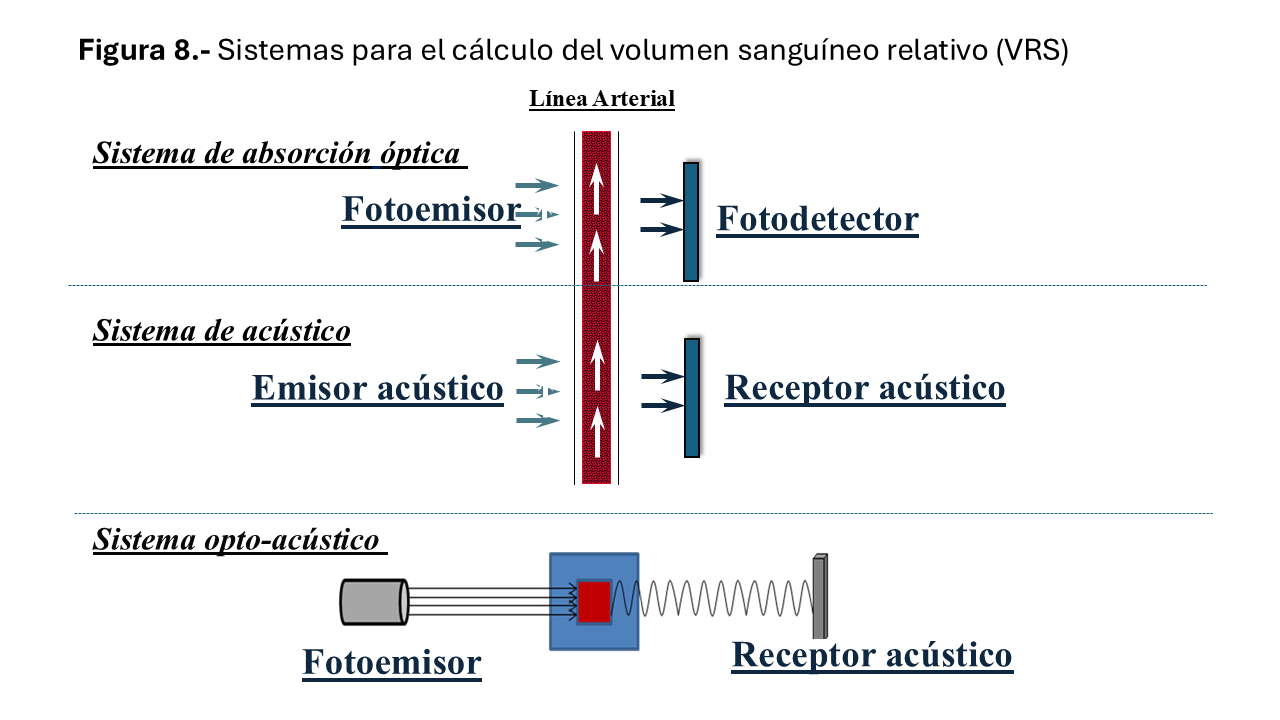
Hay varios tipos de biosensores de VS (Figura 8). El más usado consiste en un sistema de emisión-recepción de un haz de luz monocromática a través de la línea arterial, cuya adsorción óptica depende fundamentalmente de la concentración de hemoglobina o del hematocrito. El otro procedimiento está basado en el estudio de las variaciones de viscosidad mediante ultrasonidos. La determinación del VRS puede variar de forma significativa entre dispositivos.
Para utilizarlo en la práctica, es necesario tener en cuenta que hay que identificar el patrón de disminución de VRS de cada paciente en relación con la clínica para determinar cuál es su VRS crítico a partir del cual aumenta el riesgo de hipotensión. Para determinarlo se recomienda monitorizar la caída de VRS durante 3 a 6 sesiones, correlacionándola con el comportamiento de la presión arterial (PA):
- Si cae la PA, anotaremos el VRS como crítico.
- Si no hay hipotensión, el VRS mínimo podrá ser el VRS crítico.
La media de los VRS críticos de las sesiones estudiadas será el VRS crítico que indicaremos en el monitor, de forma que cuando éste se alcance, se nos alertará para que se adopten las medidas que se consideren oportunas.
Aunque teóricamente la curva nos indica los cambios en la volemia, a la hora de utilizar el VRS hay que recordar:
1) Con UF constante, la caída del VRS a lo largo de la sesión genera diferentes curvas (Figura 7).
2) No existe un valor absoluto y crítico a partir del cual aparezca hipotensión, ya que hay gran variabilidad tanto inter como intraindividuo
3) La relación entre tasa de UF y el cambio de VRS y entre este y el desarrollo de hipotensión es variable.
Esta variabilidad se explica porque la capacidad de relleno es diferente en cada paciente, en el mismo paciente según la sesión e incluso en la misma sesión según el momento, ya que depende de múltiples factores tanto del paciente como de las características de la diálisis. Por otro lado, la hipotensión también está condicionada por la respuesta cardiovascular inducida por la hipovolemia, desencadenándose o no según la capacidad de esta respuesta compensadora de corregir la hipovolemia. La disminución de VRS es mucho mejor tolerada en la primera hora de diálisis que al final de la misma, ya que la volemia se va reduciendo y cuanto más normovolémico esté el paciente mayor es el riego de hipotensión.
Según algunos autores, la caída de VS puede infraestimar la verdadera disminución de la volemia por la «translocación intravascular» de la sangre desde la microcirculación (capilares y vénulas), que tienen un menor hematocrito, hacia los vasos más grandes. La premisa de que la distribución del volumen y el volumen de células y plasma es constante e igual en todo el sistema circulatorio no sería del todo cierta: el hematocrito "corporal" es menor que el arterial o venoso debido a que en capilares y vénulas (< 200 micras) el hematocrito es menor (efecto Farhraeus). Esta diferencia (F-cell ratio: Hto global/Hto arterial o venoso) es 0,91 aproximadamente en individuos sanos. Cuando hay redistribución de sangre, su paso desde el capilar al central afectaría negativamente a la medida de VRS, de modo que infraestimaría la reducción de VS total. Finalmente, algunos trabajos afirman que la estimación de VRS por medidas ópticas se ve afectado por los cambios en la concentración de electrolitos, sobre todo del sodio, por su efecto sobre el volumen celular, mediado por cambios osmolares. Este cambio afectaría a la concentración local de hemoglobina y modificaría la absorbancia y propiedades de la sangre [19] [20] [21]
Basándose en los expuesto anteriormente, la medición de VRS serviría para prevenir la hipotensión, mediante ajustes en la velocidad de ultrafiltración y también como una herramienta para el ajuste del peso seco. De cualquier modo, al usar este método hay que tener en cuenta sus limitaciones, de hecho, en la bibliografía encontraremos múltiples datos que apoyan o no su utilidad. Dado que, como se ha dicho, estos sistemas miden cambios relativos en el volumen, diferentes volúmenes absolutos de inicio y fin (que marcan la hidratación real) originan curvas de VRS que pueden ser similares. Así, algunos autores abogan por medir el volumen absoluto y e incorporar esta medición en el software de los monitores, que parece relativamente sencillo, aunque en la actualidad, no está disponible [22][23][24]
Finalmente, el VRS puede formar parte de biosensores o sistemas de retroalimentación controlados por ordenador para modificar continuamente la tasa de ultrafiltración o la concentración de sodio durante la diálisis.
Durante la sesión de HD, la hipovolemia inducida por la UF estimula el sistema nervioso simpático que responde induciendo vasoconstricción periférica, para evitar la caída de la presión arterial. Al mismo tiempo, se produce un aumento de la producción de energía y de calor, que puede inducir un reflejo vasodilatador que anule la respuesta vasoconstrictora de la UF, favoreciendo la aparición de episodios de hipotensión, especialmente, en enfermos predispuestos. El aumento de la temperatura corporal central puede causar inestabilidad hemodinámica y, por lo tanto, se aconsejan temperaturas más bajas para mejorar la tolerancia durante las sesiones de diálisis, favoreciendo la pérdida de calor y permitiendo conservar constante la temperatura corporal. El mayor inconveniente de esta "diálisis fría" es la mala tolerancia del paciente por la pérdida de temperatura.
Se han desarrollado controles automáticos (BTM®, Hemox®) que con un método no invasivo modifican constantemente la temperatura del LD, para mantener estable la temperatura corporal, por lo que tienen los beneficios de la “diálisis fría” pero sin los efectos secundarios de la hipotermia. El sistema está compuesto por dos sensores que monitorizan en todo momento la temperatura sanguínea en la línea arterial y en la venosa. Esto permite cuantificar tanto los efectos de la hemodiálisis sobre la temperatura corporal central, como realizar balances de energía. Podremos realizar hemodiálisis “termoneutra”, cuya finalidad es conseguir balances energéticos iguales a cero, o hemodiálisis “isotérmica”, cuyo objetivo es mantener estable la temperatura corporal central. Hay que recordar que la estabilidad hemodinámica en la diálisis depende de los cambios de la temperatura central y no del balance.
Desde el punto de vista práctico, estos sistemas funcionan de forma automática y sólo precisan activarse indicando el cambio deseado en la temperatura.
La saturación venosa de O2 (SvO2) difiere en las distintas partes del organismo y depende de la extracción de oxígeno, la cual se modifica por los requerimientos metabólicos celulares. Durante la HD, la PA se mantiene estable por aumento de las resistencias vasculares sistémicas, pero el mecanismo adaptativo induce hipoperfusión tisular manifestada por una disminución en la SvO2 y por ello se ha considerado que es una expresión indirecta de la estabilidad hemodinámica. Esto ha llevado al desarrollo de sensores que durante la HD miden de forma no invasiva SvO2 con un sensor en la línea arterial.
Cuando controlamos el hematocrito/hemoglobina mediante emisión/recepción de rayos infrarrojos multifrecuencia la hemoglobina oxigenada adsorbe unas frecuencias diferentes a la no oxigenada y podemos conocer tanto la saturación de O2 (como con un pulsioxímetro) como las variaciones en la concentración del hematocrito (VRS). Cuando el emisor es monofrecuencia no pueden diferenciar entre Hb oxigenada y no oxigenada.
Así, el mismo sensor en el monitor cumple las dos funciones: mide VRS y SvO2 (Hemox®). Concretamente la aplicación Soglia® tiene la finalidad de indicar al operador la posible aparición de hipotensiones en el paciente. El método se basa en la medición de la variabilidad de la SvO2 en la sangre del paciente, que se mide como desviación estándar (DE). Hay que hacer seguimiento previo de la respuesta a la UF durante 3-6 sesiones, observando, en que DE se produce la hipotensión, que es por tanto un valor individualizado. Con ello se fija una alarma que avisará cuando se alcance el valor para tomar las medidas preventivas necesarias. La anticipación es de unos 10 minutos. En el momento actual, existen escasas publicaciones con este método, aunque avalan su utilidad en la detección de la futura hipotensión.
2.c.4 Sistemas de seguimiento del acceso vascular
Distintos elementos comentados en secciones anteriores tienen utilidad en la monitorización del acceso vascular.
La medida de la DI constituye un procedimiento para estimar el flujo del acceso vascular QA [38] [39]. Se hace obteniendo mediciones de la DI con líneas en posición normal e invertida y aplicando la siguiente fórmula se puede obtener el valor del QA:
QA = Dinv × (Dnor – TUF) / (Dnor – Dinv)
Donde Dinv es el valor de la DI con las líneas de HD en situación invertida, Dnor es la lectura de la DI con las líneas de HD en posición normal y TUF es la tasa de UF en ml/min.
El BTM®, sistema de biocontrol de temperatura, permite calcular la recirculación del AV produciendo modificaciones puntuales y automáticas de la temperatura durante la sesión de HD [40] [41]. Mediante la emisión de un bolo térmico, el monitor varía la temperatura del LD en dos grados, con la consiguiente variación de la temperatura en la línea venosa. Midiendo la variación de la temperatura en la línea arterial efectúa el cálculo de la recirculación. Con este sistema, se puede realizar una determinación del QA a partir de los valores de temperatura obtenidos con las líneas de HD en posición normal e invertida y aplicando la fórmula siguiente:
QA = (QBx – TUF) · Tartx – Tvenx / Tartn – Tartx
donde QBx es el flujo efectivo de sangre con las líneas de HD en posición invertida (ml/min), TUF es la tasa de ultrafiltración (ml/min), Tartn es la temperatura de la línea arterial, con las líneas de HD en posición normal, Tartx es la temperatura de la línea arterial, con las líneas de HD en posición invertida y Tvenx es la temperatura de la línea venosa, con las líneas de HD en posición invertida. Para calcular correctamente el QA, se precisa que se mantengan constantes el QB, la TUF y la temperatura del líquido de HD (35,5 ºC) durante todo el tiempo de la determinación.
2.c.5 Monitorización del balance de sodio (sal)
A partir de la medición de la conductividad y la estimación de K, algunos monitores calculan la conductividad plasmática y a partir de ahí estiman la natremia. Algunos de ellos representan la evolución de la natremia a lo largo de la sesión. El monitor Integra® mediante Diascan® de forma no invasiva, nos permite conocer la transferencia de masa iónica (TMI), prácticamente igual al balance de cloruro sódico durante la sesión de diálisis [42] [43] [44] [45] [46] [47] [48].
3. Sistemas de retroalimentación o biofeedback.
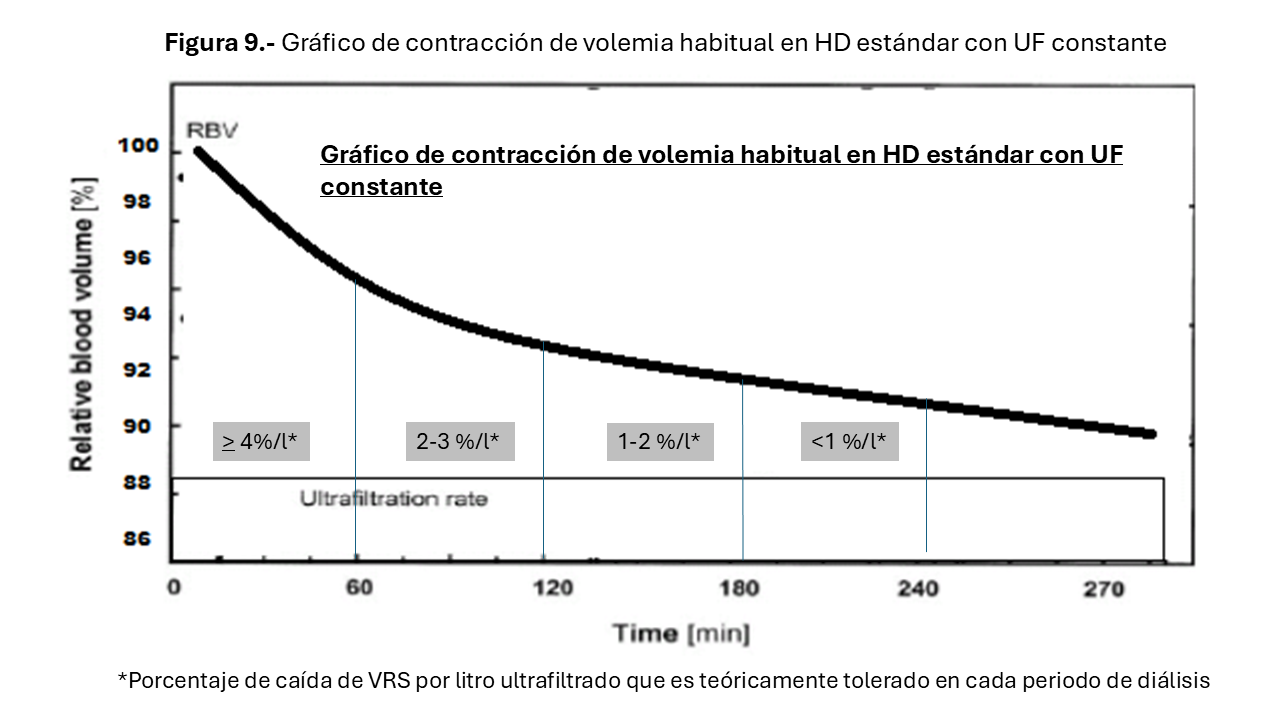
Cuando realizamos HD con UF fija (Figura 9) y observamos la curva de contracción de volumen, en la 1ª hora vemos que la volemia decrece rápidamente, en la 2ª hora, cae menos y así, progresivamente hasta el final, interpretándose que cuanto más cae la volemia, peor es el relleno vascular y al revés. Esto se explica por las diferencias osmolares compartimentales, que son mayores al inicio, de modo que cuando la urea se reequilibra hay mejor relleno. Así, en la 1ª hora, hay UF y cambio osmolar que favorece la salida del espacio vascular. Posteriormente, esa corriente cesa y mejora el relleno hasta el agotamiento de la reserva intersticial. Teóricamente, la contracción inicial mejora con conductividades altas y las finales bajando la UF. Basándose en lo anterior, se han desarrollado distintos perfiles con cambios en concentración de sodio o en la velocidad de UF y que tienen diferentes usos e interpretaciones.
3.a Automatización de la prescripción de sodio [49] [50] [51] [52] [53] [54]
Existe la posibilidad de “fijar” la natremia que se quiere lograr al final de la diálisis mediante un sistema de biofeedback que va modificando la conductividad del LD para obtener una natremia igual o más baja que la inicial. Podemos tener una diálisis “isoconductiva” (con igual conductividad al inicio que al final, Diacontrol®) o “isonátrica (con igual natremia, Aequilibrium®). Este sistema se asocia a menor ganancia de peso interdiálisis y mejor control de la PA intra e interdiálisis.
Se ha desarrollado un modelo matemático (Profiler®) que describe la cinética de urea y sodio en 2 compartimentos (intracelular e intersticial) y que se aplica para calcular perfiles de UF y sodio, a partir de la duración de la sesión, UF, concentración inicial de sodio y urea y concentración de sodio final deseada. Con esos datos se genera una curva teórica que luego se va modificando en función de la eliminación de sodio y de la UF. La estrategia intenta lograr un balance neutro de sodio (ganancia interdiálisis=eliminación) y contrarrestar la bajada de la osmolaridad en la primera hora de la sesión de diálisis. Hay algunos trabajos que, utilizando este sistema, muestran su utilidad para mejorar la estabilidad hemodinámica, con un balance adecuado de sodio y con mejoría del síndrome de desequilibrio. El problema de este sistema es que no mide la concentración inicial de sodio.
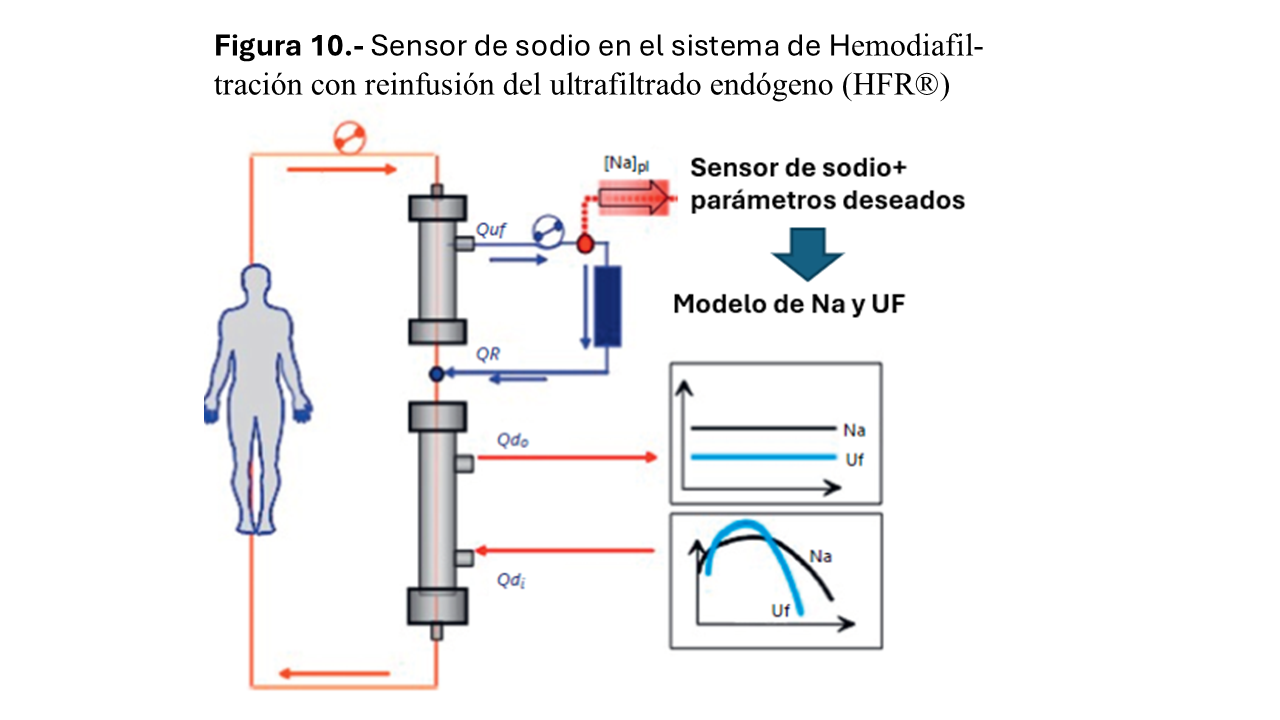
Existe un sensor de sodio (Natrium®) incorporado en la hemodiafil¬tración (HDF) con reinfusión del ultrafiltrado endógeno (HFR®). Esta es una técnica de HDF que utiliza un doble filtro en serie. En la primera membrana de alta permeabilidad se realiza la UF para obtener depuración convectiva. El ultrafiltrado pasa por un cartucho con una resina fisiológica adsorbente que permite que el ultrafiltrado se reinfunda entre los dos filtros, generando un líquido de reinfusión endógeno (Figura 10). El sensor de sodio mide la conductividad del ultrafiltrado endógeno antes de que entre en la resina y en el segundo filtro, calculando la natremia, con una diferencia de 0,5 mEq/l respecto a la natremia del laboratorio. El sistema se llama HFR-Aequilibrium®.
El Na Management es nuevo módulo, biocontrol® [55], basado en el cálculo del sodio plasmático. Cuando está inactivo, estima el Na plasmático presesión y lo monitoriza a lo largo de toda la sesión, aportando información del balance total de sodio durante la misma. También nos detalla la cantidad de trasporte de sodio por difusión y por convección. Si se activa como biocontrol se puede fijar un objetivo de sodio plasmático para toda la sesión y así, realizar diálisis isonatrémicas, que están demostrando mejores tolerancias y menores GID. Fijar un objetivo de sodio positivo (ganancia) o negativo (perdida), puede ser útil en pacientes hipo/hipertensos o en las hipo / hipernatremias
3.b Automatización del volumen relativo sanguíneo (VRS)
3.b.1 Modificación de UF y concentración de sodio en LD ajustado a VRS, Hemocontrol® Haemo-Master®
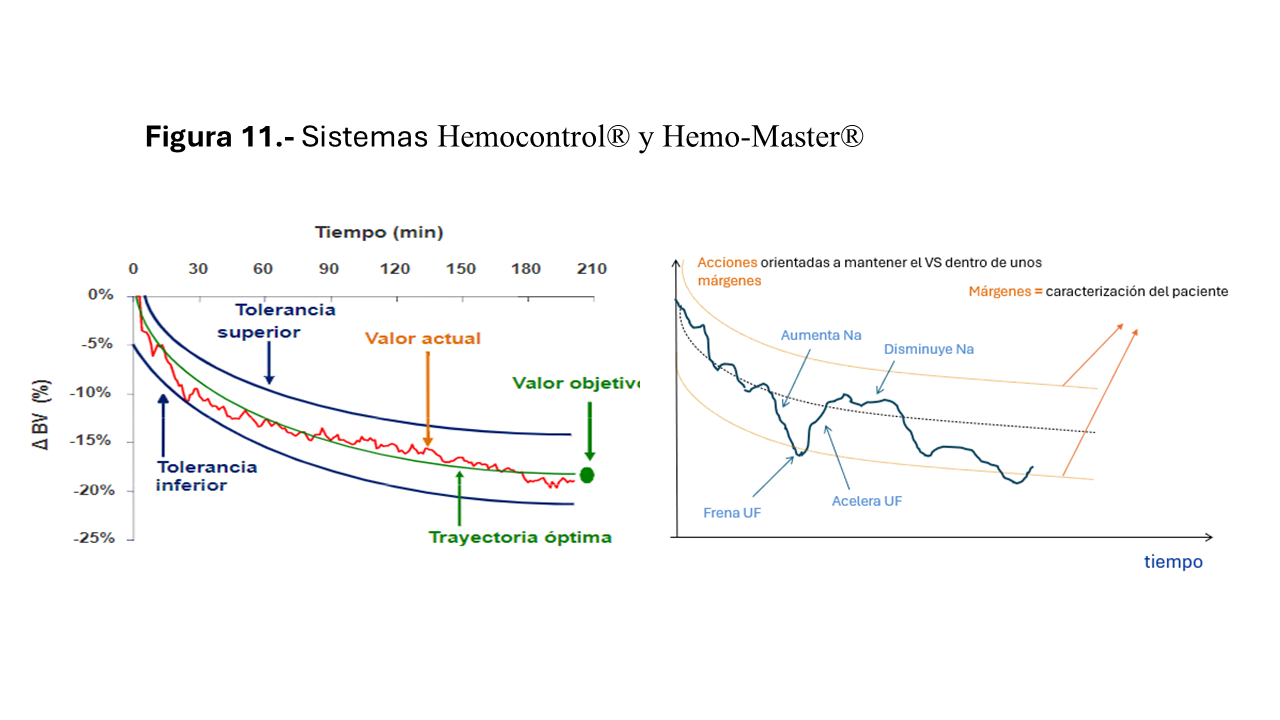
En la tolerancia hemodinámica, la tasa de UF horaria y la concentración de sodio del LD tienen un papel fundamental. Así, se ha diseñado un sistema de biofeedback que controla los cambios en la volemia mediante la medición continua de la caída de VRS, manteniéndola en un rango prefijado mediante ajustes de continuos de la UF y conductividad (Figura 11).
Para utilizarlo es necesario realizar varias sesiones de control previo, se aconsejan 6, en las que se recoja la caída de VRS y la UF en la que ha ocurrido la hipotensión, o bien, la caída final y la UF final. Con ello, se calcula un cociente VS/UF medio, que indica cuánto se prevé que va a bajar el VRS por cada litro ultrafiltrado. En este sistema, es necesario programar el tiempo de tratamiento, la UF total, el volumen de distribución y diferentes parámetros específicos que incluyen la ratio individual (VS/UF), el coeficiente de UF máxima y el equivalente y límites de sodio. El equivalente de sodio es la concentración de sodio utilizada en una diálisis estándar y los límites son los rangos entre los que va a oscilar su concentración en el LD. El coeficiente de UF máxima dependerá del volumen de UF total, acotando la UF máxima horaria.
Con estos datos, el software elabora la curva-perfil de contracción de la volemia permitida a lo largo de la sesión de diálisis y según su evolución, se realiza la UF máxima posible. Si baja VRS más de lo previsto el sistema responde bajando la UF y/o aumentando la conductividad para mejorar el relleno vascular [56] [57] [58] [59] [60] [61].
3.b.2 Modificación de UF ajustado a VRS [62]
En este caso, el biofeedback funciona haciendo ajustes en la UF, en función de la caída de VRS. Se programa una UF máxima y una caída de VRS crítica. Según va midiendo la caída del VRS, se ajusta la UF, con una UF más alta al inicio de la sesión y un descenso progresivo posterior. Se basa en que el mayor número de hipotensiones tienen lugar al final de la sesión.
3.b.3 Modificación de la concentración de sodio en LD ajustado a VRS
En este caso, es necesario fijar una concentración de sodio objetivo y otra máxima, de modo que irán realizando cambios en la concentración de sodio del LD de acuerdo con la caída de VRS, dentro de esos márgenes.
En el mercado existen monitores que incorporan un sistema capaz de modificar el Na del LD (conductividad) y la UF en función de los cambios del VRS, p. ej, Hemocontrol (Gambro/Baxter®) y Surdial (Nipro®).
3.b.4 Modificación de la UF en función de la PA del paciente.
Estableciendo unos márgenes de presiones arteriales (sistólica y diastólica), el monitor reducirá la ultrafiltración para prevenir posibles episodios de hipotensión en el paciente.
4. Los monitores y la optimización de la hemodiafiltración en línea.
Como se ha mencionado anteriormente, los monitores aptos para realizar hemodiafiltración en línea (HDF-OL) deben tener una bomba para la infusión del LD, deben ser capaces de garantizar las características ultrapuras del LD y tener un sistema acoplado de infusión / UF de gran exactitud.
La HDF-OL puede realizarse posdilucional, predilucional, mixta pre-post (mixdilution®) [63], secuencial [64] y mid-dilucional (mid-dilution®) [65]. La posdilucional es la forma más usada y de referencia y la puede realizar cualquier monitor de HDF-OL. La predilucional obtiene un menor rendimiento y no todos los monitores la pueden realizar. La mix-dilucional precisa de un sistema y monitor específico y no ha demostrado mayor eficacia que la posdilucional, por lo que se usa muy poco [66]. La mid-dilucional se puede realizar en cualquier monitor de HDF-OL, pero precisa un dializador especial. La secuencial se puede llevar a cabo en cualquier monitor de HDF-OL.
Se ha demostrado una supervivencia mayor de los pacientes en HDF-OL posdilucional respecto a los de HD de alto flujo (HD-HF) [67] cuando el trasporte convectivo en HDF-OL es superior a 23 litros por sesión. Para lograr este objetivo en pacientes con un Qb limitado se puede recurrir a dializar más tiempo o a aumentar la fracción de filtración (FF).
La limitación de la HDF-OL posdilucional es la hemoconcentración que se produce a partir del dializador hasta el punto de infusión y que condiciona la FF a utilizar. Los monitores de HDF-OL controlan la FF de distinta forma: Control del volumen de infusión fijo en el 25% del Qb; volumen de infusión constante en función del dializador, Hto. y proteínas (AutoSub. FMC ®); control presión (PTM o Ppre) constante e infusión variable (Max –Sub, Surdial-X. Nipro®; AutoFinf, Flexia. Mozarc Medical®; PTM Sub-Control. DBB-EXA, Nikkiso®); Calculadora, Dialog iQ, Braun®; Ultracontrol Artis, Baxter® y AutoSub Plus, 5008, 6008, FMC®.
El sistema Ultracontrol de Baxter® consigue FF del 30 % de media, lo que posibilita alcanzar volúmenes totales de ultrafiltración de 30 L en sesiones de 4 horas [68]. El sistema Autosub Plus de FMC® puede conseguir también FF elevadas sin complicaciones [69].
5. Sistema informático. Comunicaciones del monitor.
Un aspecto de suma importancia en los monitores de HD es su conectividad informática. Lo ideal es que el monitor tenga una conexión, interfaz, bidireccional con el servidor informático de la unidad de HD; sea capaz de ser programado de forma remota o mediante una tarjeta y que pueda volcar los datos de la sesión de HD en el servidor, que deberá contar con un programa informático específico para HD.
El monitor debe proporcionar una interfaz para la conexión a una red informática, por ejemplo, a un sistema de gestión de datos de pacientes (PDMS). Los sistemas de red de la Unidad de HD deben cumplir la norma IEC 60601-1-2.
El sistema de conexión debe permitir supervisar a distancia las sesiones de HD, incluso generando señales de alarma remota.
Debe contar con software opcional para la conexión con los programas informáticos de HD al uso.
Es útil la existencia de puertos USB que permitan acceder a los datos del monitor, que permitan las intervenciones del servicio técnico y las actualizaciones del software.
La denominada tarjeta del paciente que recoge datos del paciente, de la programación habitual de las sesiones y de las últimas sesiones, es una herramienta útil en la Unidades de HD. La tarjeta del paciente se conecta con el monitor a través de un área de contacto.
Las dificultades de algunos monitores para conectarse con ciertos programas informáticos son un grave inconveniente a la hora de elegirlos.
6. Sistemas de automatización de la preparación, conexión, tratamiento; desconexión y desinfección.
Los monitores modernos facilitan mediante la automatización todo el proceso de la sesión de hemodiálisis.
Entre estos automatismos destacan: confirmación de la prescripción de la sesión de cada paciente; colocación de las líneas y dializador; cebado automático; conexión del acceso vascular; inicio del relleno sanguíneo; control del curso de la diálisis / alarmas y desconexión automática.
Las funciones del monitor que facilitan esos automatismos son: inserción automática de líneas; cambio selectivo de líneas en el circuito; cebado y reinfusión con líquido de diálisis; ultrafiltrado del volumen de cebado durante la conexión; reinfusión automática; asistente en la extracción de muestras; detección de acodamientos en las líneas; detección de salida de agujas; tiempo de preparación; tiempo de desinfección; consumo de desinfectante; aclarado del desinfectante; tecla de emergencia.
La desinfección, desincrustación y acción detergente en el mantenimiento de los monitores de HD es fundamental. Cada fabricante recomienda los agentes a utilizar, así como si se puede realizar desinfección por calor en ese monitor. El proceso de desinfección de las máquinas esta automatizado al acabar la sesión de HD.
Todos estos sistemas de automatización facilitan la labor de la enfermería.
7. Tipos de monitores de HD 2025
7.a Comparativa.
En la (Tabla 1) se comparan las prestaciones de los monitores de uso más frecuente, actualmente, en España.
En el anexo 1 se desarrolla la OPINIÓN DE ENFERMERÍA SOBRE EL USO DE LOS DISTINTOS MONITORES PARA HEMODIÁLISIS. Corresponde a un encargo de la Dirección de Gestión y Dirección de Enfermería del H.U. Infanta Leonor de Madrid a la Unidad de Hemodiálisis/Nefrología, en el que se valoran, desde el punto de vista de la enfermería, los monitores de hemodiálisis al uso.
7.b La opinión de la enfermería.
¿Qué aspectos de un monitor de hemodiálisis tienen más importancia para la enfermería?
En general, el personal de enfermería valora dos grandes aspectos fundamentales: la seguridad y la gestión de prestaciones de un monitor de hemodiálisis, aunque otros aspectos de funcionalidad y medioambientales, también resultan de interés añadido.
Seguridad del circuito extracorpóreo
Entre los aspectos ligados a la seguridad del circuito extracorpóreo debemos destacar un sistema de alarmas que nos alerten de forma inmediata ante cualquier evento, fácil interpretación de estos y, ante todo, seguridad y facilidad para poder resolver dichos eventos.
• Ajuste seguro de límites de alarmas
• Detección de acodamientos
• Detección de salida de agujas
• Tecla de emergencia que permita de forma rápida el paro de la UF, toma de TA e infusión de bolo para solucionar eventos hipovolémicos
• Cambio selectivo de las líneas en el circuito
• Fácil resolución de alarmas
• Longitud adecuada de las líneas arterial y venosa, así como localización de las zonas de punción.
Seguridad durante el tratamiento
La seguridad durante el tratamiento es un aspecto crucial que debe ser cuidadosamente considerado para garantizar la adecuación y efectividad de la sesión. Los biosensores juegan un papel fundamental en este contexto, ya que permiten al personal sanitario evaluar y valorar datos relevantes en tiempo real. Es esencial que estos dispositivos proporcionen información precisa y oportuna sobre varios parámetros, tales como:
• Medición de la dosis de diálisis
• Valores dosis de diálisis
• Recirculación
• Volumen plasmático (BVM)
• Saturación oxígeno
• Medición del coeficiente de ultrafiltración (Kuf)
• Medición del índice de relleno plasmático
• Hemocontrol
• Control de Na
Seguridad en el registro de los tratamientos
Los aspectos de seguridad relacionados con la información y registro de los tratamientos van ligados a la integración con el programa informático y la historia clínica del paciente, por lo que la mayor integración entre el programa y los monitores, así como la bidireccionalidad que permita validar esos datos, son aspectos cuya relevancia se va incrementando progresivamente.
Gestión de los monitores
Otros aspectos también importantes, pero quizá menos relevantes, serán los relacionados con la manipulabilidad del monitor, es decir, facilidad y sencillez de montaje, actuaciones automáticas como realización y finalización de cebado, fácil ajuste de datos de tratamiento, así como su localización dentro del sistema y fácil interpretación. En este aspecto también resulta valorable la facilidad para realizar ajustes o cambios de tratamiento como poder programar UF secas dentro del tratamiento, cambios a técnica de unipunción, por ejemplo. En este sentido también serían valorables aspectos como:
• Encendido automático del monitor
• Sencillez de montaje
• Cebado automático
• Cebado y reinfusión con líquido de diálisis
• Reinfusión automática
• Tiempo de preparación
• Tiempo de desinfección
• Modo eco
• Retorno automático
• Vaciado de líneas
Por otro lado, serían valorables aspectos que, no siendo relevantes para el tratamiento, si son de gran valor por su impacto medioambiental:
• Consumo Energético: Es importante que los monitores sean eficientes en términos energéticos para reducir su impacto ambiental.
• Consumo de agua: Es importante la optimización del consumo del agua en los tratamientos de diálisis, para reducir costes operativos y contribuir a la sostenibilidad ambiental.
• Materiales Sostenibles: La fabricación debe considerar el uso de materiales reciclables o biodegradables para minimizar residuos.
• Gestión de Residuos: Los monitores generan desechos (como dializadores y tubos) que deben ser gestionados adecuadamente para evitar contaminación.
En el anexo 1 se describe la opinión de enfermería sobre el uso de los distintos monitores para hemodiálisis.
7.c Monitores para HD domiciliaria.
La HD domiciliaria es la mejor opción de HD cuando se compara con la hospitalaria o la realizada en centros satélites. Hay que tener en cuenta que implica la selección de pacientes. Cualquier monitor de HD se puede utilizar en el domicilio del paciente siempre que se instale un acceso eléctrico adecuado, una adecuación de fontanería, toma de agua y drenaje y el tratamiento del agua necesario. Para facilitar esta opción terapéutica se han desarrollado monitores más sencillos de manejar y en gran medida portátiles. Pueden funcionar con bolsas de LD, que es la opción más utilizada, o con un sistema de fabricación de LD con agua purificada. Entre los monitores más utilizados destacan: NX STAGE SYSTEM ONE. FMC®; PHYSIDIA S3. PALEX®; MONITOR AK 98. BAXTER INT®; MONITOR 5008 VERSIÓN HOME. FMC®
8. Posibles mejoras.
Los avances en la hemodiálisis incluyen nuevas técnicas de hemodiafiltración, monitores portátiles, riñones artificiales portables e implantables y riñones bioartificiales. La mayoría de estas tecnologías aún están lejos de su aplicación clínica. Varias organizaciones y empresas, entre ellas la Iniciativa de Salud Renal y Kidney X: El Acelerador de Innovación Renal, así como la Iniciativa Estadounidense para el Avance de la Salud Renal están trabajando en conjunto para desarrollar nuevas terapias que podrían personalizar el tratamiento de la enfermedad renal avanzada [70].
Los dispositivos de hemodiálisis domiciliaria aprobados recientemente por la FDA brindan características que incluyen generación del dializado, desconexión de acceso para el desplazamiento de la aguja venosa, interfaz de pantalla táctil con indicaciones y animaciones visuales y auditivas, cartuchos esterilizados directos con tubos prestrung, desinfección con agua caliente de los tubos, para un uso prolongado, caudales de dializado de hasta 500 ml/min, así como capacidades de monitoreo remoto del tratamiento. Además, actualmente, se están desarrollando dispositivos de diálisis portátiles/portables para simplificar la administración de diálisis a los pacientes [71].
La tecnología SLED (Low efficiency dialisys / Diálisis sostenida de baja eficiencia), permite, además del tratamiento de HD/HDF intermitente estándar, para pacientes agudos. La función SLED permite ampliar la duración del tratamiento con un flujo de líquido de diálisis bajo, para realizar un tratamiento alternativo continuo en pacientes críticos. Estos monitores permiten realizar: CVVHD (hemodiálisis); CVVHDF (hemodiafiltración); SCUF (ultrafiltración); cualquier combinación de CVVHD, CVVHDF y SCUF durante 24 horas y conectividad LAN [72].
La utilización de la inteligencia artificial en HD es incipiente. Permite desarrollar modelos para predecir las probabilidades de ajustar el peso seco en cada sesión [73] y otros aspectos de la HD [74].
ANEXO 1
OPINIÓN DE ENFERMERÍA SOBRE EL USO DE LOS DISTINTOS MONITORES PARA HEMODIÁLISIS
Surdial ™ X (Nipro)
Características generales:
• Monitor: Cuenta con una interfaz de usuario bastante intuitiva y proporciona orientación paso a paso en pantalla.
• Dimensiones: Tiene un diseño compacto y ergonómico, ocupando poco espacio.
• Maniobrabilidad: Está equipado con ruedas grandes que permiten un fácil desplazamiento.
Preparación del líquido de diálisis y montaje:
• Concentrados: Ofrece la posibilidad de conexión a bolsas o garrafas para los concentrados, adaptándose a diferentes configuraciones de suministro.
• Montaje: Carga asistida de los segmentos de la bomba de las diferentes líneas sanguíneas, orientación paso a paso en pantalla. Sistemas de líneas individuales que requieren varias conexiones durante el montaje.
• Encendido: Manual
Cebado de líneas y programación del tratamiento:
• Cebado: Realiza el cebado de las líneas con líquido de diálisis.
• Ahorro de líquido: Una vez finalizado el cebado el sistema activa modo ahorro.
• Programación: Intuitiva, fácil introducción manual de los datos y la programación del tratamiento.
• Tipos de tratamiento: Unipunción doble bomba, HD, HDF POST control presión y volumen.
Progreso del tratamiento, resolución de problemas y manejo de sistemas de biofeedback:
• Interfaz: El sistema proporciona una visión clara del estado del tratamiento, permitiendo monitorizar y ajustar según sea necesario.
• Alarmas: Emite alarmas con mensajes claros e indicaciones de posibles soluciones, facilitando la resolución de problemas.
• Visualización de valores importantes: Los parámetros críticos se muestran en la pantalla principal, facilitando la evaluación continua de la evolución del tratamiento.
o Dosis de diálisis DI (K, Kt, Kt/V,URR)
o Control BVM
o Biocontrol de Na, UF y Na+UF
• Integración sistema informático: Abierto y bidirecional
Desconexión del tratamiento:
• Retorno automático: El sistema no dispone de retorno automático
• Retorno: Permite el retorno en línea de la sangre con suero salino o líquido de diálisis.
• Aviso de final de retorno: El sistema notifica al operador al finalizar el retorno de sangre.
Desinfección y cambios de ultrafiltros:
• Tiempo de desinfección: Tiene un tiempo de desinfección reducido.
• Tipo de desinfección: Utilice desinfectantes suministrados en garrafas.
• Aviso de cambios de ultrafiltros: El sistema avisa cuando es necesario cambiar los ultrafiltros, procedimiento sencillo.
• Apagado: Manual
Artis Physio™ (Gambro-Baxter)
Características generales:
• Monitor: Bastante intuitivo, permitiendo una operación sencilla.
• Dimensiones: Ocupa un espacio moderado y es más pesada que otros modelos.
• Maniobrabilidad: Ruedas pequeñas que facilitan su desplazamiento dentro de las instalaciones
Preparación del líquido de diálisis y montaje:
• Concentrados: El sistema permite la conexión de concentrados a través de bolsas.
• Montaje: Las líneas sanguíneas y de diálisis están diseñadas para un montaje individual y sencillo que requieren de varias conexiones. En pantalla facilita guía de montaje.
• Encendido: Manual
Cebado de líneas y programación del tratamiento:
• Cebado: El sistema ofrece la flexibilidad de realizar el cebado de las líneas con suero salino o líquido de diálisis, dependiendo de la técnica programada.
• Ahorro de líquido: Una vez finalizado el cebado optimiza el uso del líquido de diálisis, contribuyendo a la eficiencia y sostenibilidad del tratamiento.
• Programación: El sistema permite la programación de pautas de tratamiento utilizando tarjetas de paciente, facilitando la personalización y reduciendo errores en la configuración. También permite una fácil introducción manual de datos, con ajustes rápidos y precisos según las necesidades del paciente.
• Tipos de tratamiento: Unipunción doble bomba, HD, HDF POST control presión
Progreso del tratamiento, resolución de problemas y manejo de sistemas de biofeedback:
• Interfaz: El sistema está diseñado para un manejo sencillo, permitiendo una programación eficiente y adaptada a las necesidades específicas de cada paciente. Durante la sesión, el sistema proporciona información clara y accesible.
• Alarmas: Emite alarmas con mensajes descriptivos que indican posibles soluciones, facilitando una respuesta rápida y efectiva ante cualquier incidencia.
• Programación de alertas: Permite configurar alertas personalizadas
• Visualización de valores importantes: Los parámetros críticos del tratamiento se muestran en la pantalla principal, facilitando la evaluación continua y la toma de decisiones clínicas informadas. Flexibilidad de ajustar parámetros del tratamiento en curso, adaptándose a las necesidades cambiantes del paciente durante la diálisis.
o Dosis de diálisis DI (K, Kt, Kt/V)
o Control Na plasmático
o Control BVM
o Biocontrol: Hemocontrol
• Integración sistema informático: Abierto y bidirecional
Desconexión del tratamiento:
• Retorno automático: El sistema no dispone de retorno automático
• Retorno: Permite un retorno de las líneas con suero salino o líquido de diálisis.
• Aviso de final de retorno: El sistema emite notificaciones al completar el retorno de sangre.
Desinfección y cambios de ultrafiltros:
• Tiempo de desinfección: Tiene un tiempo de desinfección reducido.
• Tipos de desinfección: Ofrece varias opciones de desinfección, incluyendo métodos térmicos y químicos. El sistema es compatible con desinfectantes suministrados en garrafas o en formatos concentrados en polvo.
• Aviso de cambios de ultrafiltros: El sistema avisa cuando es necesario cambiar los ultrafiltros, procedimiento sencillo.
• Apagado: Manual
5008 CorDiax
Características generales:
• Monitor: La interfaz de usuario está diseñada para facilitar su uso, muy intuitiva.
• Dimensiones: Tamaño medio.
• Maniobrabilidad: Su diseño ergonómico permite un fácil manejo.
Preparación del líquido de diálisis y montaje:
• Concentrados: El sistema permite la conexión de concentrados a través de bolsas.
• Montaje: Líneas individuales con carga asistida de los segmentos de la bomba, permiten un montaje sencillo y eficiente, requiere varias conexiones para su montaje.
• Encendido: Manual
Cebado de líneas y programación del tratamiento:
• Cebado: Ofrece opciones de cebado con suero salino o líquido de diálisis según las necesidades del tratamiento.
• Ahorro de líquido: Una vez finalizado el cebado el sistema activa modo ahorro
• Programación: El sistema permite la programación de pautas de tratamiento utilizando tarjetas de paciente, facilitando la personalización y reduciendo errores en la configuración. También permite una fácil introducción manual de datos.
• Tipos de tratamiento: Unipunción doble bomba, HD, HDF PRE y POST autoSub y MIXED
Progreso del tratamiento, resolución de problemas y manejo de los sistemas de biofeedback:
• Interfaz: Intuitiva durante el tratamiento. Facilita la monitorización en tiempo real permitiendo ajustes según las necesidades del paciente.
• Alarmas: Mensajes de alarmas claros con posibles soluciones: Proporciona alertas detalladas para una intervención rápida. Diseñada para una resolución eficiente de problemas.
• Alertas: Permite establecer notificaciones personalizadas para diversos eventos.
• Visualización de valores importantes: En la pantalla principal muestra parámetros clave para evaluar la evolución del paciente.
o Dosis de diálisis OCM (K, Kt, Kt/V)
o Control Na plasmático
o Recirculación por BTM
o Control BVM
o Biocontrol: UF
• Sistema de conexión informática: Cerrado y bidireccional, solo con Nefrolink
Desconexión del tratamiento:
• Retorno automático: Dispone de funciones que facilitan la finalización del tratamiento.
• Retorno: Permite el retorno en línea de la sangre con suero salino o líquido de diálisis.
• Aviso de final de retorno: El sistema notifica al operador al finalizar el retorno de sangre.
Desinfección y cambios de ultrafiltros:
• Tiempo de desinfección: Tiene un tiempo de desinfección reducido.
• Tipo de desinfección: Utilice desinfectantes suministrados en garrafas.
• Aviso de cambios de ultrafiltros: El sistema avisa cuando es necesario cambiar los ultrafiltros, procedimiento rápido y sencillo.
• Apagado: Automático tras la desinfección
6008 CorDiax
Características generales:
• Monitor: La interfaz de usuario está diseñada para facilitar su uso, muy intuitiva.
• Dimensiones: Tamaño medio.
• Maniobrabilidad: Su diseño ergonómico permite un fácil manejo.
Preparación del líquido de diálisis y montaje:
• Concentrados: El sistema permite la conexión de concentrados a través de bolsas.
• Montaje: Líneas en cassette permiten un montaje sencillo y eficiente. No requiere de varias conexiones para su montaje.
• Encendido: Manual
Cebado de líneas y programación del tratamiento:
• Cebado: Ofrece opciones de cebado con suero salino o líquido de diálisis según las necesidades del tratamiento.
• Ahorro de líquido: Una vez finalizado el cebado el sistema activa modo ahorro
• Programación: El sistema permite la programación de pautas de tratamiento utilizando tarjetas de paciente, facilitando la personalización y reduciendo errores en la configuración. También permite una fácil introducción manual de datos.
• Tipos de tratamiento: Unipunción doble bomba, HD, HDF PRE y POST autoSub
Progreso del tratamiento, resolución de problemas y manejo de los sistemas de biofeedback:
• Interfaz: Intuitiva durante el tratamiento. Facilita la monitorización en tiempo real permitiendo ajustes según las necesidades del paciente.
• Alarmas: Mensajes de alarmas claros con posibles soluciones: Proporciona alertas detalladas para una intervención rápida. Diseñada para una resolución eficiente de problemas.
• Alertas: Permite establecer notificaciones personalizadas para diversos eventos.
• Visualización de valores importantes: En la pantalla principal muestra parámetros clave para evaluar la evolución del paciente.
o Dosis de diálisis OCM (K, Kt, Kt/V)
o Control Na plasmático
o Recirculación por BTM
o Control BVM
o Biocontrol: UF
• Sistema de conexión informática: Cerrado y bidireccional, solo con Nefrolink
Desconexión del tratamiento:
• Retorno automático: Dispone de sistema de retorno automático.
• Retorno: Permite el retorno en línea de la sangre con suero salino o líquido de diálisis.
• Aviso de final de retorno: El sistema notifica al operador al finalizar el retorno de sangre.
Desinfección y cambios de ultrafiltros:
• Tiempo de desinfección: Tiene un tiempo de desinfección reducido.
• Tipo de desinfección: Utilice desinfectantes suministrados en garrafas.
• Aviso de cambios de ultrafiltros: El sistema avisa cuando es necesario cambiar los ultrafiltros, procedimiento rápido y sencillo.
• Apagado: Automático tras la desinfección
Flexya de Mozarc Medical.
Características generales:
• Monitor: Interfaz intuitiva que facilita su operación.
• Dimensiones: Tamaño medio grande.
• Maniobrabilidad: Ruedas pequeñas que facilitan su desplazamiento dentro de las instalaciones
Preparación del líquido de diálisis y montaje:
• Concentrados: El sistema permite la conexión de concentrados a través de bolsas y garrafas.
• Montaje: Líneas individuales con carga asistida de los segmentos de la bomba, permiten un montaje sencillo y eficiente, requiere varias conexiones para su montaje.
• Encendido automático: Dispone de funciones automatizadas que mejoran la eficiencia en su uso diario.
Cebado de líneas y programación del tratamiento:
• Cebado: Ofrece opciones de cebado con suero salino o líquido de diálisis según las necesidades y preferencias del tratamiento.
• Ahorro de líquido: Optimiza el uso de líquidos durante el tratamiento, contribuyendo a la eficiencia y sostenibilidad.
• Programación: El sistema permite la programación de pautas de tratamiento utilizando tarjetas de paciente, facilitando la personalización y reduciendo errores en la configuración. También permite una fácil introducción manual de datos sencilla e intuitiva.
• Tipos de tratamiento: Unipunción doble bomba, HD, HDF PRE y POST control volumen presión.
Progreso del tratamiento y resolución de problemas y manejo de los sistemas de biofeedback:
• Interfaz: Intuitiva durante el tratamiento. Facilita la monitorización en tiempo real permitiendo ajustes según las necesidades del paciente.
• Alarmas: Proporciona alertas detalladas que guían al usuario en la resolución de problemas, mejorando la seguridad del paciente y minimizando interrupciones en el tratamiento.
• Alertas: Permite establecer notificaciones personalizadas para diversos eventos, mejorando la gestión del tratamiento.
• Visualización de valores críticos: En la pantalla principal muestra parámetros clave para evaluar la evolución del paciente de manera continua.
o Dosis de diálisis Natrium (K, Kt, Kt/V, URR)
o Control BVM Hemox
o Medición de la Saturación de oxígeno.
• Sistema de conexión informática: Abierto.
Desconexión del tratamiento:
• Retorno automático: Dispone de funciones que facilitan la finalización del tratamiento de manera segura y eficiente.
• Retorno: Ofrece opciones para el retorno de sangre en línea con solución online o SSF
• Aviso de final de retorno: Notifica cuando el proceso de retorno haya concluido.
Desinfección y cambios de ultrafiltros:
• Tiempo de desinfección: Tiene un tiempo de desinfección reducido.
• Tipo de desinfección: Utilice desinfectantes suministrados en garrafas.
• Aviso de cambios de ultrafiltros: El sistema avisa cuando es necesario cambiar los ultrafiltros, procedimiento rápido y sencillo.
• Apagado: Automático tras la desinfección
NIKKISO DBB-EXA™
Características generales:
• Monitor: La interfaz de usuario está diseñada para facilitar su uso, muy intuitiva.
• Dimensiones: Tamaño compacto.
• Maniobrabilidad: Su diseño ergonómico permite un fácil manejo.
Preparación del líquido de diálisis y montaje:
• Concentrados: El sistema permite la conexión de concentrados a través de garrafas.
• Montaje: Las líneas sanguíneas y de diálisis están diseñadas para un montaje individual y sencillo que requieren de varias conexiones.
Cebado de líneas y programación del tratamiento:
• Cebado: Posibilidad de cebado con solución salina o líquido de diálisis, según la técnica programada.
• Ahorro de líquido: Al finalizar el cebado, el sistema optimiza el uso del líquido, reduciendo el desperdicio.
• Programación: Interfaz que facilita la introducción de datos de programación, permitiendo ajustes manuales o mediante tarjeta de paciente.
• Tipos de tratamiento: Unipunción doble bomba, HD, HDF y POST control volumen presión.
Progreso del tratamiento, resolución de problemas y manejo de los sistemas de biofeedback:
• Interfaz: Operación intuitiva durante el tratamiento, con monitoreo en tiempo real. Capacidad para modificar parámetros del tratamiento en curso, adaptándose a las necesidades del paciente.
• Alarmas: Mensajes de alarma claros que indican posibles soluciones, mejorando la respuesta ante incidencias.
• Alertas: Posibilidad de programar alertas personalizadas para un monitoreo proactivo.
• Visualización de valores críticos: Visualización de valores críticos en la pantalla principal para evaluar la evolución del tratamiento. Sistemas de biofeedback que permiten ajustes automáticos basados en parámetros fisiológicos del paciente.
o Dosis de diálisis absorbancia (K, Kt, Kt/V, MDD)
o Medición de la recirculación.
o Biocontrol UF y conductividad.
• Sistema de conexión informática: Abierto.
Desconexión del tratamiento:
• Retorno automático: Función de retorno automático de sangre, garantizando una finalización segura del tratamiento.
• Retorno: Permite el retorno en línea de la sangre con suero salino o líquido de diálisis.
• Aviso de final de retorno: Aviso al finalizar el retorno, asegurando una desconexión adecuada.
Desinfección y cambios de ultrafiltros:
• Tiempo de desinfección: Tiene un tiempo de desinfección reducido.
• Tipo de desinfección: Uso de desinfectantes en garrafas o concentrados en polvo, según preferencia.
• Aviso de cambios de ultrafiltros: Notificaciones para el cambio de ultrafiltros y diseño que facilita su cambio.
• Apagado: automático tras la desinfección, optimizando el tiempo y los recursos.
Dialog iQ de B. Braun
Características generales:
• Monitor: El sistema está diseñado para facilitar su uso, permitiendo una operación sencilla y eficiente.
• Dimensiones: Tamaño compacto.
• Maniobrabilidad: Su diseño ergonómico permite un fácil manejo.
Preparación del líquido de diálisis y montaje:
• Conexión de concentrados: Permite la conexión eficiente de los concentrados necesarios para la preparación del líquido de diálisis.
• Montaje: Líneas individuales con carga asistida de los segmentos de la bomba, permiten un montaje sencillo y eficiente, requiere varias conexiones para su montaje.
• Tipos de tratamiento: HDF POST control presión
Cebado de líneas y programación del tratamiento:
• Cebado con suero salino o líquido de diálisis: Posibilidad de cebado con solución salina o líquido de diálisis, según la técnica programada.
• Ahorro de líquido: Una vez finalizado el cebado, el sistema optimiza el uso de líquidos, contribuyendo a la eficiencia del tratamiento.
• Programación: Requiere la introducción de parámetros específicos para personalizar el tratamiento según las necesidades del paciente.
• Facilidad para introducir datos: La interfaz de usuario está diseñada para una entrada de datos rápida y sin complicaciones.
Progreso del tratamiento, resolución de problemas y manejo de los sistemas de biofeedback:
• Interfaz: El monitor proporciona información clara y accesible, facilitando la supervisión continua.
• Alarmas: En caso de irregularidades, el sistema emite alertas detalladas que incluyen posibles acciones correctivas.
• Alertas: Se pueden establecer alertas personalizadas para diversos parámetros, mejorando la seguridad y eficacia del tratamiento.
• Visualización de valores clave en la pantalla principal: Los parámetros más importantes se muestran de manera prominente, permitiendo una evaluación continua de la evolución del paciente.
o Dosis de diálisis absorbancia (UV, Kt/V y URR)
o BVM sensor hematocrito.
o Control de la saturación de oxígeno.
o Biocontrol UF
• Sistema de conexión informática: Abierto y bidireccional solo con Nexadia.
Desconexión del tratamiento:
• Retorno automático: El sistema facilita el proceso de finalización del tratamiento, asegurando una desconexión segura y eficiente.
• Retorno: Permite la reinfusión en línea con liquido de dialisis, optimizando la eficiencia y seguridad del procedimiento.
• Aviso de final de retorno: Aviso cuando el proceso de retorno ha concluido.
Desinfección y cambios de ultrafiltros:
• Tiempo de desinfección: Tiene un tiempo de desinfección reducido.
• Tipos de desinfección: Ofrece diversos métodos de desinfección, adaptándose a los protocolos
• Aviso de cambios de ultrafiltros: Notificaciones para el cambio de ultrafiltros y diseño que facilita su cambio.
• Apagado: El sistema puede programarse para realizar un apagado automático tras la desinfección.
Figuras
Referencias bibliográficas
1
.
Ahmad S, Misra M, Hoenich N, Daugirdas JT. Hemodialysis apparatus. Handbook of dialysis. John T. Daugirdas, Peter G. Blake, Todd S. Ing. 5th Ed. 2015; 66-88.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2015%3B+66-88
2
.
Pérez-García R y Mª Patrocinio Rodríguez Benítez. Los filtros de endotoxinas / ultrafiltros para hemodiálisis y hemodiafiltración en línea (HDF-OL). Anexo 2.2.3 de la Guía de Gestión de Calidad del Líquido de Diálisis (LD) (Segunda edición - 2015).
http://www.ncbi.nlm.nih.gov/pubmed/?term=3+de+la+Gu%C3%ADa+de+Gesti%C3%B3n+de+Calidad+del+L%C3%ADquido+de+Di%C3%A1lisis+%28LD%29+%28Segunda+edici%C3%B3n+-+2015%29
3
.
Albalate M, Pérez-García R, de Sequera P, Corchete E, Alcazar R, Ortega M, Puerta M. Is it useful to increase dialysate flow rate to improve the delivered Kt? BMC Nephrol. 2015 Feb 14;16:20. doi: 10.1186/s12882-015-0013-9. PMID: 25884763; PMCID: PMC4369100.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+25884763%3B+PMCID%3A+PMC4369100
4
.
Maduell F, Ojeda R, Arias-Guillén M, Fontseré N, Vera M, Massó E, Gómez M, Rodas L, Bazán G, Jiménez-Hernández M, Piñeiro G, Rico N. Optimization of dialysate flow in on-line hemodiafiltration. Nefrologia. 2015;35(5):473-8. English, Spanish. doi: 10.1016/j.nefro.2015.06.019. Epub 2015 Jul 22. PMID: 26306957.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+26306957
5
.
Pérez-García R, Palomares I, Merello JI, Ramos R, Maduell F, Molina M, Aljama P, Marcelli D; ORD Group. Hyponatraemia, mortality and haemodialysis: An unexplained association. Nefrologia. 2016;36(1):42-50. English, Spanish. doi: 10.1016/j.nefro.2015.10.005. Epub 2015 Dec 3. PMID: 26656402.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+26656402
6
.
Albalate Ramón M, de Sequera Ortiz P, Pérez-García R, Ruiz-Álvarez MJ, Corchete Prats E, Talaván T, Alcázar Arroyo R, Puerta Carretero M, Ortega-Díaz M. Sodium set-point in haemodialysis: is it what we see clinically? Nefrologia. 2013 Nov 13;33(6):808-15. English, Spanish. doi: 10.3265/Nefrologia.pre2013.Sep.12117. PMID: 24241368.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+24241368
7
.
Sternby J. Urea sensors ¿ a world of possibilities. Adv Ren Replace Ther 1999; 6: 265¿272.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Adv+Ren+Replace+Ther+1999%3B+6%3A+265%E2%80%93272
8
.
Polaschegg HD. Automatic, noninvasive intradialytic clearance measurement. Int. J. Artif Organs 1993; 16:185¿191.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Artif+Organs+1993%3B+16%3A185%E2%80%93191
9
.
Aslam S, Saggi SJ, Salifu M, Kossmann RJ. Online measurement of hemodialysis adequacy using effective ionic dialysance of sodium-a review of its principles, applications, benefits, and risks. Hemodial Int 2018;22:425-434.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Hemodial+Int+2018%3B22%3A425-434
10
.
Daugirdas JT. Eliminating the need for routine monthly postdialysis serum urea nitrogen measurement: A method for monitoring Kt/V and normalized protein catabolic rate using conductivity determined dialyzer clearance. Semin Dial. 2018;31:633¿636.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2018%3B31%3A633%E2%80%93636
11
.
Maduell F., Vera M., Arias M., et al: Influence of the ionic dialysance monitor on Kt measurement in hemodialysis. Am J Kidney Dis 2008; 52: pp. 85-92.
http://www.ncbi.nlm.nih.gov/pubmed/?term=85-92
12
.
Castellarnau A, Werner M, Günthner R, et al. Real-time Kt/V determination by ultraviolet absorbance in spent dialysate: technique validation. Kidney Int 2010; 78(9):920¿925
http://www.ncbi.nlm.nih.gov/pubmed/?term=Kidney+Int+2010%3B+78%289%29%3A920%E2%80%93925
13
.
Uhlin F, Fridolin I, Lindberg L et al. Estimation of delivered dialysis dose by on-line onitoring of the ultraviolet absorbance in the spent dialysate.Am J Kidney Dis 2003; 41: 1026¿1036.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Am+J+Kidney+Dis+2003%3B+41%3A+1026%E2%80%931036
14
.
Ross EA, Paugh-Miller JL, Nappo RW. Interventions to improve hemodialysis adequacy: protocols based on real-time monitoring of dialysate solute clearance. Clin Kidney J 2018;11:394-399.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Clin+Kidney+J+2018%3B11%3A394-399
15
.
Mohamed A, Davenport A. Comparison of methods to estimate haemodialysis urea clearance. Int J Artif Organs 2018;41:371-377.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Int+J+Artif+Organs+2018%3B41%3A371-377
16
.
Schneditz D, Pogglitsch H, Horina J, Binswanger U. A blood protein monitor for the continuous measurement of blood volume changes during hemodialysis. Kidney Int 1990;38:342-346.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Kidney+Int+1990%3B38%3A342-346
17
.
Johner C, Chamney PW, Schneditz D, Krämer M. Evaluation of an ultrasonic blood volume monitor. Nephrol Dial Transplant 1998; 13:2098-103.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nephrol+Dial+Transplant+1998%3B+13%3A2098-103
18
.
Dasselaar JJ et al. Relative blood volume measurements during hemodialysis: Comparisons between three noninvasive devices. Hemodialysis Int.2007: 11:448¿455.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2007%3A+11%3A448%E2%80%93455
19
.
Dasselaar JJ, van der Sande FM, Franssen CF. Critical evaluation of blood volume measurements during hemodialysis. Blood Purif 2012;33:177-82.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Blood+Purif+2012%3B33%3A177-82
20
.
Van Buren PN. Relative blood volume monitoring in hemodialysis patients: identifying its appropriate role. Nephrol Dial Transplant 2019 34: 1251¿1253
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nephrol+Dial+Transplant+2019+34%3A+1251%E2%80%931253
21
.
Keane DF, Baxter P, Lindley E, Rhodes L, Pavitt S. Time to Reconsider the Role of Relative Blood Volume Monitoring for Fluid Management in Hemodialysis. ASAIO J 2018;64:812-818.
http://www.ncbi.nlm.nih.gov/pubmed/?term=ASAIO+J+2018%3B64%3A812-818
22
.
Kron S, Wenkel R, Leimbach T, Aign S, Kron J: Effects of sodium on measuring relative blood volume during hemodialysis differ by techniques. ASAIO J 2013; 59: 612¿616.
http://www.ncbi.nlm.nih.gov/pubmed/?term=ASAIO+J+2013%3B+59%3A+612%E2%80%93616
23
.
Kron S, Wenkel R, Leimbach T, Aign S, Kron J: Effects of osmotic changes on measuring relative blood volume: comparison of three hemodialysis devices. ASAIO J 2016;62: 214¿215.
http://www.ncbi.nlm.nih.gov/pubmed/?term=ASAIO+J+2016%3B62%3A+214%E2%80%93215
24
.
Kron S, Schneditz D, Czerny J, Leimbach T, Budde K, Kron J. Adjustment of target weight based on absolute blood volume reduces the frequency of intradialytic morbid events. Hemodial Int. 2018;22:254-260.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2018%3B22%3A254-260
25
.
Bullen A, Rifkin D, Trzebinska D. Individualized Cool Dialysate as an Effective Therapy for Intradialytic Hypotension and Hemodialysis Patients'''' Perception. Ther Apher Dial 2019;23:145-152.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Ther+Apher+Dial+2019%3B23%3A145-152
26
.
Tsujimoto_Y, Tsujimoto_H, Nakata_Y, Kataoka_Y, Kimachi_M, Shimizu_S, Ikenoue_T, Fukuma_S, Yamamoto_Y, Fukuhara_S.Dialysate temperature reduction for intradialytic hypotension for people with chronic kidney disease requiring haemodialysis. Cochrane Database of Systematic Reviews 2019, Issue 7. Art. No.: CD012598. DOI: 10.1002/14651858.CD012598.pub2.
http://www.ncbi.nlm.nih.gov/pubmed/?term=pub2
27
.
Van der Sande FM, Gladziwa U, Kooman JP, Böcker G, Leunissen KML: Energy transfer is the single most important factor for the difference in vascular response between isolated ultrafiltration and hemodialysis. J Am Soc Nephrol 2000; 11: 1512-17.
http://www.ncbi.nlm.nih.gov/pubmed/?term=J+Am+Soc+Nephrol+2000%3B+11%3A+1512-17
28
.
Mustafa RA, Bdair F, Akl EA, et al. Effect of lowering the dialysate temperature in chronic hemodialysis: a systematic review and meta-analysis. Clin J Am Soc Nephrol 2016; 11:442¿457.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Clin+J+Am+Soc+Nephrol+2016%3B+11%3A442%E2%80%93457
29
.
Maggiore Q. Isothermic dialysis for hypotension-prone patients. Semin Dial 2002;15:187-90.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Semin+Dial+2002%3B15%3A187-90
30
.
Ramos R, Soto C, Mestres R, Jara J, Zequera H, Merello JI, Moreso F. How can we improve symptomatic hypotension in hemodialysis patients: cold dialysis vs isothermic dialysis]. Nefrologia 2007;27:737-41.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nefrologia+2007%3B27%3A737-41
31
.
Kooman JP, van der Sande FM. Body Fluids in End-Stage Renal Disease: Statics and Dynamics. Blood Purif 2019;47:223-229.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Blood+Purif+2019%3B47%3A223-229
32
.
Rotondi S, Tartaglione L, Muci ML, Farcomeni A, Pasquali M, Mazzaferro S. Oxygen Extraction Ratio (OER) as a Measurement of Hemodialysis (HD) Induced Tissue Hypoxia: A Pilot Study. Sci Rep 2018;8:5655.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Sci+Rep+2018%3B8%3A5655
33
.
Mancini E, Perazzini C, Gesualdo L, Aucella F, Limido A, Scolari F, Savoldi S,Tramonti M, Corazza L, Atti M, Severi S, Bolasco P, Santoro A; Italian Oxygen Saturation Study Group (SOGLIA). Intra-dialytic blood oxygen saturation (SO(2)): association with dialysis hypotension (the SOGLIA Study). J Nephrol 2017;30:811-819.
http://www.ncbi.nlm.nih.gov/pubmed/?term=J+Nephrol+2017%3B30%3A811-819
34
.
Chan L, Zhang H, Meyring-Wösten A, Campos I, Fuertinger D, Thijssen S, Kotanko P. Intradialytic Central Venous Oxygen Saturation is Associated with Clinical Outcomes in Hemodialysis Patients. Sci Rep. 2017;7:8581.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2017%3B7%3A8581
35
.
Campos I, Chan L, Zhang H, Deziel S, Vaughn C, Meyring-Wösten A, Kotanko P.Intradialytic Hypoxemia in Chronic Hemodialysis Patients. Blood Purif 2016;41:177-87.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Blood+Purif+2016%3B41%3A177-87
36
.
Harrison LE, Selby NM, McIntyre CW. Central venous oxygen saturation: a potential new marker for circulatory stress in haemodialysis patients? Nephron Clin Pract. 2014;128:57-60.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2014%3B128%3A57-60
37
.
Cordtz J, Olde B, Solem K, Ladefoged SD. Central venous oxygen saturation and thoracic admittance during dialysis: new approaches to hemodynamic monitoring. Hemodial Int 2008;12:369-77.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Hemodial+Int+2008%3B12%3A369-77
38
.
Mercadal L, Hamani A, Béné B, Petitclerc T. Determination of access blood flow from ionic dialysance: Theory and validation. Kidney Int 1999;56:1560-5.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Kidney+Int+1999%3B56%3A1560-5
39
.
Roca-Tey R, Ibeas López J. Update on vascular access for hemodialysis: The new spanish clinical guideline. Nefrologia 2017;37 (S1):1-192.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nefrologia+2017%3B37+%28S1%29%3A1-192
40
.
Schneditz D, Kaufman AM, Levin N. Surveillance of access function by the blood temperature monitor. Semin Dial 2003;16:483-7.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Semin+Dial+2003%3B16%3A483-7
41
.
Wijnen E, van der Sande FM, Kooman JP, de Graaf T, Tordoir JH, Leunissen KM, et al. Measurement of hemodialysis vascular access flow using extracorporeal temperature gradients. Kidney Int 2007;72:736-41.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Kidney+Int+2007%3B72%3A736-41
42
.
Santos SF, Peixoto AJ. Revisiting the dialysate sodium prescription as a tool for better blood pressure and interdialytic weight gain management in hemodialysis patients. Clin J Am Soc Nephrol 2008;3:522-30.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Clin+J+Am+Soc+Nephrol+2008%3B3%3A522-30
43
.
Stragier A, Lopot F, ¿vára F, Polakovi¿ V. Fallacies and Pitfalls of Dialysis Sodium Prescription and Control. Blood Purif 2018; 46:27-33.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Blood+Purif+2018%3B+46%3A27-33
44
.
Maduell F, Navarro V. [Assessment of salt intake in hemodialysis]. Nefrología 2001;21:71-7.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nefrolog%C3%ADa+2001%3B21%3A71-7
45
.
Hernández-Jaras J, García-Pérez H, Torregrosa E, Calvo C, Cerrillo V.[Usefulness of the Biofeedback Diacontrol module in the automatic programming of plasmatic conductivity and ionic mass transfer]. Nefrologia 2003;23:62-70.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nefrologia+2003%3B23%3A62-70
46
.
Manlucu J, Gallo K, Heidenheim PA, Lindsay RM. Lowering postdialysis plasma sodium (conductivity) to increase sodium removal in volume-expanded hemodialysis patients: a pilot study using a biofeedback software system. Am J Kidney Dis 2010;56:69-76.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Am+J+Kidney+Dis+2010%3B56%3A69-76
47
.
Odudu A, Lambie S, Taal MW, Fluck RJ, McIntyre CW. Use of online conductivity monitoring to study sodium mass balance in chronic haemodialysis patients: prospects for treatment individualisation. Kidney Blood Press Res 2011;34:439-46.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Kidney+Blood+Press+Res+2011%3B34%3A439-46
48
.
Bosetto A, Béné B, Petitclerc T. Sodium management in dialysis by conductivity. Adv Ren Replace Ther 1999;6:243-54.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Adv+Ren+Replace+Ther+1999%3B6%3A243-54
49
.
Locatelli F, Stefoni S, Petitclerc T, Colì L, Di Filippo S, Andrulli S, Fumeron C, Frascà GM, Sagripanti S, Savoldi S, Serra A, Stallone C, Aucella F, Gesuete A, Scarlatella A, Quarello F, Mesiano P, Ahrenholz P, Winkler R, Man¬dart L, Fort J, Tielemans C, Navino C: Effect of a plasma sodium biofeedback system ap¬plied to HFR on the intradialytic cardiovascu¬lar stability. Results from a randomized con¬trolled study. Nephrol Dial Transplant 2012; 27: 3935¿3942.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nephrol+Dial+Transplant+2012%3B+27%3A+3935%E2%80%933942
50
.
Nacca R, Fini R, Vezza E, Simeoni P, Porcu M, Bartolomucci M, Trombetta M,Rifici N, Palombo P, Lamberti M, Di Silva A, Treglia A, Caliendo A, Simonelli R, Corazza L, Atti M. [HFR-AEQUILIBRIUM and intradialytic cardiovascular stability: results of the first multicenter study in Lazio]. G Ital Nefrol. 2013;30. pii: gin/30.5.13.
http://www.ncbi.nlm.nih.gov/pubmed/?term=13
51
.
Donati G, Ursino M, Spazzoli A, Natali N, Schillaci R, Conte D, Angeletti A,Croci Chiocchini AL, Capelli I, Baraldi O, La Manna G. Sodium Prescription in the Prevention of Intradialytic Hypotension: New Insights into an Old Concept. Blood Purif. 2018;45(1-3):61-70.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2018%3B45%281-3%29%3A61-70
52
.
Mercadal L, Piékarski C, Renaux JL, Petitclerc T, Deray G. Isonatric dialysis biofeedback in hemodiafiltration with online regeneration of ultrafiltrate (HFR): rationale and study protocol for a randomized controlled study. J Nephrol. 2012;25:1126-30.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2012%3B25%3A1126-30
53
.
Petitclerc T, Gaillard F. [The different modalities of isonatric hemodialysis]. Nephrol Ther. 2019;15:22-28.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2019%3B15%3A22-28
54
.
Gaillard F, Petitclerc T. From Isonatric to Isotonic Hemodialysis. Blood Purif 2018;46:77-80. Kuhlmann U, Maierhofer A, Canaud B, Hoyer J, Gross M. Zero Diffusive Sodium Balance in Hemodialysis Provided by an Algorithm-Based Electrolyte Balancing Controller: A Proof of Principle Clinical Study. Artif Organs. 2019;43:150-158.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2019%3B43%3A150-158
55
.
Petitclerc T. Dialysate sodium management in hemodialysis and online hemodiafiltration: The single-pool kinetic model revisited. Artif Organs. 2022 Nov;46(11):2215-2225. doi: 10.1111/aor.14327. Epub 2022 Jun 14. PMID: 35652561.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+35652561
56
.
Gil HW, Bang K, Lee SY, Han BG, Kim JK, Kim YO, Song HC, Kwon YJ, Kim YS. Efficacy of hemocontrol biofeedback system in intradialytic hypotension-prone hemodialysis patients. J Korean Med Sci 2014;29:805-10.
http://www.ncbi.nlm.nih.gov/pubmed/?term=J+Korean+Med+Sci+2014%3B29%3A805-10
57
.
Nesrallah GE, Suri RS, Guyatt G, Mustafa RA, Walter SD, Lindsay RM, Akl EA. Biofeedback dialysis for hypotension and hypervolemia: a systematic review and meta-analysis. Nephrol Dial Transplant 2013; 28:182-91.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nephrol+Dial+Transplant+2013%3B+28%3A182-91
58
.
Nesrallah GE, Suri RS, Thiessen-Philbrook H, Heidenheim P, Lindsay RM. Can extracellular fluid volume expansion in hemodialysis patients be safely reduced using the hemocontrol biofeedback algorithm? A randomized trial. ASAIO J 2008;54:270-4.
http://www.ncbi.nlm.nih.gov/pubmed/?term=ASAIO+J+2008%3B54%3A270-4
59
.
Locatelli F, Buoncristiani U, Canaud B, Köhler H, Petitclerc T, Zucchelli P. Haemodialysis with on-line monitoring equipment: tools or toys? Nephrol Dial Transplant 2005;20:22-33.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Haemodialysis+with+on-line+monitoring+equipment%3A+tools+or+toys%3F+Nephrol+Dial+Transplant+2005%3B20%3A22-33
60
.
Santoro A, Mancini E, Basile C, Amoroso L, Di Giulio S, Usberti M, Colasanti G, Verzetti G, Rocco A, Imbasciati E, Panzetta G, Bolzani R, Grandi F, Polacchini M. Blood volume controlled hemodialysis in hypotension-prone patients: a randomized, multicenter controlled trial. Kidney Int 2002;62:1034-45.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Kidney+Int+2002%3B62%3A1034-45
61
.
Basile C, Giordano R, Vernaglione L, Montanaro A, De Maio P, De Padova F, Marangi AL, Di Marco L, Santese D, Semeraro A, Ligorio VA. Efficacy and safety of haemodialysis treatment with the Hemocontrol biofeedback system: a prospective medium-term study. Nephrol Dial Transplant 2001;16:328-34.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nephrol+Dial+Transplant+2001%3B16%3A328-34
62
.
Leung KCW, Quinn RR, Ravani P, Duff H, MacRae JM. Randomized Crossover Trial of Blood Volume Monitoring-Guided Ultrafiltration Biofeedback to Reduce Intradialytic Hypotensive Episodes with Hemodialysis. Clin J Am Soc Nephrol 2017;12:1831-1840.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Clin+J+Am+Soc+Nephrol+2017%3B12%3A1831-1840
63
.
Pedrini LA, De Cristofaro V. On-line mixed hemodiafiltration with a feedback for ultrafiltration control: effect on middle-molecule removal. Kidney Int 64:1505-1513, 2003.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Kidney+Int++64%3A1505-1513%2C++2003
64
.
Kanter J, Puerta MC, Pérez-García R, Gómez JM, Jofré R, Rodríguez PB. Hemodiafiltración en línea secuencial (HDF-OL-S): una nueva opción terapéutica [On-line sequential hemodiafiltration (HDF-OL-S): a new therapeutic option]. Nefrologia. 2008;28(4):433-8. Spanish. PMID: 18662152.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+18662152
65
.
Krieter DH, Falkenhain S, Chalabi L, Collins G, Lemke HD, Canaud B. Clinical cross-over comparison of mid-dilution hemodiafiltration using a novel dialyzer concept and post-dilution hemodiafiltration. Kidney Int 67: 349-356, 2005.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Kidney+Int+67%3A+349-356%2C+2005
66
.
de Sequera P, Albalate M, Pérez-García R, Corchete E, Puerta M, Ortega M, Alcázar R, Talaván T, Ruiz-Álvarez MJ. A comparison of the effectiveness of two online haemodiafiltration modalities: mixed versus post-dilution. Nefrologia. 2013 Nov 13;33(6):779-87. English, Spanish. doi: 10.3265/Nefrologia.pre2013.Sep.12223. PMID: 24241365.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+24241365
67
.
Pérez-García R. On-line haemodiafiltration after the ESHOL study. Nefrologia. 2014;34(2):139-44. English, Spanish. doi: 10.3265/Nefrologia.pre2014.Feb.12472. PMID: 24658188.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+24658188
68
.
Albalate Ramón M, Pérez García R, de Sequera Ortiz P, Alcázar Arroyo R, Corchete Prats E, Puerta Carretero M, Ortega Díaz M, Mosse A. Clinical application of Ultracontrol®: infusion volume and use with different dialyzers. Nefrologia. 2011;31(6):683-9.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2011%3B31%286%29%3A683-9
69
.
F. Maduell y cols. Sistema CorDiax-Autosub-Plus FMC. Hosp Clinic Barcelona. Nefrologia. 2014 Sep 26; 34(5): 599-604.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2014+Sep+26%3B+34%285%29%3A+599-604
70
.
Thajudeen B, Issa D, Roy-Chaudhury P. Advances in hemodialysis therapy. Fac Rev. 2023 May 16;12:12. doi: 10.12703/r/12-12. PMID: 37284495; PMCID: PMC10241346.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+37284495%3B+PMCID%3A+PMC10241346
71
.
Shamy OE, Sloand JA. Automation and innovation in home hemodialysis machines. Curr Opin Nephrol Hypertens. 2025 Jan 1;34(1):90-94. doi: 10.1097/MNH.0000000000001033. Epub 2024 Oct 29. PMID: 39470227.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+39470227
72
.
Zasuwa GA, Yee J, Passalacqua KD, Frinak S. Remote Monitoring of Sustained Low-Efficiency Dialysis (SLED) Machines in Intensive Care Unit. Kidney Med. 2022 Mar 18;4(5):100452. doi: 10.1016/j.xkme.2022.100452. PMID: 35518838; PMCID: PMC9065420.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+35518838%3B+PMCID%3A+PMC9065420
73
.
Inoue H, Oya M, Aizawa M, Wagatsuma K, Kamimae M, Kashiwagi Y, Ishii M, Wakabayashi H, Fujii T, Suzuki S, Hattori N, Tatsumoto N, Kawakami E, Asanuma K. Predicting dry weight change in Hemodialysis patients using machine learning. BMC Nephrol. 2023 Jun 29;24(1):196. doi: 10.1186/s12882-023-03248-5. PMID: 37386392; PMCID: PMC10308746.
http://www.ncbi.nlm.nih.gov/pubmed/?term=PMID%3A+37386392%3B+PMCID%3A+PMC10308746
74
.
de Francisco ALM, ARTIFICIAL: La Nueva Inteligencia y su Aplicación en Nefrología. En: Lorenzo V., López Gómez JM (Eds). Nefrología al día. ISSN: 2659-2606. Disponible en: https://www.nefrologiaaldia.org/609.
http://www.ncbi.nlm.nih.gov/pubmed/?term=org%2F609