Síndrome de Horner, dolor cervical y trasplante renal
INTRODUCCIÓN
La inmunosupresión en los trasplantes de órgano sólido es necesaria para evitar los eventos de rechazo, pero no está exenta de riesgos. Qué hacer con la inmunosupresión en pacientes con complicaciones infecciosas de riesgo vital sigue siendo, hoy por hoy, motivo de estudio pues no hay trabajos que abalen el manejo más adecuado.
El síndrome de Lemierre es una complicación infrecuente de las infecciones que afectan a cabeza y cuello. Cuando además asocian un síndrome de Horner con dolor cervical o facial, se requiere descartar de forma rápida y dirigida un aneurisma o disección carotídea, una condición todavía más rara, pero con una mortalidad sin tratamiento muy elevada dada la fragilidad de la pared vascular y el alto riesgo de ruptura que presentan. Al igual que con la inmunosupresión, no hay grandes series que indiquen el manejo más adecuado de estas complicaciones, limitándose la bibliografía disponible a series de casos (1).
A continuación, presentamos a un paciente trasplantado renal con desarrollo de un síndrome de Lemierre y un pseudoaneurisma de arteria carótida interna secundarios a un absceso periamigdalino, que se presentó inicialmente como dolor cervical, fiebre y un síndrome de Horner.
EXPOSICIÓN DEL CASO:
Varón de 69 años, portador de un segundo trasplante renal desde 2002 con buena función del injerto y creatinina basal de 0,9 mg/dl, inmunosuprimido hasta el momento actual con triple terapia estándar: Prednisona, Tacrolimus (FK) y Micofenolato. Además, antecedentes de cardiopatía isquémica revascularizada en 2009.
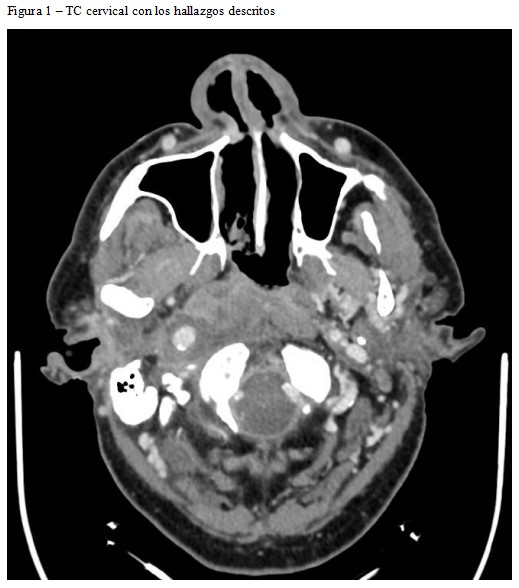
El paciente ingresa por cuadro de desorientación, alteración del habla y cervicalgia de 4-5 días de evolución. A la exploración física, destaca un síndrome febril con miosis y ptosis del ojo derecho sin otras alteraciones en el examen neurológico, y un abombamiento de la amígdala derecha que provoca desplazamiento contralateral de la úvula. Analíticamente muestra marcada elevación de reactantes de fase aguda por lo que, con la sospecha de una infección periamigdalina con síndrome de Horner asociado, se realiza una tomografía computarizada (TC) cervical urgente (Figura 1). Los hallazgos son de un absceso periamigdalino con edema de partes blandas que hace efecto masa sobre la vía aérea, asociando un defecto de repleción de la vena yugular derecha y una dilatación aneurismática de la arteria carótida interna (ACI) ipsilateral a nivel de la base del cráneo. Se inicia tratamiento empírico con Meropenem y Linezolid, y se cursa ingreso en Nefrología con seguimiento conjunto por Infecciosas, Otorrinolaringología y Neurorradiología.
En los hemocultivos extraídos crece un S. pyogenes, por lo que se pudo desescalar la antibioterapia a Amoxicilina a los pocos días de ingreso. Se realizaron dos intentos de punción del absceso periamigdalino, siendo ambos infructuosos.
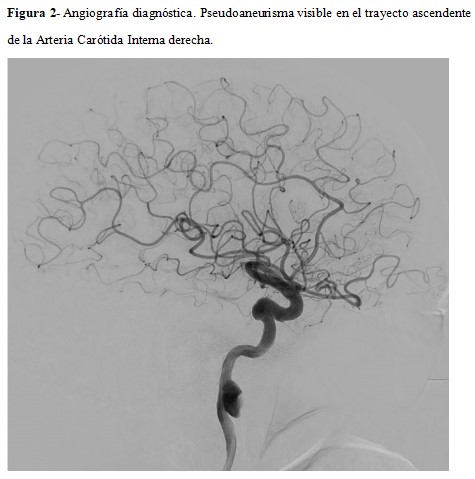
A los dos días, se decidió realizar de una arteriografía en la que se evidencia el pseudoaneurisma en la pared anterior de la ACI derecha distal, adyacente al foramen carotídeo de tamaño 20x15x10 mm con asimetría del drenaje yugular interno ipsilateral en relación con la trombosis séptica conocida (Figura 2), compatible con un síndrome de Lemierre.
En el seguimiento posterior, el paciente desarrolló lesiones herpéticas con distribución metamérica en el ala nasal derecha y afectación del paladar superior ipsilateral, obteniendo un exudado positivo para Virus Herpes Simplex (VHS) tipo 1 por lo que recibió tratamiento con Valaciclovir. Pese al tratamiento antibiótico, presentó una sobreinfección bacteriana de las lesiones con crecimiento de Klebsiella aerogenes productora de AmpC, que motivaron el cambio de antibioterapia a Ertapenem.
Como complicación añadida, el paciente sufrió un episodio de hemorragia digestiva alta (HDA) por úlceras duodenales de estrés con anemización de tres puntos sin inestabilidad hemodinámica, que requirieron tratamiento endoscópico. Sobre las muestras de las úlceras, no pudo demostrarse la presencia de citomegalovirus (CMV) o VHS.
Con el tratamiento instaurado, se realizó un seguimiento con TC cervical objetivándose una disminución de la inflamación y el edema parafaríngeo, pero con un crecimiento progresivo del pseudoaneurisma y persistencia de la trombosis yugular. Además, desarrolló una colección dependiente de la articulación esternoclavicular izquierda sugerente de artritis séptica.
Con las múltiples complicaciones infecciosas presentes y teniendo en cuenta que la determinación de anticuerpos HLA fue negativa, y que las poblaciones linfocitarias, los niveles de inmunoglobulinas y de complemento eran normales, se decidió reducir la inmunoterapia al máximo manteniendo monoterapia con Tacrolimus (con objetivo de niveles valle en 3-4 ng/ml).
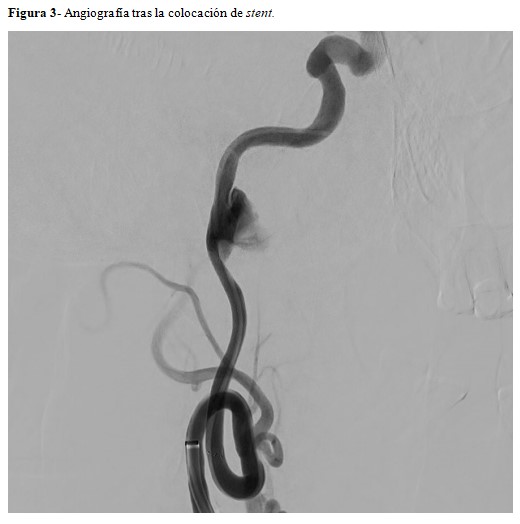
La decisión de tratamiento sobre el pseudoaneurisma estuvo limitada por el riesgo a introducir un material extraño en una región sobreinfectada. Sin embargo, con el crecimiento descrito y habiendo completado dos semanas de antibiótico, se realizó tratamiento endovascular del pseudoaneurisma mediante colocación de una endoprótesis de tipo “flow-diverter”. Este tipo de stent redirige el flujo sanguíneo principalmente por dentro del mismo de manera que con el tiempo, la sangre que ha quedado remansada se trombosa y hace que el aneurisma quede excluido de la circulación, evitando así un potencial riesgo de sangrado.
El resultado angiográfico fue satisfactorio, con una retención de contraste en las imágenes que indica el buen funcionamiento del stent (Figura 3). Tras más de seis meses de seguimiento, el paciente permanece estable con normofunción del injerto renal y una desaparición progresiva del aneurisma en las pruebas de imagen de control.
COMENTARIOS DEL CASO:
El Síndrome de Lemierre es una complicación atípica de las infecciones orofaríngeas en la que ocurren eventos trombóticos locales con posibilidad de embolismos sépticos, entre otras complicaciones. Aunque las especies de Fusobacterium suelen ser las más frecuentemente aisladas, los microorganismos gram positivos como Staphylococcus spp. y Streptococcus spp. ocupan el segundo puesto (2). Pese a ser una enfermedad ampliamente descrita en los libros de medicina, el manejo general del síndrome y sus complicaciones no está bien establecido. Entre ellas destacan los embolismos asociados a la trombosis venosa, en ocasiones como émbolos sépticos, fundamentalmente a nivel pulmonar e intracraneal, y que ocurren hasta en un 14% de los casos según algunas de las series descritas (2). La anticoagulación en estos casos sigue siendo tema de debate y no está ampliamente recomendada. En nuestro paciente, el uso de anticoagulantes añadidos a la doble antiagregación que iba a precisar por el tratamiento endovascular propuesto hubiese supuesto un riesgo sobreañadido para la HDA acontecida.
Los pseudoaneurismas de carótida interna producidos por fenómenos infecciosos locales son condiciones todavía más raras, pero con una alta mortalidad sin tratamiento. El tratamiento puramente quirúrgico conlleva un alto riesgo, especialmente en la localización tan cercana a la base del cráneo como presentaba nuestro paciente (1). La posibilidad de un tratamiento endovascular con “stent” o embolización con “coils” está limitada por el riesgo que conlleva introducir un material extraño en un área infectada, aunque la literatura al respecto no siempre apoya esta posible complicación. No obstante, dada la escasa experiencia, tendríamos que valorar un posible sesgo de publicación al respecto.
Las infecciones más frecuentes en los pacientes trasplantados de largo tiempo de evolución, suelen ser las neumonías adquiridas en la comunidad, infecciones del tracto urinario, infecciones virales latentes (CMV, VEB…), entre otras (Ver NAD: Infecciones en el trasplante renal) (3). Estas infecciones comunitarias que podrían resultar benignas en la población normal pueden complicarse en los trasplantados por el estado de inmunosupresión que presentan. La debilidad de los diferentes sistemas que integran la inmunidad humana está condicionada por la dosis, la duración y el tipo de inmunosupresión que reciben. De esta forma, en los pacientes trasplantados, la inmunosupresión supone la base de la balanza entre el riesgo de complicaciones infecciosas o tumorales con el riesgo de rechazo. La práctica clínica respecto al manejo de estos fármacos cuando transcurren complicaciones infecciosas graves es muy dispar, y la evidencia científica, escasa (4). Monitorizar los niveles en sangre para evitar la excesiva inmunosupresión, así como la minimización de los fármacos son las estrategias habitualmente utilizadas (Ver NAD: Inmunosupresión en el trasplante renal). Existen trabajos que apoyan la minimización de la inmunusepresión en cuanto a supervivencia del injerto y del paciente, planteando la monoterapia con tacrolimus como tratamiento único (5)(6). Si bien, estos buenos resultados suelen darse en pacientes de bajo riesgo inmunológico de base. Por último, se han propuesto modelos para estratificar el riesgo infeccioso de los receptores de órgano sólido basados en la determinación de varios parámetros clínicos y analíticos que evalúan el estado neto de inmunosupresión (Ver NAD: Infecciones en el trasplante renal) pero su uso no está estandarizado y no se han implementado de forma efectiva en la práctica clínica habitual (7).
Nuestro caso se trataba de un segundo trasplante renal con 22 años de evolución con una adecuada función del injerto. Apoyados por la probable adaptación inmunológica del paciente y el no presentar anticuerpos preformados dirigidos frente al complejo mayor de histocompatibilidad, decidimos disminuir la inmunosupresión al máximo dejando en monoterapia con Tacrolimus.
BIBLIOGRAFÍA:
1. Davidson C, Holihan C, De Oliveira Sillero R, Lee K, Mitchell RB, Shah G. Infectious Pseudoaneurysm of the Internal Carotid Artery in a Child Secondary to Parapharyngeal Abscess. Ear Nose Throat J. 2023 Jan;102(1):NP31–4.
2. Valerio L, Zane F, Sacco C, Granziera S, Nicoletti T, Russo M, et al. Patients with Lemierre syndrome have a high risk of new thromboembolic complications, clinical sequelae and death: an analysis of 712 cases. J Intern Med. 2021 Mar;289(3):325–39.
3. Agrawal A, Ison MG, Danziger-Isakov L. Long-Term Infectious Complications of Kidney Transplantation. Clin J Am Soc Nephrol. 2022 Feb;17(2):286–95.
4. Roberts MB, Fishman JA. Immunosuppressive Agents and Infectious Risk in Transplantation: Managing the ‘Net State of Immunosuppression’. Clin Infect Dis Off Publ Infect Dis Soc Am. 2021 Oct 5;73(7):e1302–17.
5. Sayegh J. Long-term maintenance immunosuppressive regimen with tacrolimus monotherapy. Ann Transplant. 2013;18:368–77.
6. de Weerd AE, Fatly ZA, Boer-Verschragen M, Kal-van Gestel JA, Roelen DL, Dieterich M, et al. Tacrolimus Monotherapy is Safe in Immunologically Low-Risk Kidney Transplant Recipients: A Randomized-Controlled Pilot Study. Transpl Int Off J Eur Soc Organ Transplant. 2022;35:10839.
7. Fernández-Ruiz M, López-Medrano F, Aguado JM. Predictive tools to determine risk of infection in kidney transplant recipients. Expert Rev Anti Infect Ther. 2020 May;18(5):423–41.