Síndrome cardiorrenal: Nuevas herramientas diagnósticas.
Introducción
El síndrome cardiorrenal (SCR) tipo 1 se caracteriza por la disfunción cardíaca aguda que induce disfunción renal aguda. Este deterioro de la función renal puede ser debido a múltiples causas entre los que destacan la activación neurohumoral, las alteraciones hemodinámicas, la congestión venosa y la iatrogenia.
Presentamos el caso de un varón que ingresa por insuficiencia cardíaca y que presenta un empeoramiento progresivo de la función renal, con el consecuente reto diagnóstico y terapéutico que supone, viendo lo que aporta la utilización de nuevas herramientas diagnósticas.
Caso clínico
Varón de 73 años que ingresa en noviembre 2021 en cardiología por insuficiencia cardíaca. Entre sus antecedentes destaca diabetes mellitus tipo 2 con buen control glucémico, cardiopatía isquémica con doble baipás aortocoronario en 2014, estenosis aórtica grave con prótesis biológica en posición mitral, hipertensión arterial y dislipemia. Además, presenta una enfermedad renal crónica (ERC) estadio 3a A2 con creatinina basal en torno a 1,1 mg/dl sin seguimiento por nefrología con atrofia renal izquierda en pruebas de imagen. Su tratamiento habitual era semaglutida 1 0,25 mg semanal, metformina 850 mg/12h y furosemida 40 mg en desayuno y comida.
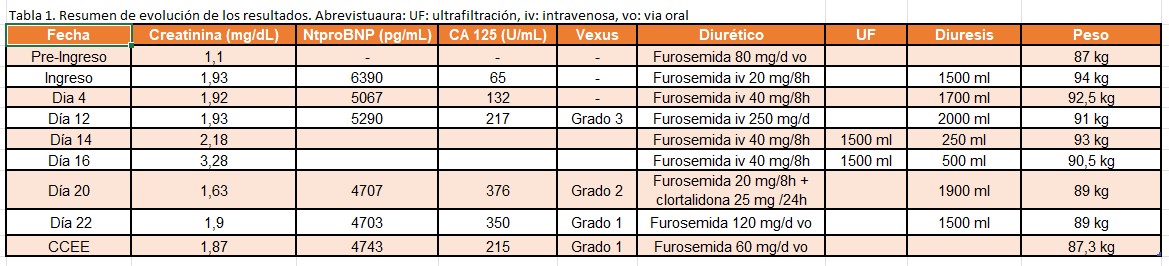
Ingresa con apoyo de la unidad cardiorrenal, por insuficiencia cardíaca y agudización de su enfermedad renal (Tabla 1) iniciándose tratamiento diurético intravenoso con discreta mejoría clínica y leve deterioro de la función renal. Se inicia también un iSGLT2. Se va aumentando el tratamiento diurético en los días siguientes, pero a pesar de lograr diuresis adecuadas y discreta pérdida de peso, el duodécimo día persiste disneico sin que su función renal alcance cifras basales y con un aumento de algunos de los marcadores bioquímicos de congestión venosa. Se incrementa entonces más el tratamiento diurético y se realiza ecografía a pie de cama (POCUS) con valoración mediante escala VEXUS (VExUS Ultrasound Score) para optimizar el tratamiento diurético. Ver evolución en (Tabla 1)
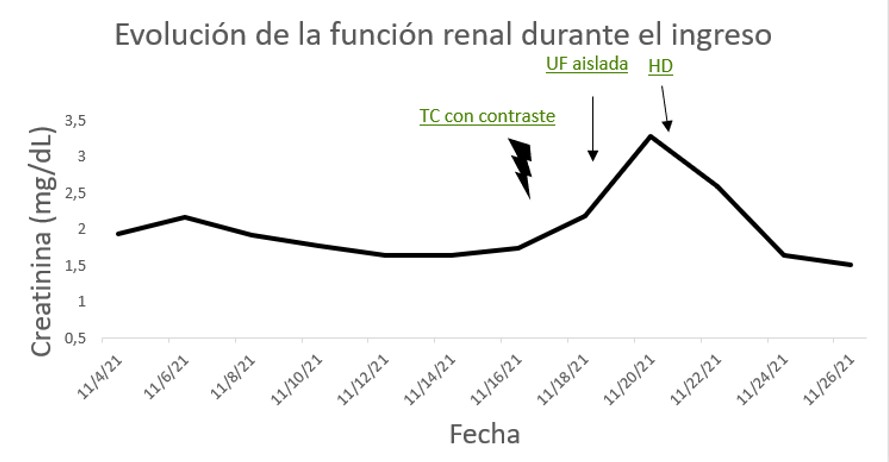
Pese a los cambios, persiste la necesidad de oxigenoterapia, por lo que se realiza un angio-TC de arterias pulmonares urgente que no evidencia tromboembolismo pulmonar y que muestra persistencia de datos de hipervolemia. En los días posteriores, se produce una rápida disminución de la diuresis, en probable relación con nefropatía asociada al contraste, junto con un incremento de los marcadores congestivos, que requiere iniciar hemodiálisis (HD). (Figura 1)
Se observa después una recuperación del ritmo de diuresis persistiendo todavía la sobrecarga de volumen con necesidad de oxígeno y de perfusión de furosemida. Se intenta la retirada paulatina de tratamiento diurético, con nuevo empeoramiento respiratorio e incremento de congestión valorado mediante POCUS, por lo que se incrementa de nuevo la furosemida con asociación de clortalidona. Finalmente, se consigue retirada de diuréticos endovenosos y se cita en nuestra unidad cardiorrenal para seguimiento donde clínicamente no existían signos o síntomas de insuficiencia cardiaca.
En la (Tabla 1) (Figura 1) se recogen los datos clínicos y analíticos más relevantes.
Comentarios:
El SCR se define por trastornos del corazón y riñón en los que la disfunción aguda o crónica en un órgano induce la disfunción aguda o crónica del otro. Se realizó una clasificación en 5 subtipos (ver NAD: Síndrome Cardiorrenal) y de ellos, el tipo 1, caracterizado por disfunción cardíaca que origina disfunción renal, es el más frecuente.
En nuestro caso, en el momento del ingreso ya existía un deterioro agudo de la función renal clasificado como KDIGO 2 (ver NAD: Insuficiencia renal aguda), que mejoró sólo parcialmente durante los primeros días. En este momento, se había añadido al tratamiento un inhibidor de iSGLT2, por sus beneficios cardiovasculares incluso en la fase aguda de la insuficiencia cardíaca (1). De hecho, ante el deterioro de la función renal inicial, se valoró la existencia del fenómeno de “permissive AKI” en relación con los efectos hemodinámicos iniciales de estos fármacos (2), aunque la impresión diagnóstica era que se debía a la persistencia de nefropatía congestiva, cuya solución es intensificar el tratamiento diurético, incluyendo la estrategia del bloque secuencial, para alcanzar cuanto antes la euvolemia (3).
Dentro de los parámetros bioquímicos que se utilizan para la valoración de la congestión nos encontramos el propéptido natriurético cerebral N-terminal (NtproBNP) y el antígeno carbohidrato 125 (CA 125) El NtproBNP es un indicador de hipertrofia ventricular y no valora de forma adecuada la congestión en pacientes con insuficiencia renal (4). Por lo que respecta al CA 125, en los últimos años ha destacado por ser un marcador de congestión adecuado de forma aislada, incluso sin una clínica compatible que además no se modifica en pacientes con ERC, por lo que parece una herramienta interesante en este grupo (5).
Actualmente, también se ha incorporado como una herramienta fundamental la ecografía a pie de cama o POCUS para la valoración de la congestión en los pacientes cardiorrenales. La escala VEXUS (6) nos ayuda a establecer el grado de congestión y a optimizar el tratamiento diurético si presentan un empeoramiento de la función renal durante el tratamiento de la insuficiencia cardíaca. En el caso de nuestro paciente, la valoración mediante POCUS, permitió junto a la valoración conjunta clínica y analítica, un tratamiento diurético dirigido. Esta medición se realiza mediante sonda de ecografía convexa por parte de nefrología, complementándola en caso de ser necesario con la sonda de ecocardiografía por parte de los cardiólogos.
La nefropatía asociada al contraste en el contexto de insuficiencia cardíaca se produce sobre todo en los pacientes sometidos a cateterismo coronario percutáneo, y se relaciona con un incremento de días de hospitalización y mortalidad. Es importante en estos pacientes con SCR, la limitación del uso de contrastes y la prevención de la aparición de esta entidad que añade otro factor al daño renal. (ver NAD: Lesión Renal Aguda poscontraste yodado)
Tras la resolución del episodio agudo de insuficiencia renal generado por el contraste, se encontraba en un punto muy similar al del ingreso, de nuevo con insuficiencia cardíaca descompensada e insuficiencia renal, por lo que, de nuevo, fue importante el ajuste dirigido del tratamiento diurético de cara posibilitar el alta usando todas las herramientas que teníamos en nuestra mano.
Para finalizar comentar que la aplicación conjunta de los diferentes marcadores resulta importante también en la consulta cardiorrenal, donde se revisó tras el ingreso, ya que a pesar de deterioro de la función renal y NtproBNP elevado, el CA 125 y el POCUS, nos indican que probablemente no requiera tanto diurético y que en este momento el deterioro renal puede deberse a tratamiento excesivo.
Concluimos con 3 mensajes para llevar a casa:
1) En un paciente con SCR que ingresa por insuficiencia cardiaca, el deterioro de función renal puede ser inicialmente secundario a nefropatía congestiva y precisar tratamiento diurético intensivo.
2) El objetivo en la insuficiencia cardiaca es conseguir la euvolemia. Para ello hay que realizar una valoración global del paciente más allá de la diuresis y/o la clínica que pueden ofrecer resultados engañosos, integrando según nuestros medios, otras medidas diagnósticas bioquímicas o POCUS.
3) Finalmente, durante el ingreso hospitalario es importante la prevención, evitando el uso de nefrotóxicos, y el diagnóstico precoz y tratamiento del fracaso renal en caso que se produzca.
Bibliografía:
1. Voors AA, Angermann CE, Teerlink JR, Collins SP, Kosiborod M, Biegus J, et al. The SGLT2 inhibitor empagliflozin in patients hospitalized for acute heart failure: a multinational randomized trial. Nat Med. 2022;28(3):568-74.
2. Parikh CR, Coca SG. «Permissive AKI» with treatment of heart failure. Kidney Int. 2019;96(5):1066-8.
3. Husain-Syed F, Gröne H-J, Assmus B, Bauer P, Gall H, Seeger W, et al. Congestive nephropathy: a neglected entity? Proposal for diagnostic criteria and future perspectives. ESC Heart Fail. febrero de 2021;8(1):183-203.
4. Wang AY-M, Lai K-N. Use of Cardiac Biomarkers in End-Stage Renal Disease. JASN. 2008;19(9):1643-52.
5.. Núñez J, Bayés-GA, Revuelta -López Elena, ter MJM, Miñana G, Barallat J, et al. Clinical Role of CA125 in Worsening Heart Failure. JACC: Heart Failure. 2020;8(5):386-97.
6.. Argaiz ER. VExUS Nexus: Bedside Assessment of Venous Congestion. Adv Chronic Kidney Dis. 2021;28(3):252-61.