Enfermedad renal por litiasis asociada al déficit de adenina fosforribosiltransferasa
INTRODUCCIÓN
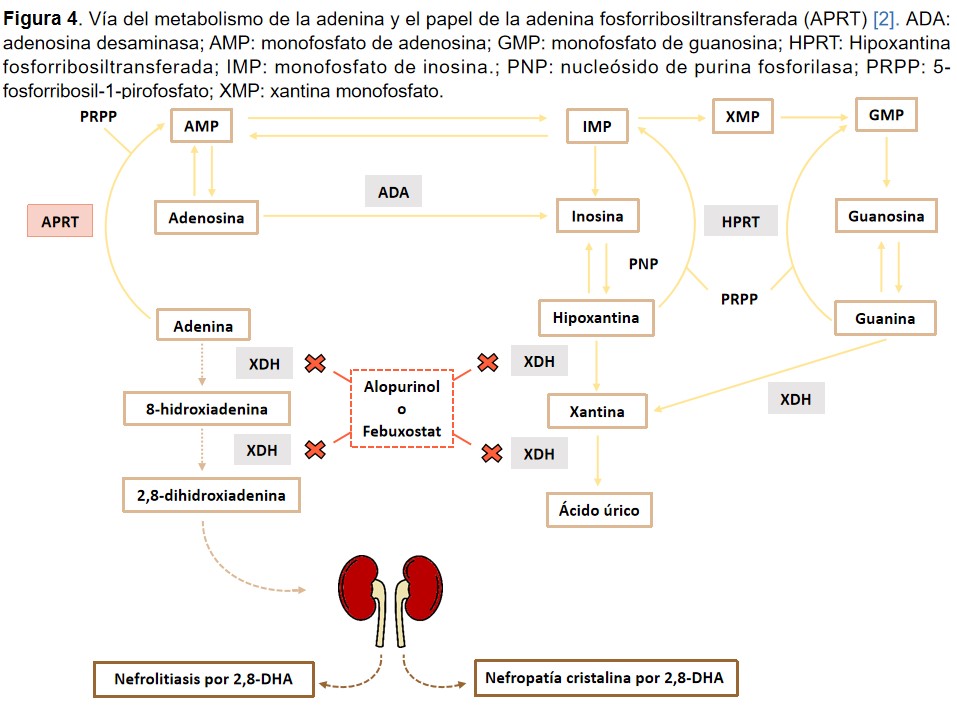
La deficiencia de adenina fosforribosiltransferasa (APRT) es una enfermedad genética rara de herencia autosómica recesiva [1]. Su prevalencia se estima en 1/ 50.000 - 1/ 100.000 en individuos caucásicos, 1/ 27.000 en japoneses y >1/15.000 en islandeses. La enzima APRT cataliza la síntesis de adenosinmonofosfato a partir de adenina y 5-fosforribosil-1-pirofosfato en la vía de recuperación de las purinas. En el déficit de APRT, la adenina se cataboliza oxidativamente a 8-hidroxiadenina y al producto final 2,8-dihidroxiadenina (DHA) que es extremadamente insoluble en medio acuoso y causa cristaluria y litiasis (Figura 4) [2]. El depósito de cristales en el parénquima renal es el inicio de la enfermedad renal en este tipo de nefropatía, que puede recidivar en el injerto renal, conduciendo a su pérdida hasta en el 25% de los casos [1][2].
A continuación, presentamos una deficiencia de APRT que debuta como un fallo renal agudo pero que permanece como enfermedad renal crónica (ERC) y con un manejo difícil debido a la complejidad del diagnóstico.
CASO CLÍNICO
Paciente de 51 años con antecedentes de obesidad y diabetes mellitus tipo 2 conocida desde 2016 sin complicaciones crónicas, sin litiasis renal previa ni antecedentes familiares relevantes. En noviembre de 2018, fue derivado al hospital por lesión renal aguda objetivada en un análisis de control (creatinina 6.09 mg/dL que en febrero de 2018 era 0.84 mg/dL). Hasta el momento de la consulta, estaba asintomático y tampoco había antecedentes de ingesta de fármacos nefrotóxicos.
A su llegada a urgencias se encontraba hemodinámicamente estable, afebril, con diuresis conservada y sin alteraciones en la exploración física.
En los análisis: Hb 10.9 gr/dL, creatinina 6.36 mg/dL, urea 23.6 mmol/L, FG estimado <10 mL/min, pH 7.27, bicarbonato 20 mmol/L; sedimento urinario sin hematuria, leucocituria, ni proteinuria, fracción de excreción de sodio 3,7%.
Radiografía de abdomen normal.
Ecografía renal: Riñón derecho 12.8 cm e izquierdo 11.2 cm con aumento global y bilateral de la ecogenicidad cortical y disminución de la diferenciación corticomedular. Presencia de litiasis de 12 mm localizada en el tercio proximal del uréter izquierdo que condicionaba una ureterohidronefrosis ipsilateral y múltiples litiasis en el parénquima renal de dicho riñón. No se observaron litiasis ni dilatación de la vía urinaria derecha.
Se colocó un catéter doble J. En control analítico posterior, se objetivó una discreta mejoría de la función renal con creatinina de 5.93 mg/dL y equilibrio ácidobase normalizado.
Se orientó como un fallo renal agudo en contexto de uropatía obstructiva, en paciente con probable nefropatía crónica de etiología incierta. Se amplió estudio: autoinmunidad negativa, proteinograma normal y serologías víricas negativas (VIH, VHC, VHB).
En los meses posteriores, durante el seguimiento, continúo la progresión a ERC hasta creatinina 11.21 mg/dL y se preparó para terapia renal sustitutiva.
En marzo de 2019, consulta en urgencias por sintomatología urémica. Destacaba en los análisis: Hb 7.2 gr/dL, creatinina 15.7 mg/dL y FG 3 ml/min, sin presentar criterios de diálisis urgente. Se realizó nueva ecografía renal que no presentó cambios con respecto a ecografía previa. Se recambió el catéter doble J sin que se observase mejoría de la función renal (creatinina 15.62 mg/dl). Dada la mala evolución clínica, se decidió iniciar hemodiálisis.
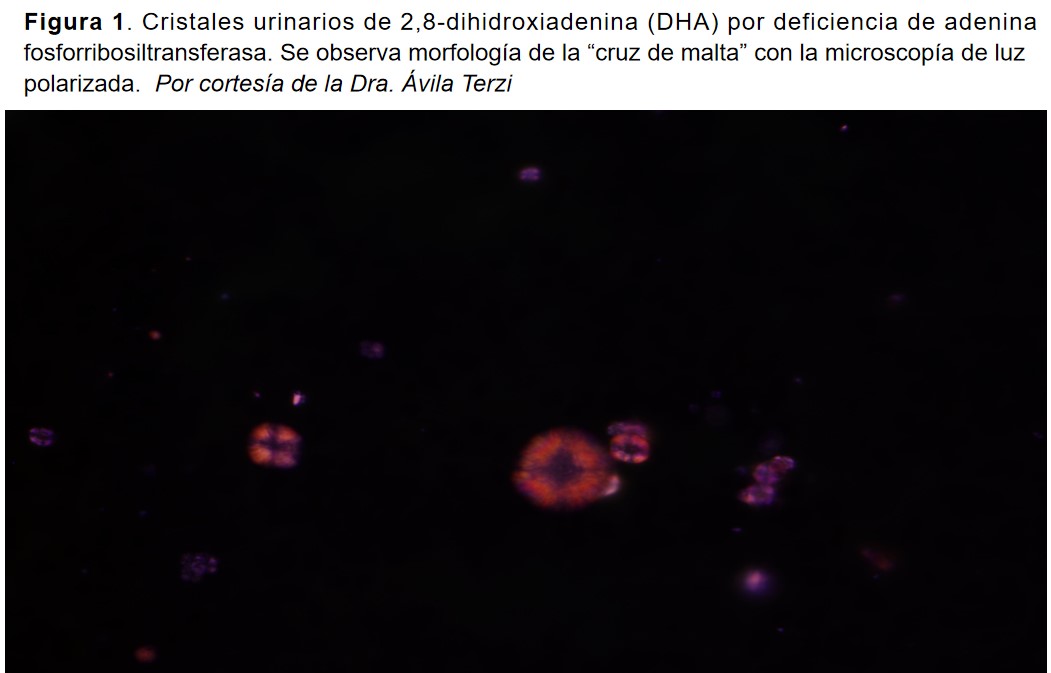
Por la forma de progresión, se insistió en el estudio etiológico. Se realizó orina de 24h con proteinuria 1061 mg y albuminuria 38 mg/L, uricosuria, citraturia y oxaluria normales. Citología urinaria: cristales urinarios compatibles de 2,8-DHA (Figura 1).
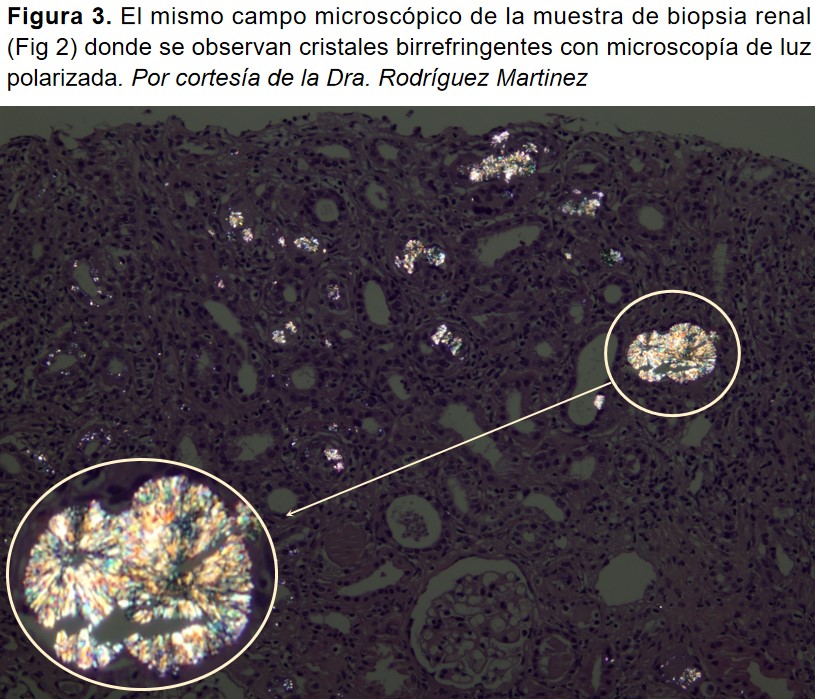
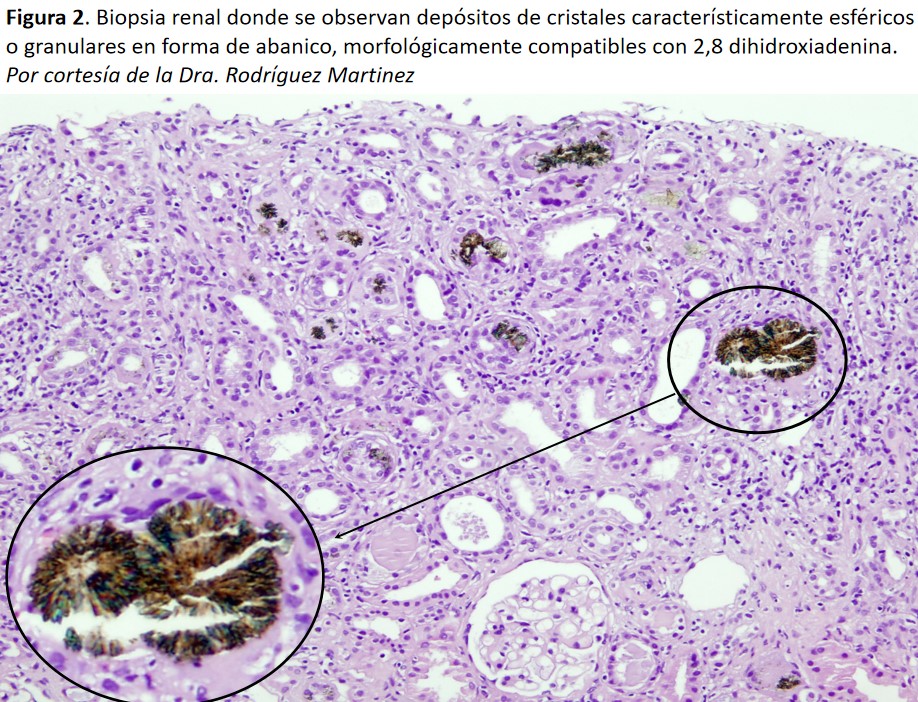
Se realizó biopsia renal donde se observaron abundantes cristales en las luces tubulares, en el epitelio tubular y en el intersticio comprometiendo a más del 50% de la corteza renal representada, evidenciando nefritis intersticial crónica morfológicamente compatible con depósito de 2,8 dihidroxiadenina. (Figura 2) y (Figura 3).
Posteriormente, se derivó a la consulta genética donde se identificaron dos mutaciones (una variante patogénica c.286_287 deI AC por deleción y una variante de significado incierto c.428T>C p.Leu 143Pro en el gen APRT). Se diagnosticó entonces de ERC secundaria a nefropatía por 2,8-DHA, iniciándose tratamiento con alopurinol y manteniéndose en programa de hemodiálisis crónica hasta la actualidad. Se ha incluido recientemente en lista de espera de trasplante renal.
COMENTARIOS
Presentamos un caso de disfunción renal rápida, progresiva y grave, asociada al depósito de cristales, la cual es una enfermedad hereditaria rara con una edad de inicio variable, que se diagnosticó mediante biopsia renal y donde el estudio genético evidenció una mutación que originaba un déficit de APRT.
La enfermedad puede presentarse de dos formas, que pueden ocurrir simultáneamente o por separado: urolitiasis y nefropatía cristalina. Aunque la deficiencia de APRT ocurre en todas las células, no se ha reportado ningún síntoma extrarrenal en los individuos afectados. Los cristales de DHA pueden precipitar en los túbulos renales y el intersticio y afectar gravemente la función renal. Se ha propuesto el término “nefropatía por DHA” para la nefropatía cristalina secundaria a la precipitación de DHA. Ésta puede presentarse como una enfermedad aguda que conduce a insuficiencia renal en unos pocos días o semanas o, con mayor frecuencia, desarrollarse insidiosamente y causar disminución progresiva de la función renal durante un período de varios años. En nuestro caso, se constataron depósitos tubulares e intersticiales de cristales en la biopsia renal, por lo que se cree que ésta es la causa del deterioro de la función renal. [2].
El diagnóstico de la deficiencia de APRT se basa en la identificación de DHA, ya sea mediante el examen de cristales en la orina o mediante el análisis de los cálculos. Generalmente, son cristales radiolúcidos que tienen poca especificidad en el estudio radiológico (ver NAD: Litiasis renal). La cristaluria revela cristales de DHA redondos y marrones que son patognomónicos. Son de tamaño pequeño y mediano y muestran una morfología en “cruz de malta” central cuando se ve por microscopía de luz polarizada (Figura 1). El análisis de los cálculos realizado con una combinación de microscopio estereoscópico y espectroscopia infrarroja permite la identificación de DHA constituidos principalmente de purinas (ver NAD: Litiasis renal, tabla 1).
En la biopsia realizada, se evidenciaron depósitos de cristales esféricos en forma de abanico con una coloración parduzco-rojiza, morfológicamente compatibles con cristales de DHA (Figura 2). La combinación de la microscopía de polarización y de la microscopía transformada de Fourier es un método fiable para caracterizar los cristales en la biopsia renal. (Figura 3).
La determinación de la alteración genotípica establece un diagnóstico definitivo evidenciando las mutaciones en ambos alelos del gen APRT [1]. En el presente caso, el estudio genético identificó 2 mutaciones del gen APRT una variante patogénica c.286_287 deI AC por deleción y una variante de significado incierto c.428T >C p.Leu 143Pro en el gen APRT. Esto da lugar a una enzima anormalmente corta y no funcional.
Se recomienda la detección de la deficiencia de APRT en todos los casos de urolitiasis en niños, casos recurrentes (especialmente si son radiotransparentes) y pacientes con disfunción renal de causa incierta sea aguda o crónica (incluidos aquellos con ERCT y receptores de trasplante renal).
En el caso presentado, inicialmente se orientó el cuadro como un fallo renal agudo con componente obstructivo, pero llamó la atención el importante deterioro de la función renal tratándose de un paciente con función renal previa normal y con obstrucción unilateral, por lo cual, se amplió estudio realizándose una biopsia renal por sospecha de posible nefropatía crónica.
El tratamiento de la deficiencia de APRT se realiza con alopurinol o febuxostat, que actúan bloqueando la xantina deshidrogenasa (Figura 4). Esto permite estabilizar o mejorar la función renal y prevenir la recurrencia después del trasplante renal. En caso de trasplante renal, y en ausencia de tratamiento profiláctico, dicha nefropatía puede reaparecer en el aloinjerto renal, lo que lleva a la pérdida del mismo en más del 25% de los casos. Actualmente, se está estudiando comparativamente ambos tratamientos, evidenciando hasta el momento una mayor reducción en la excreción urinaria de DHA con febuxostat, aunque aún no se dispone de estudios de equivalencia de dosis [3].
Como conclusión, este caso presenta varios aspectos docentes. El primero, de carácter general, radica en la importancia de buscar la causa de ERC siempre que se pueda, ya que nos podemos encontrar con causas tratables y por tanto de ERC prevenible. El segundo es recordar que el déficit de APRT existe. Hay que considerar esta patología en el diagnóstico diferencial de cálculos renales radiolúcidos y ERC inexplicable, litiasis de repetición que comienzan en la infancia y en casos de disfunción del injerto renal de etiología poco clara. La terapia farmacológica oportuna retrasa la progresión de la enfermedad, incluso en individuos gravemente afectados, por lo cual, es importante realizar un diagnóstico precoz.
BIBLIOGRAFÍA
1.- George S, Rushaidan S. 12,8-Dihydroxyadenine Nephropathy Identified as Cause of End-Stage Renal Disease After Renal Transplant. Experimental and Clinical Transplantation 2017; 5: 574-577.
2.- Bollée G et al. Adenine phosphoribosyltransferase deficiency. Clin J Am Soc Nephrol. 2012 Sep;7(9):1521-7.
3.- Edvardsson V, Runolfsdottir H. Comparison of the effect of allopurinol and febuxostat on urinary 2,8-dihydroxyadenine excretion in patients with APRT deficiency: a clinical trial.Eur J Intern Med. 2018 February ; 48: 75–79.