Glomeruloesclerosis focal y segmentaria asociada a inyección intravítrea de anti-VEGF (aflibercept)
Tercer premio 16º Encuentro Nacional de residentes de Nefrología. Cocentaina. Alicante. Organizado por la Sociedad Española de Nefrología
INTRODUCCIÓN
Los inhibidores del factor de crecimiento del endotelio vascular (VEGF) han sido ampliamente usados en las últimas décadas como parte del arsenal de tratamiento para diferentes patologías oncológicas. Desde entonces se han descrito numerosos efectos adversos entre los que destaca la hipertensión o la microangiopatía trombótica [1] [2] [4].
El VEGF es producido por los podocitos glomerulares, funcionando como uno de los principales estabilizadores de la barrera podocitaria, por lo que no sorprende que su inhibición se haya asociado a proteinuria, deterioro de función renal e incluso glomerulopatías [1] [2] [3] [4].
Además de su aplicación en el campo de la Oncología, cada vez es más creciente el uso de esta familia de fármacos en forma de inyecciones intravítreas para inhibir la angiogénesis en patologías oftalmológicas proliferativas como la retinopatía diabética o la degeneración macular asociada a la edad (DMAE) [1] [2] [3].
Presentamos el caso de un hombre de 85 años que posterior a la inyección intravítrea de anti-VEGF desarrolla un síndrome nefrótico.
EXPOSICIÓN DEL CASO
Varón de 85 años con antecedentes a destacar de cáncer de próstata en remisión y DMAE que acude a Urgencias por edemas, disnea progresiva e hipertensión de nueva aparición con mal control acompañado de ganancia ponderal de 7kg en 2 meses y la presencia de orinas espumosas. Niega otra sintomatología o introducción de nuevos fármacos salvo inicio reciente de inyecciones intraoculares de aflibercept (anti-VEGF).
En la exploración física destaca anasarca, cifras elevadas de presión arterial (178/99mmHg), necesidad de oxigenoterapia con gafas nasales para alcanzar adecuadas saturaciones y crepitantes húmedos en bases pulmonares.
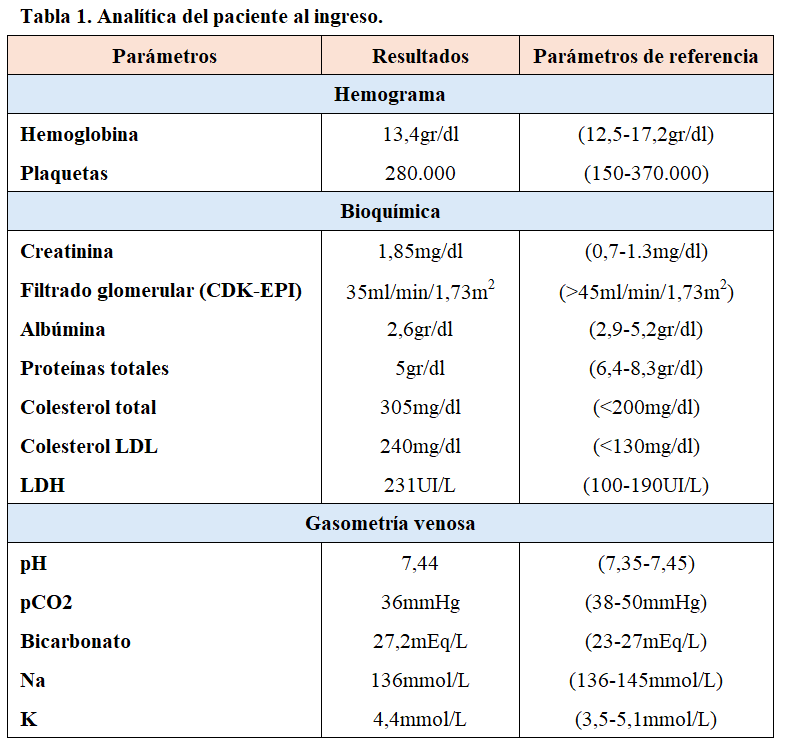
Las pruebas complementarias se muestran en la (Tabla 1), destacando la presencia de fracaso renal agudo hasta creatinina de 1,85 mg/dl y síndrome nefrótico (proteinuria 9 gr/24h, albúmina 2,6 gr/dl), sin microhematuria asociada.
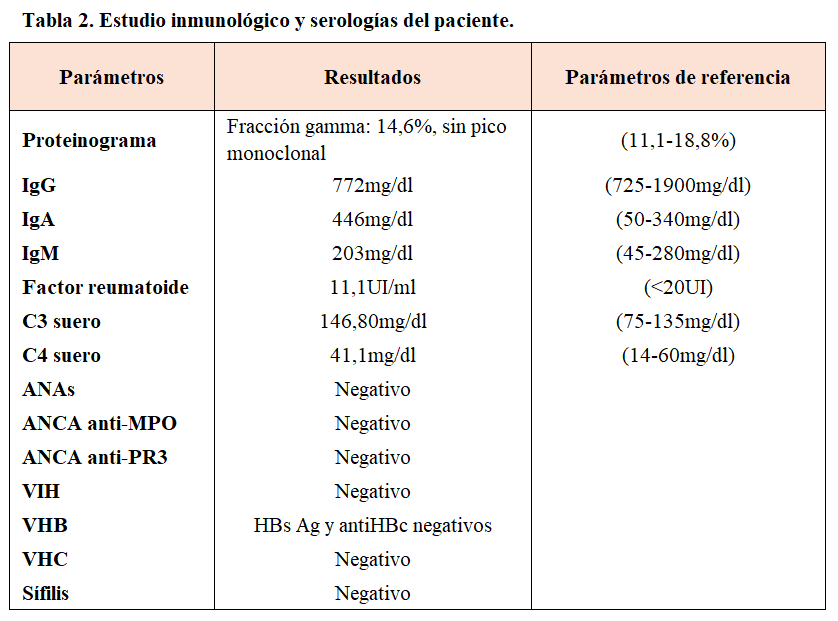
Ante la presencia de síndrome nefrótico completo ingresa en el servicio de Nefrología, donde se inicia tratamiento diurético y se solicita estudio inmunológico y serológico que resulta negativo (Tabla 2).
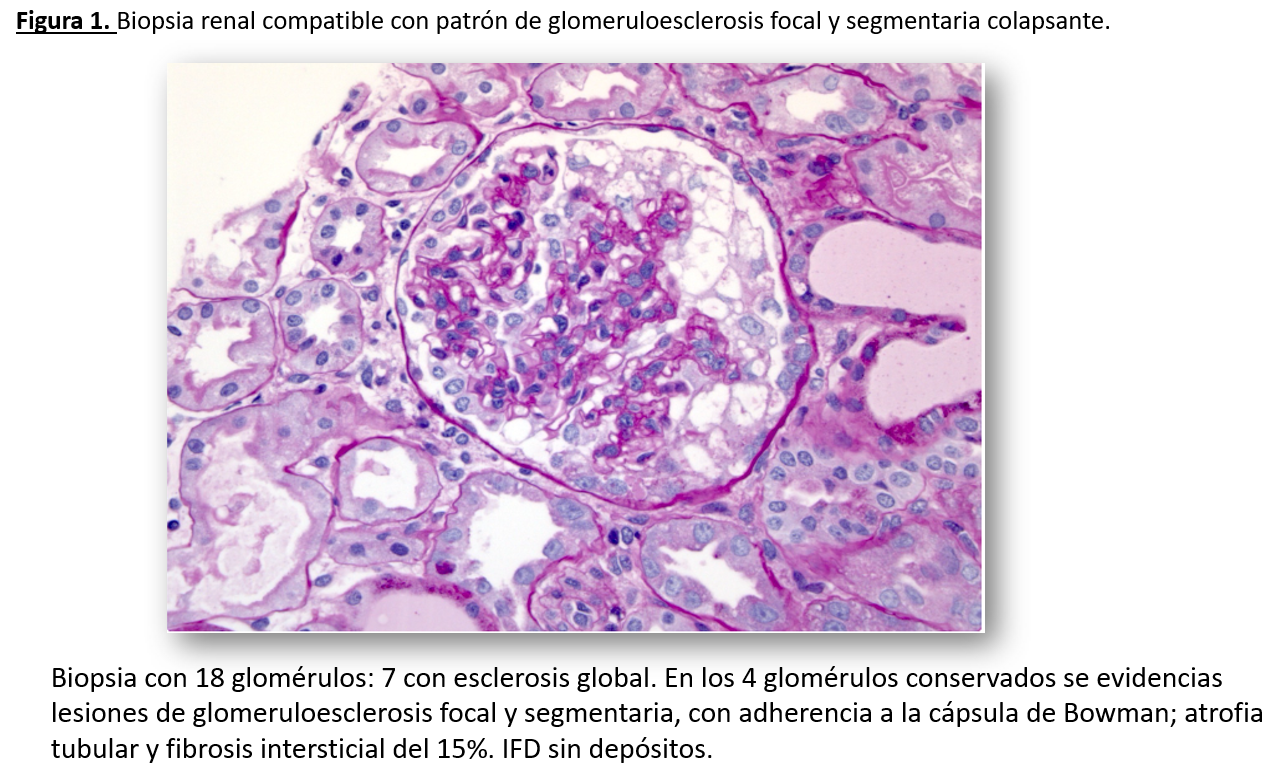
Se realiza una biopsia renal que objetiva glomeruloesclerosis focal y segmentaria colapsante (Figura 1), por lo que ante la sospecha de podocitopatía de curso agresivo asociada al tratamiento intravítreo de inicio reciente con aflibercept, se procede al inicio de terapia con esteroides (prednisona a 0,5mg/kg/día) con objetivo de estabilizar el podocito y a la suspensión del tratamiento oftalmológico.
Tras 1 mes de suspensión del tratamiento intravítreo e inicio de esteroides a bajas dosis, se objetiva mejoría del síndrome nefrótico con función renal normal. Junto con el servicio de Oftalmología se valoran alternativas de tratamiento para la DMAE, decidiendo de forma conjunta la suspensión de aflibercept y el inicio de ranibizumab ante las características del paciente (alto riesgo de ceguera completa por DMAE bilateral asociada a pérdida de visión total en ojo izquierdo).
Finalmente se mantiene tratamiento esteroideo con reducción progresiva (dosis menores a 2,5mg/día a los 3 meses y suspensión definitiva a los 6 meses) simultáneo al inicio de ranibizumab, consiguiendo la remisión completa del cuadro a los 3 meses sin presentar nuevas recidivas hasta el momento actual.
COMENTARIOS
El factor de crecimiento del endotelio vascular (VEGF) se ha postulado como uno de los puntos determinantes en la supervivencia del podocito, controlando la estabilidad del citoesqueleto por medio de diferentes vías donde destaca su interacción con la nefrina [2] [4]. Su activación está estrechamente ligada con la vía de activación del Receptor del Factor de Crecimiento Epidérmico (EGFR ), compartiendo ambos mediadores similares.
Media la regulación del óxido nítrico y con ello la vasodilatación [2] [4], además de inhibir el diacilglicerol, siendo con ello un mecanismo defensivo contra la agregación plaquetaria y en último término contra la microangiopatía trombótica [2].
Con el uso de anti-VEGF sistémico como terapia oncológica la aparición de hipertensión y proteinuria es posible y suele ser dosis dependiente [4] [2]. Se han descrito numerosos casos de glomerulopatías (enfermedad por cambios mínimos, glomeruloesclerosis focal y segmentaria…) y microangiopatías trombóticas tras su inicio [3]. En relación a las administraciones intravítreas, con la aprobación del fármaco inicialmente no se consideró importante su absorción sistémica, sin embargo, estudios de farmacocinética posteriores han demostrado una absorción suficiente como para inhibir los niveles intravasculares del VEGF más del 50% (IC50), con casos publicados de nefrotoxicidad similares a los descritos con el uso de inhibidores del VEGF sistémicos [1] [2].
Estos estudios muestran notables diferencias entre los fármacos: el aflibercept permanece con niveles por encima del IC50 entre 22-33 días tras la inyección, mientras que el ranibizumab, con menor vida media, lo hace durante 5-8 días; por tanto es de esperar que agentes como el aflibercept o el bevacizumab, siendo más potentes y con mayor vida media, tengan más nefrotoxicidad. Sin embargo, la correlación entre supresión de niveles de VEGF y su relevancia clínica está aún hoy en día en fase de investigación [1] [2].
Por otro lado, estudios en animales han mostrado la presencia de anti-VEGF en el glomérulo tras su administración intravítrea, pero aún no han podido aseverar una asociación entre la misma y el fracaso renal o la proteinuria [1] [2] [3].
La bibliografía en relación a glomerulopatías o casos de microangiopatía trombótica tras la inyección intravítrea de anti-VEGF es escasa. En nuestro caso el paciente presentó un síndrome nefrótico completo tras la administración del fármaco. Como parte del estudio del cuadro (Véase Síndromes Clínicos en Nefrología) se solicitó estudio de laboratorio completo y serológico, que resultó negativo. Con el objetivo de filiar la entidad se realizó una biopsia renal (Véase Nefrología al día: Biopsia Renal) que mostró la presencia de glomeruloesclerosis focal y segmentaria colapsante. Ante la agresividad del cuadro se inicio tratamiento con prednisona a 0,5mg/kg/día para estabilizar el podocito. Sin embargo, al haber una clara asociación temporal con el inicio de aflibercept y con ello presumiblemente encuadrarse la glomeruloesclerosis focal y segmentaria dentro del tipo de las secundarias, el tratamiento principal consistió en la retirada del fármaco.
Tras la progresiva retirada de los esteroides (menos de 2,5 mg al día de prednisona a los 3 meses) y en consenso con Oftalmología, por el alto riesgo de ceguera del paciente, se decidió hacer el cambio a ranibizumab, logrando mantener la función renal estable (FG>45ml/min) y la proteinuria negativa, sin recidivas hasta el momento actual con la administración concomitante mensual del nuevo fármaco.
Los anti-VEGF intravítreos son fármacos cada vez más empleados dado el envejecimiento progresivo de la población y la alta prevalencia de diabetes mellitus. Su nefrotoxicidad, principalmente relacionada con el daño podocitario y endotelial, ha sido ampliamente descrita con su administración sistémica, sin embargo, cada vez hay más evidencia de efectos adversos similares con la administración intravítrea.
Este caso clínico lo ejemplifica mediante una glomeruloesclerosis focal y segmentaria asociada a aflibercept que se resuelve tras la retirada de este y se mantiene en remisión completa a pesar del cambio a ranibizumab que se realizó en base a su perfil farmacocinético.
BIBLIOGRAFÍA:
1. Hanna RM, Barsoum M, Arman F, Selamet U, Hasnain H, Kurtz I. Nephrotoxicity induced by intravitreal vascular endothelial growth factor inhibitors: emerging evidence. Kidney Int. 2019 Sep;96(3):572-580. doi: 10.1016/j.kint.2019.02.042. Epub 2019 Apr 9. PMID: 31229276.
2. Shye M, Hanna RM, Patel SS, Tram-Tran N, Hou J, Mccannel C, Khalid M, Hanna M, Abdelnour L, Kurtz I. Worsening proteinuria and renal function after intravitreal vascular endothelial growth factor blockade for diabetic proliferative retinopathy. Clin Kidney J. 2020 Jun 28;13(6):969-980. doi: 10.1093/ckj/sfaa049. PMID: 33391740; PMCID: PMC7769550.
3. Kikuchi Y, Odashima Y, Yoshikawa K, Oda T, Tanaka F, Oikawa H, Ishigaki Y, Asahi K. Renal thrombotic microangiopathy and nephrotic proteinuria induced by intravitreal injection of aflibercept for diabetic macular edema. BMC Nephrol. 2022 Nov 28;23(1):380. doi: 10.1186/s12882-022-03006-z. Erratum for: BMC Nephrol. 2022 Oct 29;23(1):348. PMID: 36443705; PMCID: PMC9706977.
4. Izzedine H, Massard C, Spano JP, Goldwasser F, Khayat D, Soria JC. VEGF signalling inhibition-induced proteinuria: Mechanisms, significance and management. Eur J Cancer. 2010 Jan;46(2):439-48. doi: 10.1016/j.ejca.2009.11.001. Epub 2009 Dec 16. PMID: 20006922.