Sospecha clínica de Nefropatía IgA con fracaso renal agudo asociado
Palabras clave
Nefropatía IgA
Introducción
La nefropatía IgA (NIgA) es la glomerulopatía más frecuente a nivel mundial con una incidencia de 25 casos por millón de habitantes y un riesgo de enfermedad renal crónica avanzada (ERCA o estadio V con FGe < 15 mL/min) entre 20-40% a los 20 años. Presenta diferencias geográficas con mayor incidencia en países asiáticos, donde además presenta mayor riesgo de ERCA. La hipótesis fisiopatológica más aceptada en la actualidad consiste en el modelo “multi-hit”, que pone de manifiesto el papel de la mucosa gastrointestinal y la relevancia de la inmunidad de tal forma que la IgA es fundamental en el desarrollo de lesión renal. (NAD: Nefropatía IgA).
La manifestación de la enfermedad es heterogénea, desde hematuria y/o proteinuria aislada, hasta el fracaso renal agudo (FRA) asociado. La biopsia renal es una prueba de vital importancia de cara a confirmar el diagnóstico y aportar información pronóstica valiosa, con el fin de estratificar el riesgo de los pacientes e individualizar el tratamiento. Presentamos un caso clínico de inicial sospecha de NIgA que debutó con FRA y discutiremos los aspectos teórico-prácticos del mismo.
Caso clínico
Mujer de 32 años oriunda de Rusia, residiendo en Barcelona desde hace años. Sin alergias medicamentosas conocidas, ni antecedentes patológicos o medicación habitual. Consulta al servicio de urgencias por molestias abdominales y coluria de 48 horas tras el inicio de una faringoamigdalitis, la cual debutó un día antes de la misma, en tratamiento con amoxicilina empírica y analgesia con ibuprofeno. La paciente había tenido dos episodios previos de coluria en el pasado coincidiendo con infecciones faringoamigdalares, autolimitados tras la resolución de la infección.
Exploración física: Buen estado general. Afebril, PA 110/70 mmHg. Resto sin alteraciones.
Exploraciones complementarias:
- Análisis sanguíneos: Leucocitos 6.50 10^9/L, hemoglobina 11.1 g/dL, hematocrito 35%, VCM 88.3fl, HCM 28.4pg, plaquetas 246 10^9/L, eosinófilos 0.10 10^9/L, Cr 3,52 mg/dL (CKD-EPI 16 mL/min), HCO3 20,7 mmol/L, Na 136 mEq/L, K 3.5 mEq/L, Cl 103 mEq/L, Mg 2.2 mg/dL, Ca corregido 7.8 mg/dL, Alb 37 g/L., PCR 6 mg/dL, VSG 70 mm/h. Proteinograma y complemento normales. IgA sérica 1g/L. ANCA y antiDNA negativos. Serología virus hepatotropos negativa.
- Orina: Hematíes 100-150/campo, leucocitos 5-10/campo, cociente proteínas/Cr 765 mg/g, cociente albúmina/Cr 170 mg/g.
- Ecografía renal: riñones prominentes, difusamente hiperecogénicos con pérdida de la diferenciación cortico-medular; sugestivo de nefropatía aguda.
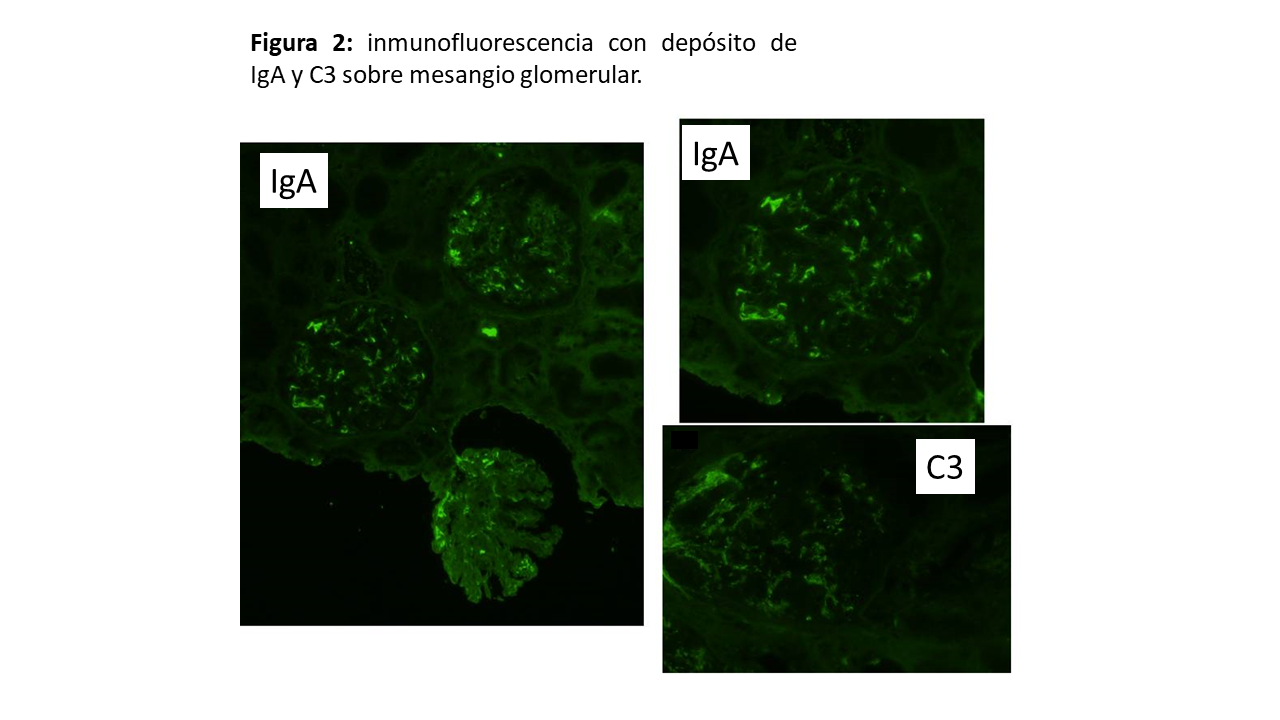
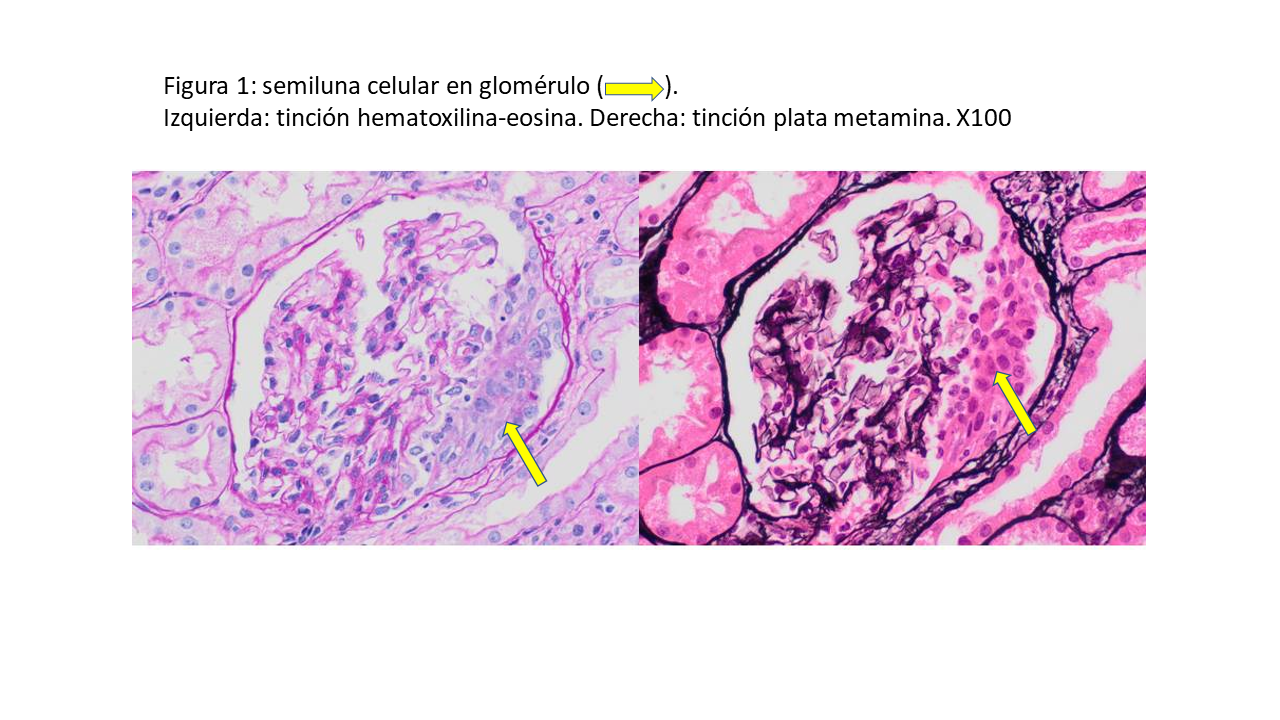
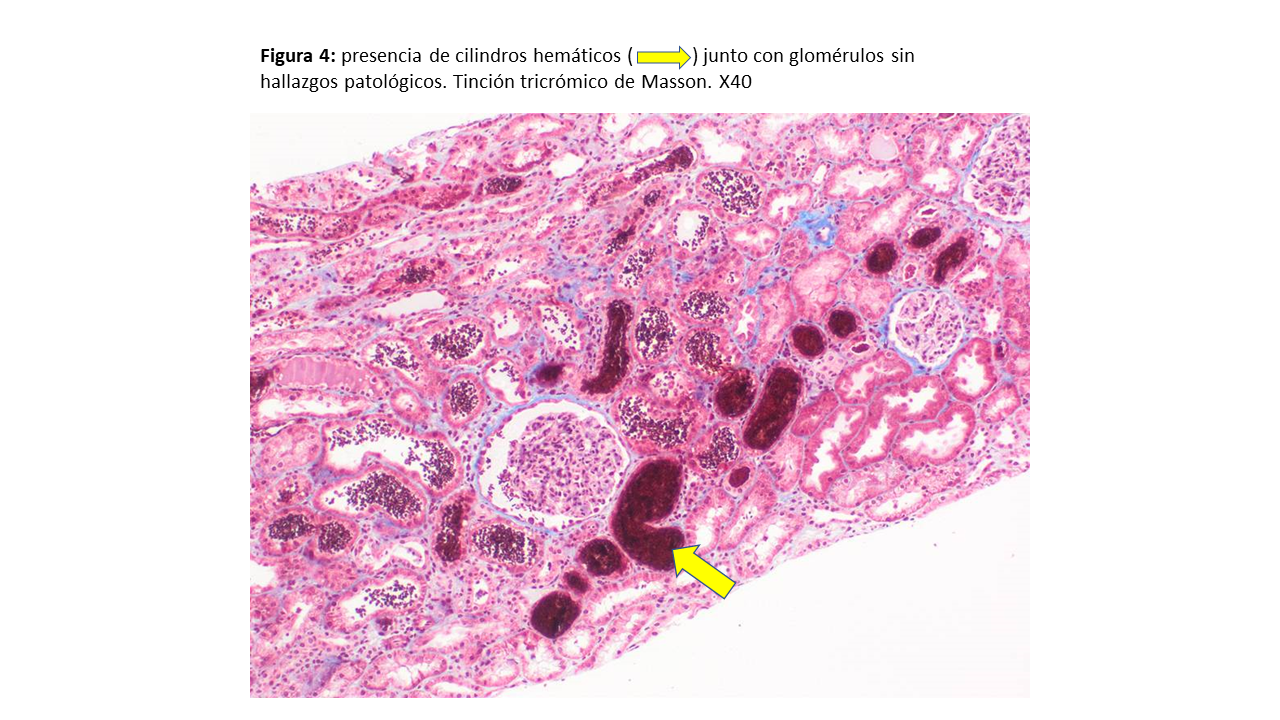
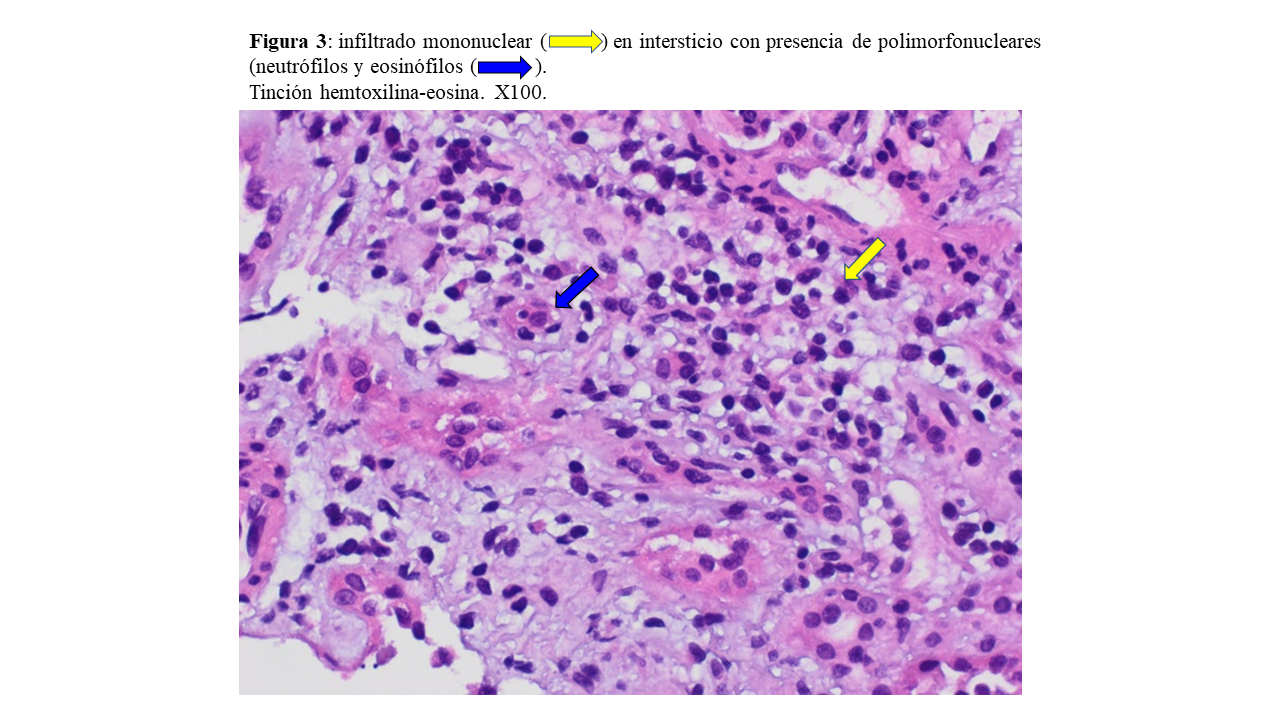
Ante un FRA AKI-3 (Cr 0,7 mg/dL un mes atrás) con alta sospecha de nefropatía IgA, se realiza biopsia renal con el siguiente resultado: 29 glomérulos con hipercelularidad mesangial en 2 de los mismos, sin proliferación endocapilar. Además, glomeruloesclerosis segmentaria en 2 glomérulos junto con la presencia de 2 semilunas celulares (Figura 1). En la inmunofluorescencia destaca positividad para IgA, C3 y cadenas ligeras kappa y lambda (Figura 2). En el intersticio se observa un infiltrado inflamatorio compuesto por células mononucleares, y ocasionales polimorfonucleares neutrófilos y eosinófilos (Figura 3); con un IFTA (fibrosis intersticial y atrofia tubular) inferior al 10%. Por último, cilindros hemáticos (Figura 4) y túbulos dilatados con células descamadas, compatible con necrosis tubular aguda (NTA). En resumen: NIgA con clasificación de Oxford M0 E0 S0 T0 C1 con NTA asociada.
Ante el posible componente de nefritis tubulointersticial inmunoalérgica, se decide inicio de corticoterapia en forma de 3 bolus de 250 mg de metilprednisolona, junto con posterior dosis a razón de 0.4 mg/Kg/día (20mg prednisona total). La paciente presenta una buena evolución desde el punto de vista de función renal (FR) con Cr de 0.77 mg/dL (FGe > 90mL/min) y proteinuria de 300 mg/24h en el control ambulatorio tras tres semanas de tratamiento.
Comentarios
Nuestro caso consiste en una mujer joven que presenta episodios de hematuria macroscópica coincidentes con infecciones respiratorias (“sinfaringítica”), con un FRA grado 3 en el episodio actual. Las etiologías más frecuentes del FRA en el seno de una sospecha de NIgA son: la glomerulonefritis rápidamente progresiva (GNRP), la cual asociaría >50% semilunas en la biopsia, o una NTA asociada a la toxicidad tubular de los hematíes, incluso por la obstrucción tubular por cilindros hemáticos en casos de hematuria macroscópica. En nuestro caso, la presentación clínica era altamente sugestiva de NIgA, pero la presencia de FRA obligaba a descartar otras causas de insuficiencia renal rápidamente progresiva en una mujer joven, como podrían ser: nefritis lúpica, glomerulonefritis extracapilar, glomerulopatía por C3 o glomerulonefritis asociada a infección. Por ello, se amplió la batería de pruebas diagnósticas (inmunología y complemento) y se realizó la biopsia renal, que no sólo nos confirmó el diagnóstico de sospecha, sino que propuso dos causas para el FRA de nuestra paciente: primero, la NTA asociada a la NIgA secundaria a la toxicidad tubular hemática, y segundo, la presencia de un infiltrado mononuclear con eosinófilos sugestivo de nefritis tubulointersticial inmunomediada (NTI), a pesar de la ausencia de eosinofilia en la analítica inicial, que podría estar relacionada con la antibioterapia recibida (amoxicilina) o con el fármaco analgésico (ibuprofeno).
Histológicamente, la NIgA se describe según la escala de Oxford (MEST-C), siendo la más utilizada y validada, y que presenta los siguientes hallazgos: hipercelularidad mesangial (M), hipercelularidad endocapilar (E), glomeruloesclerosis segmentaria (S), atrofia tubular y fibrosis intersticial (T) y semilunas (C). Cada una de estas variables se correlaciona independientemente con el pronóstico renal; además, la presencia de semilunas presenta una relación directamente proporcional al fallo renal. Nuestra paciente presenta una puntuación C1 junto con NTA y NTI; siendo este último hallazgo el responsable del inicio de corticoterapia en forma de bolus, ya que actualmente no existe evidencia suficiente según las guías internacionales para inicio de terapia inmunosupresora en NIgA basándonos en la histología.
Los hallazgos histológicos añadidos a variables clínicas y demográficas conforman una escala predictiva de deterioro del 50% de la FR conocida como “International IgAN Prediction Tool”. No obstante, no existen biomarcadores séricos o urinarios que permitan estratificar e identificar aquellos pacientes con mayor riesgo de deterioro renal, ni biomarcadores pronósticos más allá de la proteinuria y la FR para el seguimiento. Nuestra paciente presenta un riesgo de pérdida del 50% de la FR al año del 26,5%, sin tener en cuenta la presencia de semilunas, la cual era el único hallazgo histológico del MEST-C en nuestro caso y, como hemos comentado previamente, su presencia se correlaciona directamente con peor pronóstico renal.
En relación con el tratamiento de la NIgA, no existen dudas sobre la terapia de soporte basada en nefroprotección con IECAs/ARA-2 añadiendo, si hiciera falta, los inhibidores del SGLT-2, junto con un control de los diversos factores de riesgo cardiovascular. Respecto a la corticoterapia, existe controversia a raíz de los dos únicos grandes estudios en NIgA: STOP-IgAN vs TESTING. A pesar de sus diferencias poblacionales, el primero subraya la ausencia de riesgo/beneficio de la inmunosupresión añadida a la terapia de soporte convencional; mientras que el segundo muestra resultados estadísticamente significativos respecto al beneficio de la corticoterapia, incluso a bajas dosis y con menores tasas de toxicidad farmacológica. Este debate abre la puerta a futuros trabajos que respondan a la cuestión del posible beneficio de esta terapia añadida en la NIgA y especialmente los posibles subgrupos que se beneficiarían de este tratamiento. Otras alternativas terapéuticas en desarrollo son: budesonida oral, que ejercería un papel inmunomodulador a nivel local (mucosa gastrointestinal), inhibiendo los primeros pasos del modelo fisiopatológico aceptado; inhibidores del complemento (ej.: ravulizumab, iptacopan, avacopan, narsolipmab), bloqueadores de la señal de linfocitos B (ej.: rituximab, atacicep, telitacicept) y antagonistas de la endotelina (ej.: sparsentan).
Nuestro caso podría sugerir una presentación agresiva de la NIgA dada la presencia de semilunas, así como el llamativo hallazgo de cilindros tubulares que ocasionaron NTA y que, añadiendo la presencia de NTI, todo en su conjunto, explicaría el deterioro de FR. La evolución pone de relieve la cuestión del papel que haya podido tener la corticoterapia, ya que esta evolución favorable podría ser por: 1) resolución de la NTA independiente de la prednisona, 2) efecto beneficioso de los corticoides sobre la presentación de la NIgA, con semilunas en la biopsia o 3) la resolución de la NTI secundaria a toxicidad farmacológica con la corticoterapia administrada.
Todo lo expuesto previamente nos sirve para concluir acerca de la suma importancia de la biopsia renal en la sospecha de NIgA como método diagnóstico, pronóstico y de caracterización etiológica del posible FRA asociado. Subrayamos que no todo FRA en NIgA es secundario a la NTA asociada a la hematuria y como en nuestro caso, pueden aparecer diagnósticos no sospechados que son consecuencia de la exposición a fármacos (NTI) y no tienen que ver con la patología de base. No debemos olvidar la incógnita de la caracterización clínica e histológica de la NIgA, de cara a la estratificación de los pacientes para un tratamiento individualizado, a la espera de biomarcadores, así como el desarrollo de estrategias terapéuticas que modifiquen la historia natural de la enfermedad.