Nefropatía Tubulointersticial Familiar. Utilidad del Panel Renal
INTRODUCCIÓN
Las nefropatías tubulointersticiales son un grupo de enfermedades que afectan principalmente el intersticio renal e incluyen enfermedades familiares asociadas a la mutación de un gen (UMOD, MUC1, HNF1B, REN y de forma más rara, SEC61A1) (NAD: Nefropatía tubulointersticial autosómica dominante). Este daño tubulointersticial puede asociarse a la hiperuricemia y está relacionado a la progresión de la enfermedad renal. Actualmente el panel renal, se incluye como herramienta diagnóstica en el estudio etiológico de la enfermedad renal crónica (ERC) en pacientes con segregación familiar. Presentamos un caso clínico en una paciente trasplantada sin diagnóstico preimplantacional.
EXPOSICIÓN DEL CASO
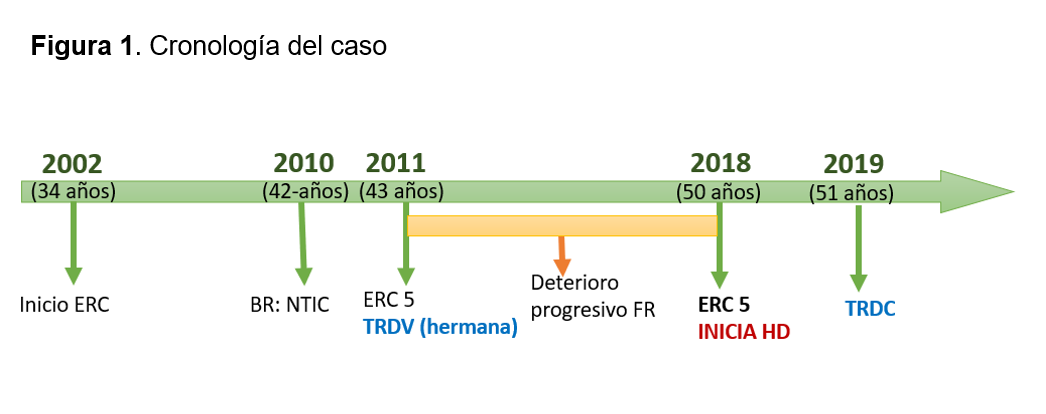
Se trata de una mujer que en 2002 se diagnostica lupus eritematoso cutáneo (a los 34 años), sin afectación sistémica en ningún momento (ANA+1/320 estables y complemento normal) y se detecta ERC. En los años siguientes: hipertensión arterial (HTA) controlada, con deterioro progresivo de la función renal (FR) y albuminuria (200-400mg/día).
Antecedentes familiares: padre con ERC (multifactorial: monorreno funcional por nefrolitiasis e HTA mal controlada). En 2010 se realiza biopsia renal (BR) que mostró fibrosis intersticial y atrofia tubular (FIAT) del 30%, 3/7 glomérulos esclerosados globalmente e inmunofluorescencia (IF) negativa, compatible con nefritis tubulointersticial crónica (NTIC) inespecífica. Así se encontró una ERC avanzada no pudiéndose filiar patología de base (Figura 1).
En situación de prediálisis en 2011 recibió un trasplante renal de donante vivo (TRDV) de hermana HLA idéntica (creatinina nadir 0.9 mg/dL). Posteriormente, presentó deterioro de la FR, con microhematuria y mínima albuminuria (100-300mg/día) en algunos sedimentos, realizándose varias BR entre 2011-2018, compatibles con NTIC (FIAT 30%/infiltrado linfocitario) sin signos de rechazo y con IF negativa. En 2018 perdió el injerto renal e inició hemodiálisis (HD). En 2019 se realizó el segundo trasplante renal de donante cadáver (TRDC) (creatinina nadir 0.9 mg/dL).
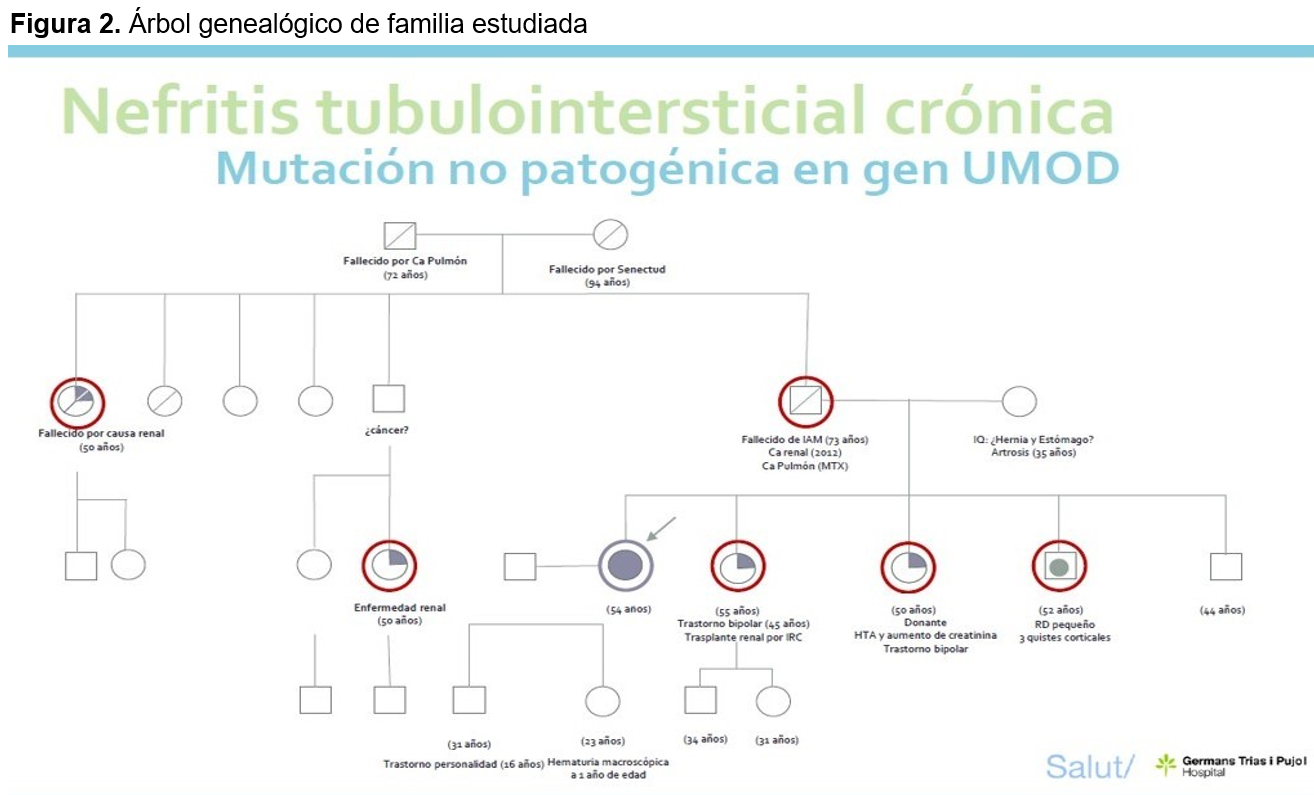
Tras el segundo trasplante, se inició estudio de enfermedad renal en la hermana donante de vivo. Revisando los antecedentes, se identificó una importante agregación familiar (Figura 2):
- Padre (único con ERC conocida inicialmente) y tía paterna ya fallecidos con ERC y en tratamiento sustitutivo con HD.
- Primera hermana con ERC (en la BR presentaba NTIC, trasplantada actualmente)
- Segundo hermano sin ERC (también en el momento actual)
- Tercer hermano con ERC estadio 3 (sin BR)
- Cuarta hermana (donante) afecta de ERC en situación de prediálisis (sin BR)
Dados los antecedentes renales familiares se remitió a la paciente para estudio genético y panel renal o secuenciación paralela masiva (análisis molecular next generation sequencing-NGS).
Se identificó entonces variante de significado incierto en la posición c.172G>A del gen UMOD (asociado a enfermedad renal tubulointersticial autosómica dominante). Dada la fuerte agregación familiar y el hallazgo de la mutación, se derivó al resto de hermanos para búsqueda de la mutación, encontrándose la misma en tres de los cuatro hermanos (es decir, en todos los hermanos afectos de ERC) (Figura 2).
COMENTARIOS:
Las nefropatías intersticiales presentan una afectación principalmente del intersticio renal; las formas crónicas se caracterizan histológicamente por la presencia de FIAT pudiendo hallarse infiltrados celulares aislados, y en los casos de mayor cronicidad, presencia de lesiones glomerulares en forma de fibrosis periglomerular y esclerosis glomerular global, así como engrosamiento fibrointimal vascular (NAD: Nefropatías intersticiales).
Dentro de las nefropatías tubulointersticiales crónicas existen algunas formas familiares con una herencia autosómica dominante (HAD) asociadas a varias mutaciones genéticas (NAD: Nefropatía tubulointersticial autosómica dominante, Tabla 2). Las guías KDIGO han agrupado estas nefropatías bajo el nombre de nefropatía tubulointersticial autosómica dominante (NTAD), caracterizándose por la triada de FIAT, ERC estadio 5 y HAD [1].
Las NTAD se caracterizan por presentar una penetrancia del 100% aunque con gravedad y edad de aparición variables incluso dentro de una misma familia. Clínicamente, se caracterizan por un sedimento poco activo sin proteinuria o siendo esta menor a 1g/día, y sólo excepcionalmente presencia de microhematuria. Los afectos suelen presentar HTA, aunque no es grave ni precoz. En los casos de mutaciones en el gen UMOD (gen que codifica la uromodulina o proteína de Tamm-Horsfall) el debut de la enfermedad renal es entre los 25-70 años, siendo más precoz en pacientes con crisis gotosas (NAD: Nefropatía tubulointersticial autosómica dominante).
En la histología la BR es inespecífica habitualmente con FIAT con glomérulos normales, IF negativa y una microscopía electrónica con acumulación de uromodulina mutante en el retículo endoplásmico (RE) de las células del asa de Henle. La uromodulina es la proteína más abundante de la orina en individuos sanos que se produce por las células epiteliales de la porción ascendente del asa de Henle, cuya función no se conoce, aunque se ha relacionado con la impermeabilización del túbulo distal y con actividad proinflamatoria [2]. La presencia de uromodulina mutante se ha asociado con la incapacidad de concentrar la orina y con la fibrosis tubulointersticial. Están descritas más de 125 mutaciones en el gen UMOD asociándose la mayoría de ellas a hiperuricemia y con una fracción de excreción de uratos inferior a 0.05 (NAD: Nefropatía tubulointersticial autosómica dominante).
No existe un tratamiento dirigido contra las NTAD, por lo que el tratamiento se basa en el control de los factores de riesgo de progresión de ERC (HTA, DM, tabaco, obesidad) y en controles anuales de la función renal. No se recomienda la restricción de sal y el uso de diuréticos debe realizarse con precaución en pacientes con hiperuricemia, pues esta puede agravarse. Se recomienda el tratamiento con hipouricemiantes como alopurinol e incluso febuxostat, y se recomienda en estos casos el losartán como antihipertensivo por su efecto uricosúrico. Sin embargo, una vez llegados a ERC estadio 5 el trasplante renal es el tratamiento de elección ya que la enfermedad no recurre en el injerto.
En el caso expuesto, la paciente presentó HTA precoz, microalbuminuria, microhematuria, deterioro de la FR en ausencia de hiperuricemia que se inició a los 34 años y una BR compatible con NTIC tanto en su riñón nativo como en el primer injerto renal de donante vivo HLA idéntico. El estudio genético puso de manifiesto la variante de significado incierto c.172G>A del gen UMOD, mutación que se ha asociado a NTAD [3].
Ante el hallazgo de dicha mutación y la importante agregación familiar, se realizó screening encontrándose la mutación en todos los hermanos que presentaban alteración de la función renal (4/5). La recidiva en el primer injerto recibido se debió a que la donante (hermana) estaba también afecta de la NTAD, a pesar de que en el momento de la donación no presentaba todavía signos de ERC. Especial atención merecería el estudio de la enfermedad renal con sospecha de agregación familiar. Se debe resaltar la importancia de la historia clínica con énfasis en la anamnesis familiar, con intención de identificar un probable componente genético, en especial en los casos de nefropatía no filiada, aunque en nuestro caso la sospecha fue tardía dada la inespecificidad de la clínica y la variabilidad intrafamiliar en el debut de la enfermedad renal.
En conclusión, el uso de técnicas de NGS-exoma en el estudio de la ERC, es de gran importancia y debe considerarse, ante pacientes con ERC no filiadas y patrón de agregación familiar, además del estudio en potenciales donantes consanguíneos con el receptor, permitiendo un diagnóstico precoz de los familiares de riesgo y un control estricto de los factores de riesgo en los familiares afectos.
REFERENCIAS BIBLIOGRÁFICAS:
1.- Eckardt KU, Alper SL, Antignac C, Bleyer AJ, Chauveau D, Dahan K, Deltas C, Hosking A, Kmoch S, Rampoldi L, Wiesener M, Wolf MT, Devuyst O; Kidney Disease: Improving Global Outcomes. Autosomal dominant tubulointerstitial kidney disease: Diagnosis, classification, and management - A KDIGO consensus report. Kidney Int. 2015;88:676–83. doi: 10.1038/ki.2015.28.
2.- Bleyer AJ, Kmoch S. Tamm Horsfall Glycoprotein and Uromodulin: It Is All about the Tubules! Clin J Am Soc Nephrol. 2016;11: 6-8. doi: 10.2215/CJN.12201115.
3.- Ayasreh N, Bullich G, Miquel R, Furlano M, Ruiz P, Lorente L, et al. Autosomal Dominant Tubulointerstitial Kidney Disease: Clinical Presentation of Patients With ADTKD-UMOD and ADTKD-MUC1. American Journal of Kidney Diseases. 2018 Sep 1;72(3):411–89)