Nefronoptisis con displasia esquelética. Síndrome de Mainzer-Saldino
INTRODUCCIÓN
Las nefronoptisis o ciliopatias relacionadas con la nefronoptisis son un grupo de enfermedades de causa genética producidas por mutaciones en proteínas que afectan la función o la estructura del aparato ciliar. Todas ellas comparten características anatomopatológicas y clínicas, siendo la alteración en la funcionalidad renal el nexo común y dando por ello lugar al desarrollo una nefritis tubulointersticial crónica con alteración en la capacidad de concentración urinaria y en ocasiones un déficit de reabsorción de sodio y progresión paulatina del deterioro del filtrado glomerular.
En un 10-20% de los pacientes puede además aparecer afectación extrarrenal, siendo el cerebro, el esqueleto, el hígado y los ojos los principales órganos afectados.
Representa una de las principales causas de enfermedad renal terminal de origen genético en la infancia, siendo la primera causa monogénica en las tres primeras décadas de la vida. Se han identificados diferentes genes implicados, con una herencia autosómica recesiva en la mayoría de los casos, siendo el NHPH1 el más frecuente (20%). Sin embargo, en torno al 30% de los pacientes no se identifica ninguna mutación genética responsable (Ver Nefronoptisis en NAD: https://www.nefrologiaaldia.org/es-articulo-nefronoptisis-256: )
CASO CLÍNICO
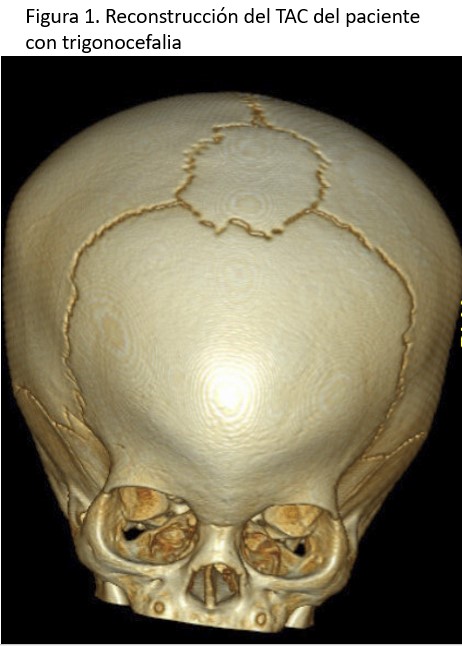
Lactante de 12 meses de edad, derivado a consultas de nefrología por alteración en la función renal detectada en una analítica preoperatoria. Se trata de un niño de sexo masculino con antecedentes de estancamiento ponderoestatural, cifoscoliosis en seguimiento con traumatología, retraso psicomotor y craneosinostosis (trigonocefalia como consecuencia de la fusión de sutura metópica), que se encuentra pendiente de intervención quirúrgica (Figura 1).
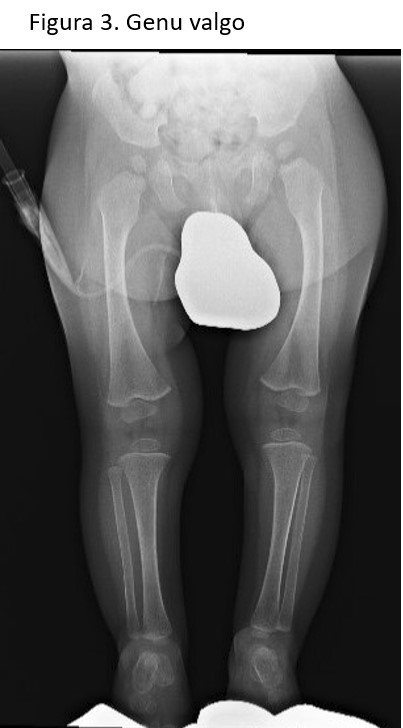
No tenía antecedentes familiares de enfermedades renales y la gestación había transcurrido sin incidencias y con un período perinatal normal. El paciente presentaba en la exploración, además de las malformaciones esqueléticas mencionadas, un genu valgo marcado bilateral (Figura 3). La tensión arterial estaba dentro de los rangos de normalidad.
Ya en su seguimiento en consulta se detecta una primera creatinina de 1.26 mg/dL (Filtrado glomerular estimado Schwartz IDMS -0,413- 32 mL/min/1.73m2), elevación de cifras de urea (163 mg/dL), hiperpotasemia (potasio 6.50 mmol/L), hiperfosfatemia (fosfato 8.3 mg/dL), acidosis metabólica e hiperparatiroidismo (PTH de 419 pg/mL).
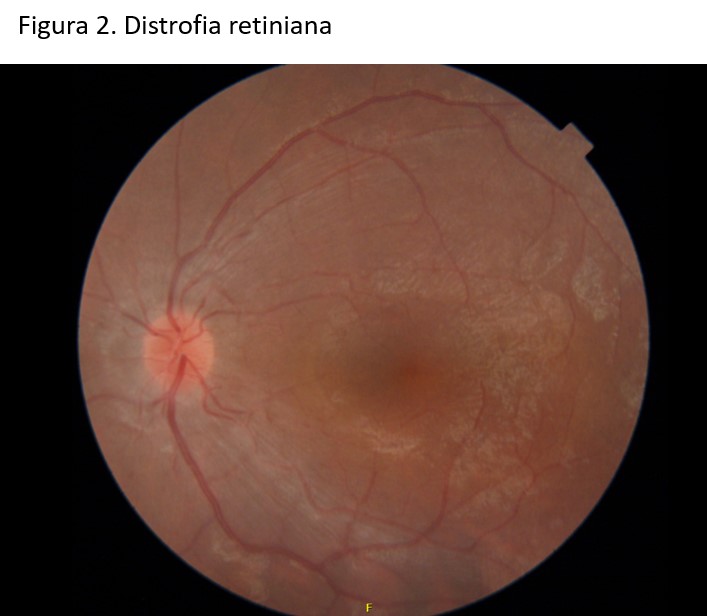
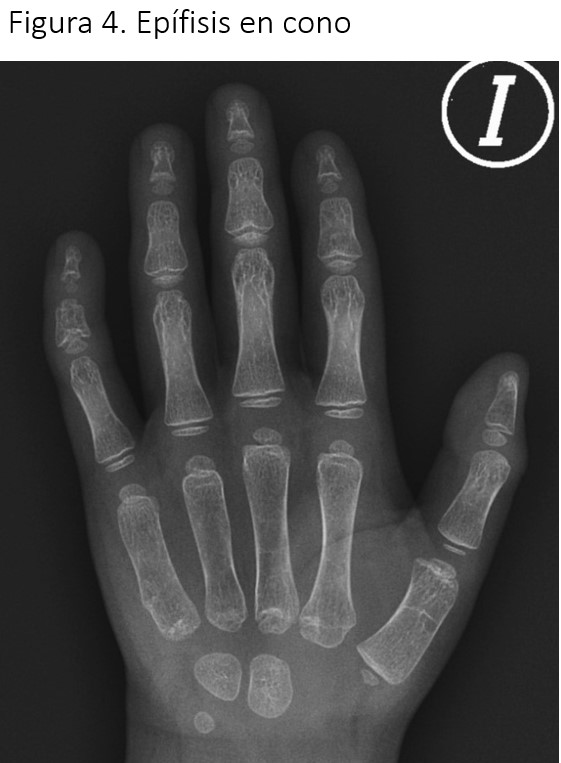
Se amplió estudio con ecografía renal donde se observaron riñones hiperecogénicos con mala diferenciación corticomedular de forma bilateral y sin evidencia de quistes. Dentro del estudio de extensión extrarrenal se encontraron quistes en la vía biliar intrahepática con dilatación de la misma y, en radiografías óseas, la presencia de falanges distales con epífisis en cono (Figura 4). Durante el seguimiento presenta clínica de ceguera nocturna progresiva, con exploración oftalmología compatible con distrofia retiniana (Figura 2).
Se realizó estudio genético con secuenciación masiva de panel de genes asociados a enfermedades renales quísticas y de anomalías congénitas del riñón y el tracto urinario, con negatividad para NPHP1 pero encontrándose dos variantes en heterocigosis en el gen WDR19 (c.[14424>G] y c.[2741C>A], catalogadas como probablemente patogénicas.
A los pocos meses de evolución, y pese al tratamiento médico, el paciente presenta progresión de su enfermedad renal crónica, llegando a estadio terminal y precisando inicio de depuración extrarrenal (diálisis peritoneal) a los 20 meses de edad. El paciente recibió un trasplante renal de donante cadavérico 3 meses después (23 meses).
COMENTARIOS
La nefronoptisis es una enfermedad de base genética que se manifiesta en la infancia. El diagnóstico se sugiere por los hallazgos clínicos, la presencia o no de manifestaciones extrarrenales y los resultados ecográficos (generalmente riñones de tamaño normal o levemente disminuidos, hiperecogénicos con pérdida de la diferenciación corticomedular y solo en algunas ocasiones con visualización de quistes cortico-medulares). Aun así, debido a la amplia variabilidad genotípica-fenotípica, la confirmación mediante pruebas de genética debería ser imprescindible en todos los casos.
El fenotipo clínico identificado como síndrome de Mainzer-Saldino o síndrome conorrenal incluye enfermedad renal crónica en forma de nefronoptisis junto a al hallazgo de epífisis en cono en las falanges. Además, la degeneración retininana en forma de retinitis pigmentaria atípica (sin depósito de pigmento) es casi constante, pudiendo presentar otras afectaciones de forma variable como displasias esqueléticas (alteración en fémur proximal o craneosinostosis), talla baja, fibrosis hepática y ataxia cerebelosa.
Se trata de una ciliopatía multisistémica muy infrecuente, y las mutaciones que se identifica con más frecuencia son las del gen IFT140, aunque pacientes con estas mutaciones también pueden presentar fenotipos solapados con la displasia torácica asfixiante (síndrome de Jeune).
En el caso que presentamos, se representa un paciente con una enfermedad renal crónica sugestiva de nefronoptisis y con un fenotipo clínico muy sugerente de síndrome de Mainzer-Saldino (enfermedad renal crónica con riñones hiperecogénicos y mal diferenciados, distrofia retiniana, craneosinostosis y epífisis en cono). No obstante, las mutaciones encontradas en nuestro paciente se encuentran el gen WDR19, que se han documentado de forma infrecuente como responsable del síndrome de Senior-Løken, que también puede presentar nefronoptisis y degeneración macular. En la literatura también se ha descrito un caso con mutación en WDR19 y manifestaciones clínicas sugerentes del síndrome de Mainzer-Saldino.
La heterogeneidad genética y clínica es el distintivo de las ciliopatias multisistémicas. Se ha demostrado que diferentes mutaciones en el mismo gen ciliar único pueden dar lugar a una amplia gama de fenotipos distintos, con una expresividad y variabilidad genotipo-fenotipo muy relevante, teniendo como resultado desde nefronoptisis aisladas a condiciones letales durante el período embrionario. Este punto remarca la necesidad de realizar estudios genéticos en todos los pacientes, siendo arma fundamental para su manejo diagnóstico y pronóstico.
Pese a no existir un tratamiento específico de las nefronoptisis, un diagnóstico precoz puede permitir una mayor vigilancia y prevención de las manifestaciones extrarrenales, una intervención temprana para enlentecer la progresión de la enfermedad renal crónica, programación adecuada del método de terapia renal sustitutiva y poder ofrecer al paciente y a su familia información adecuada sobre el pronóstico y evolución esperable de la enfermedad.
BIBLIOGRAFÍA
-Perrault I et al; Mainzer-Saldino syndrome is a ciliopathy caused by IFT140 mutations. The American Journal of Human Genetics 90, 864-870, 2012.
-Luo F, Tao Y-H; Nephronophthisis: A review of the genotype-phenotype correlation. Nephrology 23, 904-911; 2018.