Hipertensión Arterial Esencial
Palabras clave
Presión arterial, Tensión arterial, Riesgo cardiovascular, Hipertensión arterial resistente
Introducción
La presión arterial (PA) elevada desde niveles óptimos es el principal factor de riesgo de enfermedad y muerte en el mundo [1]. La PA es una variable que se distribuye de forma aproximadamente normal en la población mientras que la relación entre la PA y el desarrollo de enfermedad cardiovascular (ECV) es continua y lineal a partir de cifras > 115/75 mmHg [2]. En España, la prevalencia de hipertensión arterial (HTA) en población adulta oscila entre el 33,3% y el 42,6% [3][4], siendo los grados de conocimiento (en torno al 60%) y control global (en torno al 25%) muy bajos [5]. La HTA constituye uno de los principales motivos de consulta médica alcanzando la prevalencia 47,5% en adultos en Atención Primaria [6]. Estas prevalencias y el impacto en el pronóstico cardiovascular y global justifican que la PA deba medirse de forma sistemática en cualquier contacto de las personas con el sistema sanitario o con cualquier tipo de reconocimiento médico de tal forma que todo adulto debería conocer sus cifras de PA.
Aunque la relación entre la PA y la morbimortalidad por ECV y enfermedad renal es continua, los umbrales para el diagnóstico de HTA y para los objetivos de control son arbitrarios y se basan en que los beneficios de tratar sean superiores a los de no tratar. Los objetivos de control han constituido clásicamente fuente de controversia si bien evidencias recientes han promovido unos objetivos terapéuticos de PA más bajos, especialmente en sujetos con alto riesgo cardiovascular (RCV) [7][8][9][10], e incluso se ha propuesto una redefinición de la HTA en Estados Unidos de América [11][12].
El presente capítulo constituye la actualización del tema HTA esencial que ha sido tratado por José María Alcázar y Luis Orte desde las primeras ediciones en formato clásico de Nefrología al Día [13] y continúa la larga tradición de la Nefrología española en participar en la elaboración de las guías sobre HTA en nuestro país [14][15][16].
Definición
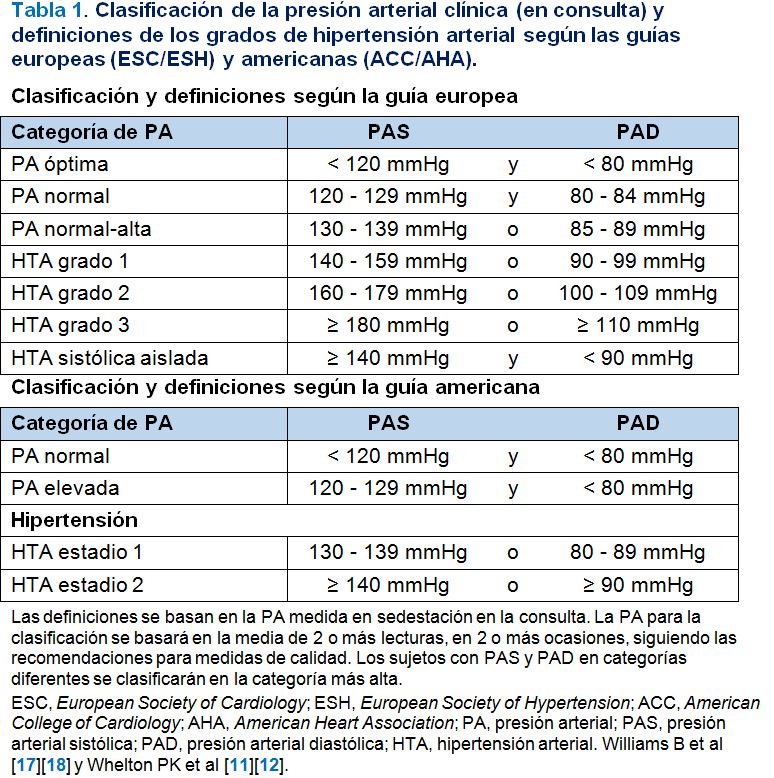
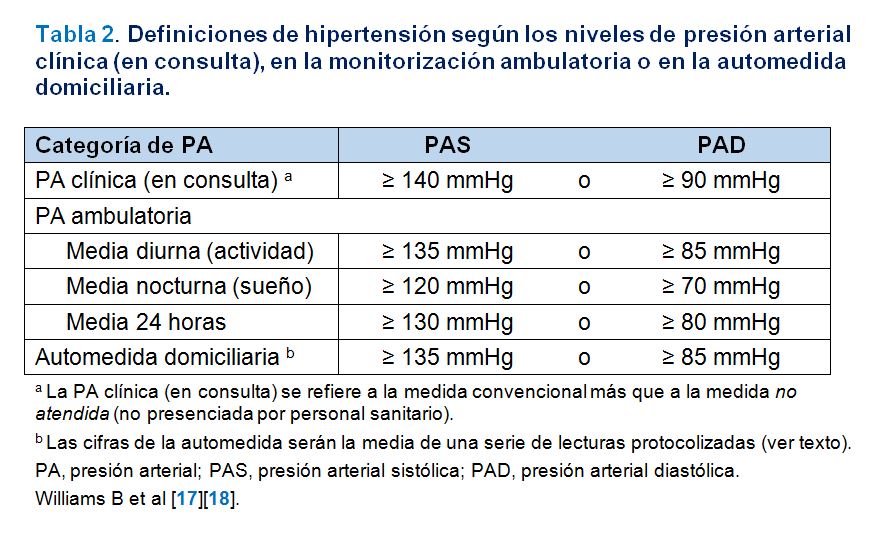
La HTA se define como una PA elevada de forma mantenida. La relación entre la PA y el RCV y renal es continua pero, por razones prácticas de cara al diagnóstico y a la toma de decisiones terapéuticas, se establecen valores umbral arbitrarios para definir ‘normotensión’ e ‘hipertensión’. Las guías norteamericanas, recientemente propuestas por el American College of Cardiology, la American Heart Association y una serie de sociedades e instituciones relacionadas (ACC/AHA 2017), han definido HTA como unas cifras de PA iguales o superiores a 130/80 mmHg [11][12]. Sin embargo, en Europa las guías conjuntas de la Sociedad Europea de Cardiología (European Society of Cardiology, ESC) y de la Sociedad Europea de Hipertensión (European Society of Hypertension, ESH) de 2018 han mantenido el umbral definitorio de HTA en 140/90 mmHg [17][18]. En la (Tabla 1) se expone la clasificación de la PA clínica (en consulta) y las definiciones de los grados de HTA según las guías europeas ESC/ESH 2018 y las guías americanas ACC/AHA 2017. Además, y como se comentará más adelante, ambas guías recomiendan conocer los niveles de PA ambulatoria, aquella tomada fuera de la consulta, para confirmar el diagnóstico de HTA. En el caso de la guía ESC/ESH 2018 incluso también se define la HTA en función de las cifras de PA ambulatoria tal y como se expone en la (Tabla 2).
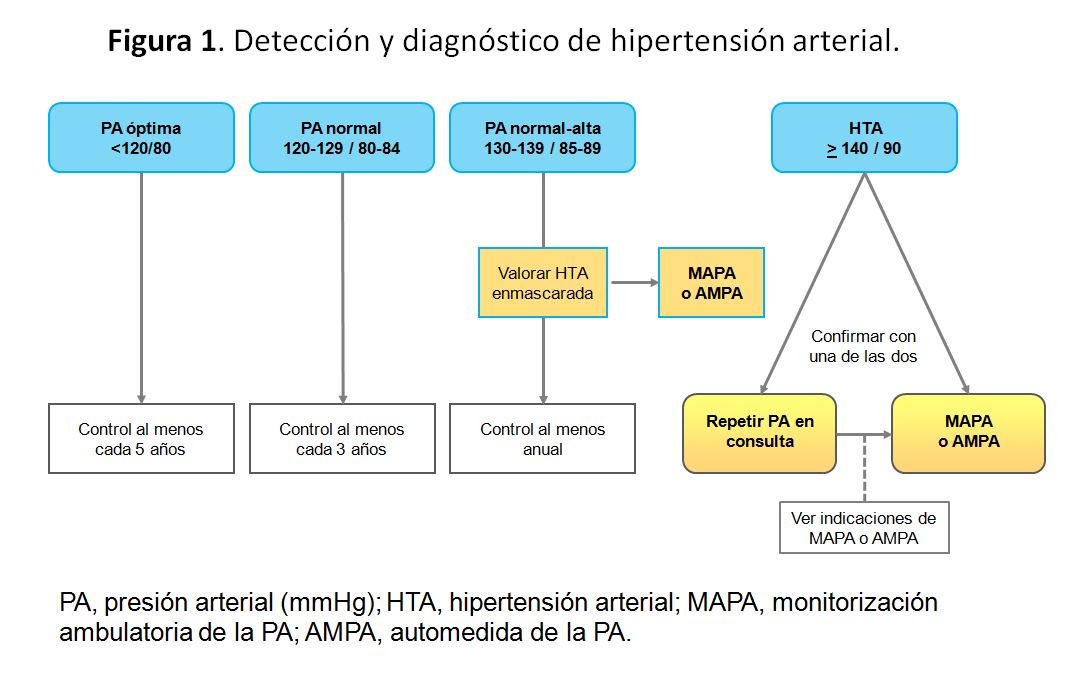
Como se ha comentado anteriormente, la elevada prevalencia de la HTA y el impacto de ésta en el pronóstico vital justifican que todo adulto debería conocer sus cifras de PA. La medida de la PA debe llevarse a cabo de forma sistemática en cualquier contacto de las personas con el sistema sanitario o en cualquier tipo de reconocimiento médico y posteriormente registrarse con periodicidad ajustada al nivel de PA inicial como se refleja en la (Figura 1) [17][18].
Causas de hipertensión arterial
La causa principal de HTA es la HTA esencial o primaria que corresponde a aproximadamente el 90% de los casos. La HTA secundaria a una causa en principio corregible se puede detectar en un 10% de los pacientes. La HTA esencial es un trastorno muy heterogéneo de base poligénica en el que influyen múltiples genes o combinaciones genéticas [17]. Se han identificado hasta 120 loci asociados con la regulación de la PA pero, incluso analizados conjuntamente, explican una mínima parte de la herencia de la HTA [19]. Existen unas formas monogénicas de HTA, muy infrecuentes, como el síndrome de Liddle o el aldosteronismo corregible mediante glucocorticoides en las que una única mutación genética condiciona la HTA [20].
En la HTA esencial, sobre la base poligénica citada, una serie de factores adquiridos o ambientales ejercen un efecto deletéreo para el desarrollo de HTA. Entre estos factores destacan el sobrepeso y la obesidad, el sedentarismo, el contenido elevado en sal de la dieta, la dieta pobre en potasio y la ingesta excesiva de alcohol.
Con respecto a la HTA secundaria, las causas se clasifican en frecuentes e infrecuentes. Entre las primeras figuran la enfermedad renal parenquimatosa, la enfermedad renovascular, el hiperaldosteronismo primario, el síndrome de apnea-hipopnea del sueño y la HTA inducida por fármacos o drogas incluido el alcohol. Entre las causas infrecuentes de HTA destacan el feocromocitoma, el síndrome de Cushing, el hipertiroidismo, el hipotiroidismo, el hiperparatiroidismo, la coartación de aorta y varios síndrome de disfunción suprarrenal distintos a los anteriores [21]. En el apartado dedicado a la evaluación del paciente hipertenso se expondrán las claves para la sospecha de una HTA secundaria.
Medida de la presión arterial
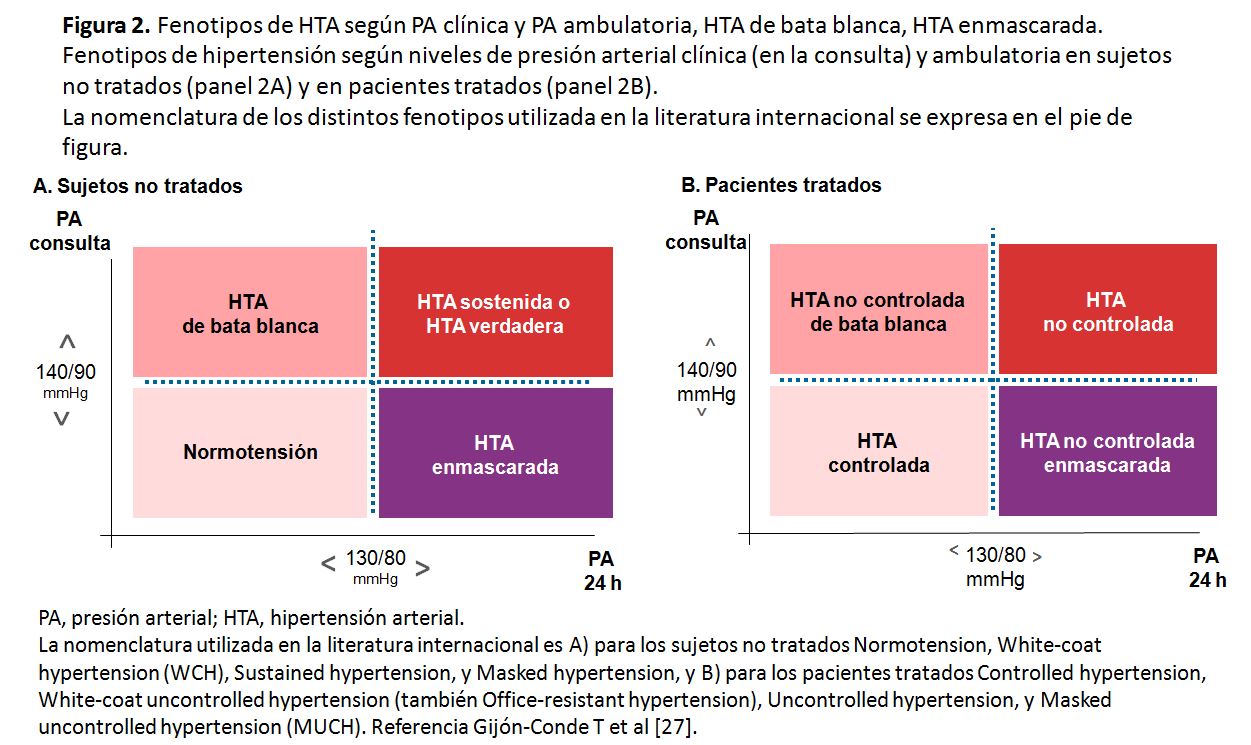
La mayoría del conocimiento actual sobre la HTA está basado en estudios con medidas de la PA clínica (en la consulta). Sin embargo, esta técnica es considerada como limitada pues ofrece información únicamente de un momento concreto y presenta numerosos sesgos [11][12][17][18]. Por ello, tanto en la guía Americana ACC/AHA 2017 [11][12] como en la Europea ESC/ESH 2018 [17][18] se recomienda conocer las niveles de PA ambulatoria para confirmar el diagnóstico de HTA. Como se ha comentado antes, en la guía ESC/ESH 2018 incluso también se define la HTA en función de las cifras de PA ambulatoria (Tabla 2). Las guías británicas NICE (National Institute for Health and Clinical Excellence) ya recomendaron en 2011 realizar una monitorización ambulatoria de la PA (MAPA) para confirmar el diagnóstico de HTA [22]. Posteriormente, otras guías nacionales también han implementado esta recomendación [23][24][25][26][27]. En nuestro medio se recomienda confirmar el diagnóstico de HTA bien con medidas estandarizadas en la consulta repetidas o mediante técnicas ambulatorias de medida de la PA como la MAPA o la automedida domiciliaria de la PA (AMPA). La disponibilidad de la MAPA en nuestro medio presenta una variabilidad elevada [28] por lo que en la reciente guía de la Sociedad Española de Hipertensión - Liga Española para la Lucha contra la Hipertensión Arterial (SEH-LELHA) se indica la recomendación a los profesionales sanitarios, a las sociedades científicas y a las administraciones sanitarias de implementar la MAPA para el diagnóstico de la HTA y para su seguimiento [27]. Además, la MAPA permite diagnosticar aquellas situaciones de falta de concordancia en la clasificación de los pacientes según la PA clínica y la PA ambulatoria como son la HTA de bata blanca y la HTA enmascarada. Las denominaciones de los 4 fenotipos de HTA según la situación de la PA en la consulta y la PA ambulatoria, tanto en pacientes no tratados como tratados, se exponen en la (Figura 2) [27]. Las prevalencias de HTA de bata blanca y de HTA enmascarada son elevadas pudiendo llegar a estar presentes en uno de cada 3 individuos o pacientes con PA elevada o con PA normal en la consulta respectivamente [27][29]. El correcto diagnóstico de estos fenotipos de HTA es crucial pues el sujeto o paciente con HTA de bata blanca puede verse sometido a exploraciones complementarias no indicadas y a un tratamiento innecesario y no exento de riesgos mientras que el sujeto o paciente con HTA enmascarada estará sometido al riesgo del infratratamiento.
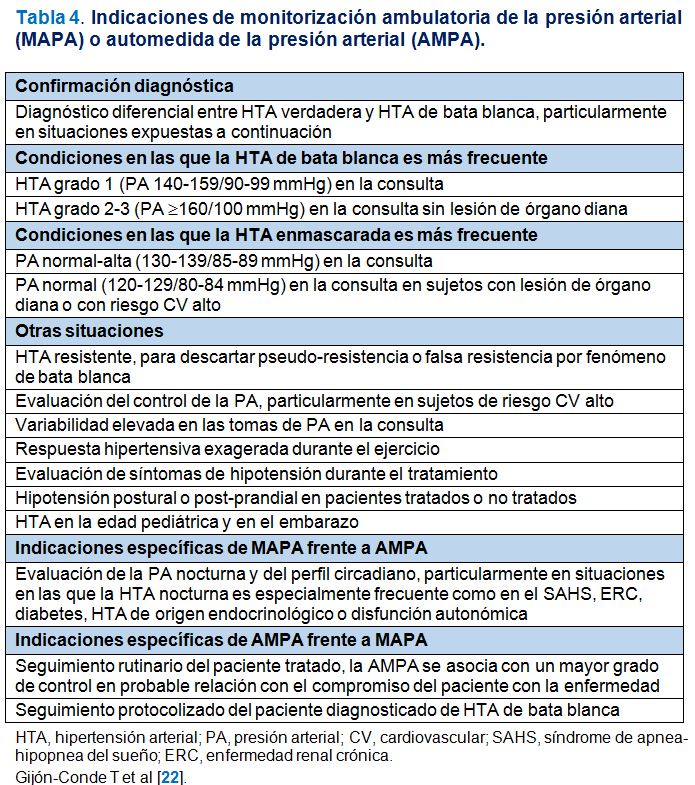
En la (Tabla 3) se exponen las condiciones básicas para una toma protocolizada de la PA en la consulta y en la (Tabla 4) se exponen las indicaciones de la MAPA y la AMPA. Además, se considera que la AMPA constituye una herramienta muy importante en el seguimiento fundamentalmente del paciente tratado. La AMPA debe indicarse de forma sistemática en el paciente tratado pues no solo aporta una información básica acerca de los niveles de PA en circunstancias normales sino que, además, favorece el control en probable relación con un mayor compromiso del paciente en el autocuidado. La AMPA debe realizarse de forma protocolizada para que constituya una herramienta útil y segura en la toma de decisiones sobre el tratamiento. El paciente debe recibir información básica acerca del procedimiento preferiblemente por escrito. En el Anexo I (Véase Figuras complementarias (Figura 9) y (Figura 10)) figura un modelo de hoja de información y de recogida de datos.
Evaluación del paciente con hipertensión arterial
Los objetivos básicos de la evaluación protocolizada de la HTA son estratificar el RCV del paciente hipertenso y detectar posibles situaciones de HTA secundaria. El protocolo inicial de estudio incluirá una historia clínica dirigida, una exploración física básica y la realización de una serie de exploraciones complementarias generales. Este protocolo de estudio servirá para cumplir los objetivos citados en una amplia mayoría de pacientes. En casos seleccionados serán necesarias exploraciones complementarias avanzadas para una mayor precisión diagnóstica tanto para estratificar el RCV como para precisar el diagnóstico de HTA secundaria.
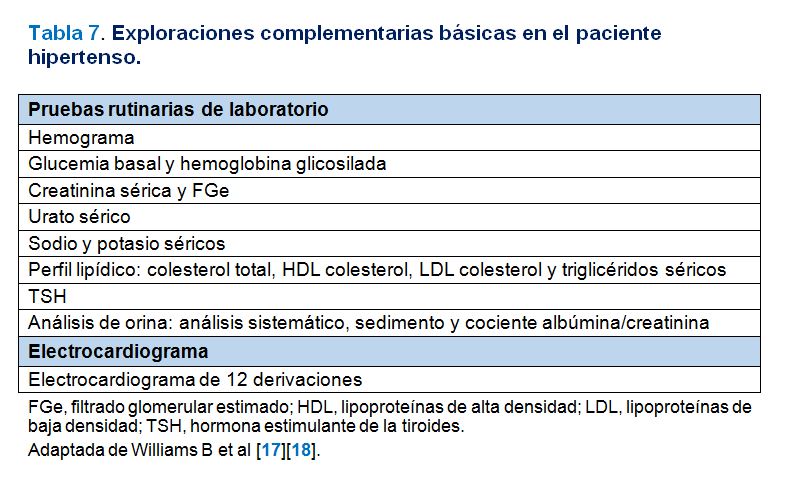
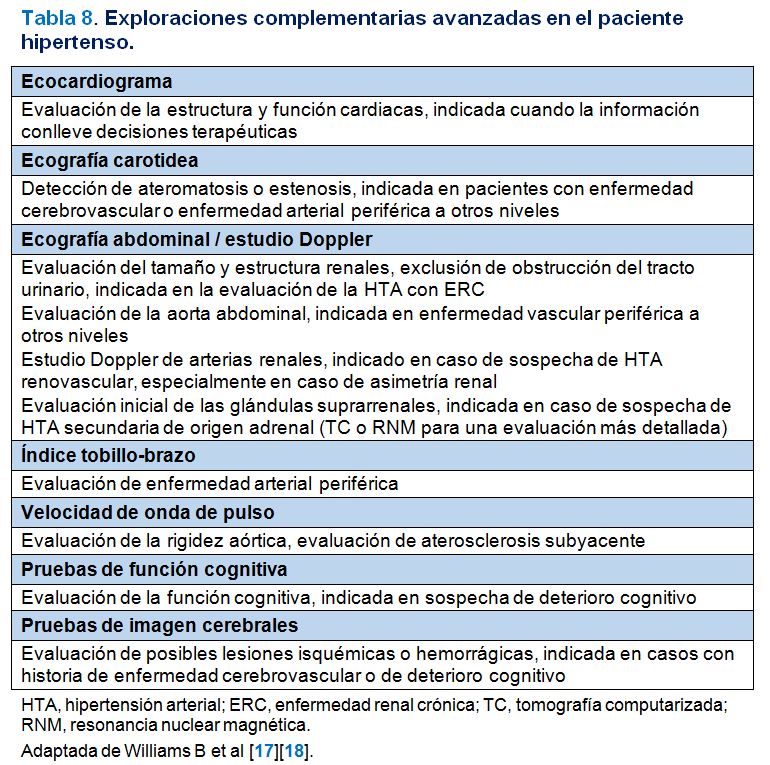
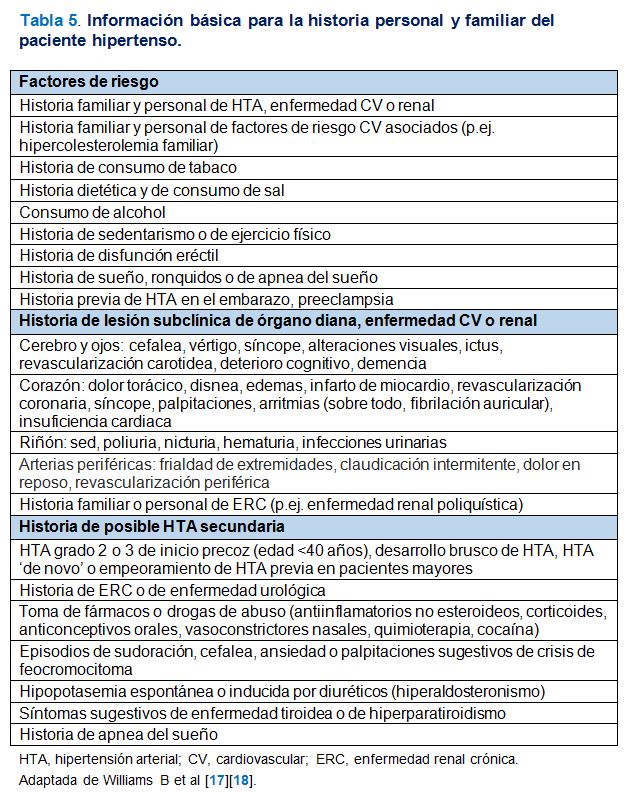
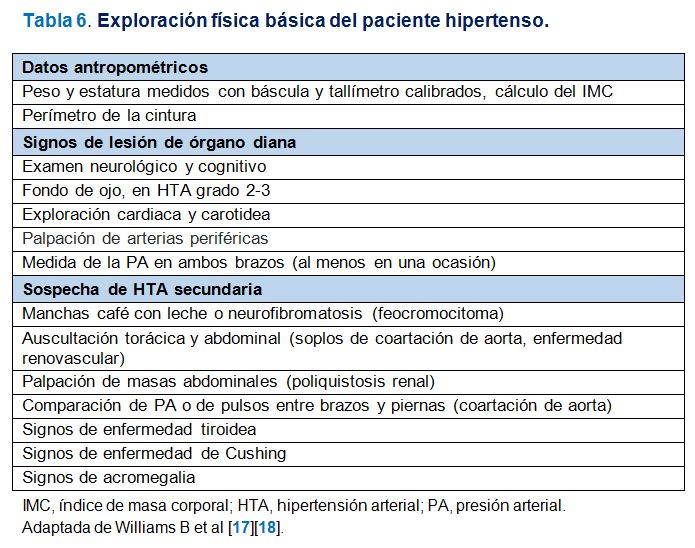
En las (Tabla 5) (Tabla 6) y (Tabla 7) se exponen la información básica a recoger en la historia personal y familiar del paciente hipertenso, la exploración física básica a realizar y las exploraciones complementarias rutinarias necesarias respectivamente. En la (Tabla 8) se exponen las exploraciones complementarias avanzadas que pueden ser útiles para una evaluación más precisa del daño vascular, particularmente para la detección de lesión subclínica en sujetos con PA normal-alta o en casos con HTA grado 1 en los que se planteen dudas acerca del inicio del tratamiento antihipertensivo farmacológico.
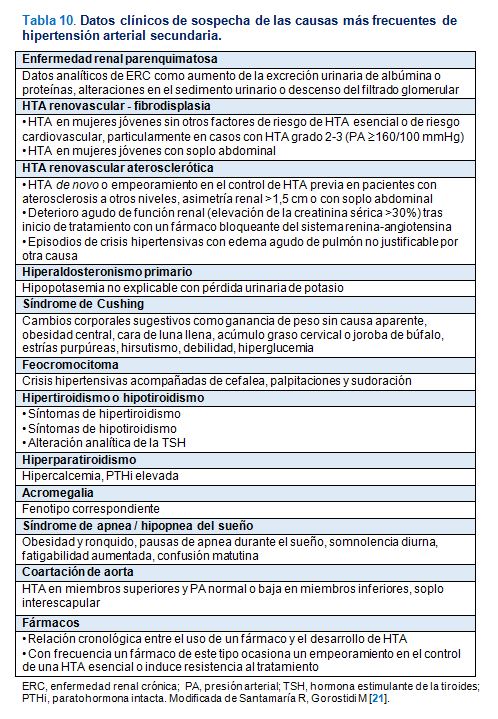
Como se ha comentado, los objetivos básicos del protocolo de estudio inicial del paciente con HTA son estratificar el riego cardiovascular del paciente hipertenso y detectar posibles situaciones de HTA secundaria. En la (Tabla 9) se exponen las situaciones clínicas de sospecha de HTA secundaria en las que estaría indicado ampliar las exploraciones complementarias para descartar una causa corregible de HTA [21]. La orientación diagnóstica de la HTA secundaria se dirigirá hacia una determinada causa o grupo de causas en función del contexto y las características clínicas de cada caso. El estudio del paciente con sospecha de HTA secundaria puede ser costoso y requerir pruebas diagnósticas invasivas no exentas de riesgos, por lo que se valorará de manera individual cada caso para realizar una búsqueda etiológica lo más selectiva posible y siempre que el diagnóstico pueda conllevar cambios en el manejo terapéutico. En la (Tabla 10) se exponen las situaciones clínicas de sospecha de las causas más frecuentes de HTA secundaria [21].
Estratificación del riesgo cardiovascular del paciente hipertenso
Tanto la guía Americana ACC/AHA 2017 [11][12] como la Europea ESC/ESH 2018 [17][18] indican la necesidad de estratificar el RCV en el paciente hipertenso y establecen esta evaluación como herramienta básica de información y de toma de decisiones terapéuticas.
La guía Americana propone el cálculo de riesgo de ASCVD (atherosclerotic cardiovascular disease) mediante una fórmula basada en una cohorte conjunta que incluye las cohortes del estudio de Framingham, del estudio ARIC (Atherosclerosis Risk in Communities) y del estudio CARDIA (Coronary Artery Risk Development in Young Adults) [30]. Esta ecuación calcula el riesgo de un evento cardiovascular mortal o no mortal en el plazo de 10 años y se basa en una serie de parámetros que incluyen la edad, el sexo, la raza, los niveles de PA sistólica y diastólica y de colesterol total, HDL y LDL, la presencia de diabetes y de tabaquismo, y el estar recibiendo o no tratamiento antihipertensivo, hipolipemiante o antiagregante [ASCVD Risk Estimator Plus]. El riesgo de ASCVD en 10 años se categoriza en bajo (< 5%), limítrofe o borderline (5 a 7,4%), intermedio (7,5 a 19,9%) y alto (= 20%). La guía ACC/AHA 2017 utiliza el umbral de riesgo de ASCVD del 10% para, por ejemplo, indicar tratamiento antihipertensivo farmacológico en casos que clasifica como HTA estadio 1 (PA 130-139/80-89 mmHg).
La guía ESC/ESH 2018 recomienda, como en ediciones previas, el uso del sistema SCORE (Systematic Coronary Risk Evaluation) [https://www.escardio.org/Education/Practice-Tools/CVD-prevention-toolbox/SCORE-Risk-Charts] que estima el riesgo de muerte cardiovascular en el plazo de 10 años utilizando como variables únicamente la edad, el sexo, la presencia o no de tabaquismo y los niveles de PA sistólica y de colesterol [31].
Las ventajas principales del sistema SCORE son que se ha desarrollado en población europea, que existen adaptaciones para diferentes áreas geográficas con riesgos diferentes (España está considerada como área de riesgo bajo) y que es de fácil aplicación. El principal inconveniente es que estima únicamente el riesgo de mortalidad por eventos cardiovasculares, y no el riesgo de eventos no mortales, estando el primero influenciado por la calidad de la atención sanitaria. La propia guía ESC/ESH reconoce esta limitación e indica que el riesgo de eventos no mortales podría corresponder al riesgo de mortalidad cardiovascular multiplicado por 3 en varones y por 4 en mujeres. El riesgo estimado mediante la fórmula SCORE se categoriza en bajo (< 1%), moderado (1 a 5%), alto (5 a 10%) y muy alto (=10%).
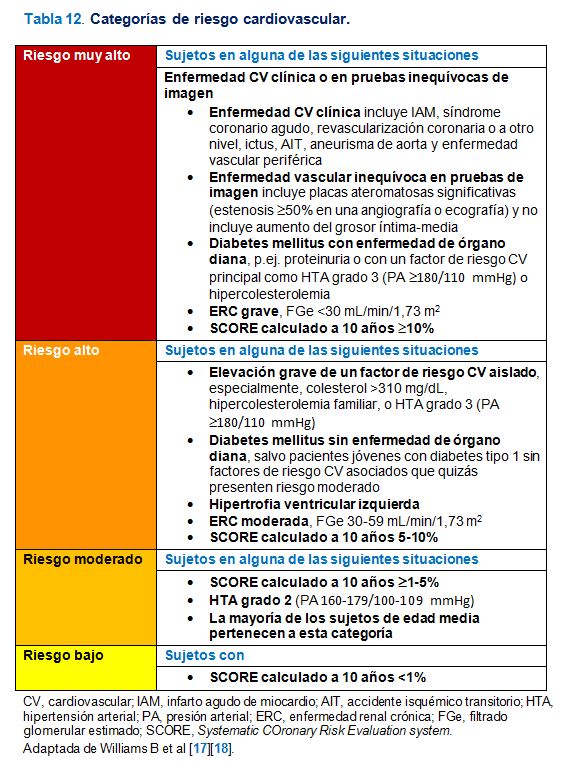
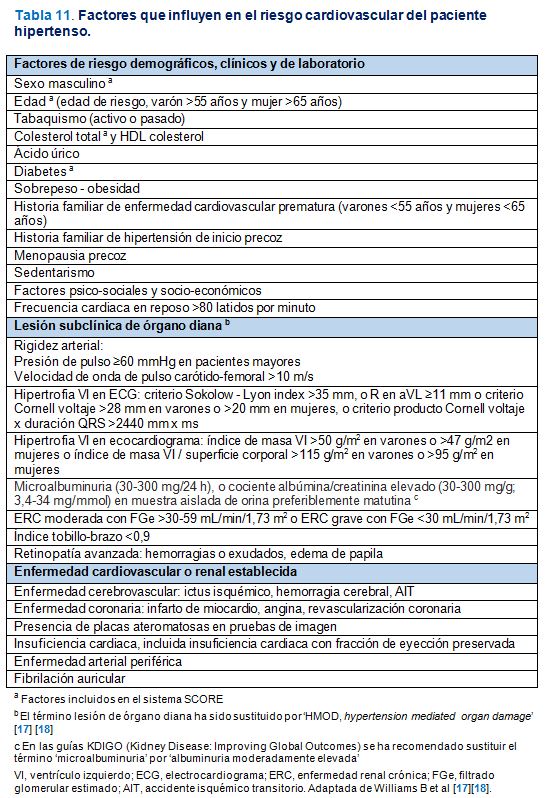
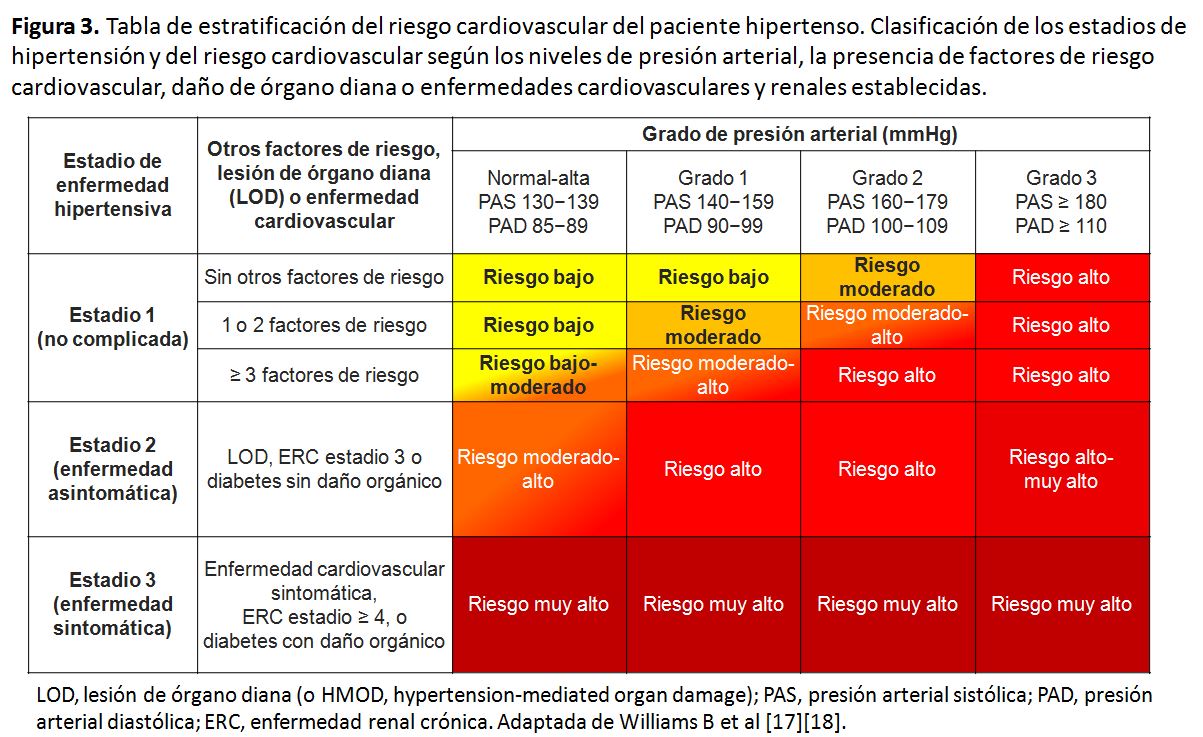
Para una evaluación más avanzada del RCV, la guía ESC/ESH 2018 mantiene la tabla de estratificación en la que se valoran más factores de riesgo que los incluidos en la ecuación SCORE y, sobre todo, se incluyen datos de daño vascular a nivel cardiaco, renal, cerebral, retiniano y vascular. Esta tabla de estratificación se expone en la (Figura 3). En este sentido, el término previo target organ damage (TOD) se sustituye por el de hypertension-mediated organ damage (HMOD). Bajo este epígrafe se siguen incluyendo, sobre todo, la presencia de hipertrofia ventricular izquierda, de enfermedad renal crónica (ERC) o de datos de rigidez arterial. En la Tabla 11 se exponen los factores de RCV, los datos de lesión subclínica de órgano diana, o las situaciones de enfermedad cardiovascular establecida que han de considerarse para llevar a cabo la estratificación. En la (Tabla 12) se exponen las situaciones clínicas básicas que conllevan los 4 grados de riesgo comentados.
Tratamiento
Las bases terapéuticas de la HTA son las modificaciones del estilo de vida (tratamiento no farmacológico) y el tratamiento farmacológico. Las modificaciones en el estilo de vida constituyen la base del tratamiento de la HTA en particular y de la prevención cardiovascular en general. Sin embargo, la mayoría de los pacientes necesitarán además tratamiento farmacológico. La evidencia acerca de la eficacia del tratamiento farmacológico en reducir la morbimortalidad relacionada con la HTA está avalada por el mayor número de ensayos clínicos aleatorizados de la medicina clínica [17][18]. El tratamiento de la HTA se ha considerado como uno de los grandes avances de la Medicina de las últimas décadas [32]. Los metanálisis de ensayos clínicos aleatorizados que han incluido varios cientos de miles de pacientes indican que una reducción de 10 mmHg en la PA sistólica o de 5 mmHg en la PA diastólica conlleva una reducción en torno a un 10-15% en la mortalidad, un 20% en complicaciones cardiovasculares mayores, un 35% en ictus, el 40% en insuficiencia cardiaca y un 20% en eventos coronarios [33][34]. Estas reducciones de riesgo se han observado de forma consistente e independiente en cualquier grado de HTA, y en cualquier grado de RCV, y en cualquier edad, sexo, raza o comorbilidad [33][35].
Inicio del tratamiento
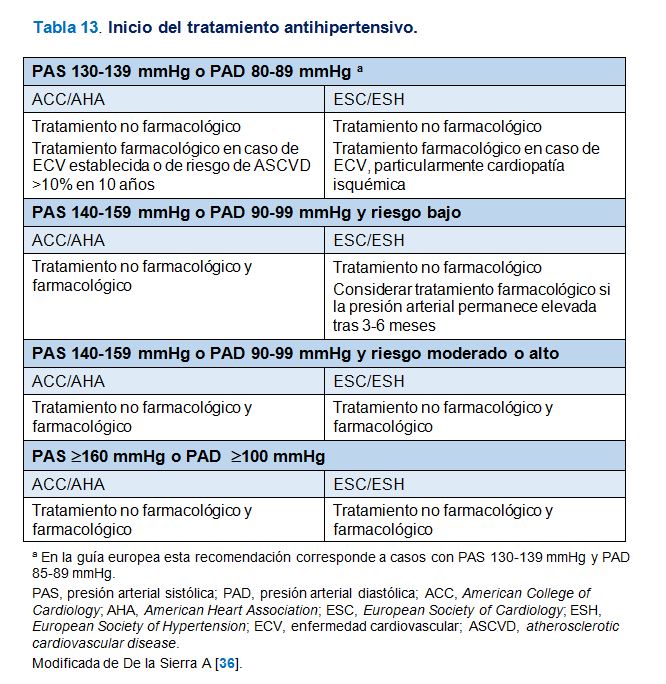
En la (Tabla 13) se resumen las recomendaciones de la guía Americana ACC/AHA 2017 y de la Europea ESC/ESH 2018 acerca de cuándo iniciar, y con qué estrategia (no farmacológica o no farmacológica y farmacológica), el tratamiento de la HTA [11][12][17][18][36]. En nuestro medio el inicio con tratamiento únicamente no farmacológico se recomienda sólo en casos de HTA grado 1 y RCV en los niveles más bajos. En todas las demás circunstancias (HTA grados 2 o 3, y HTA grado 1 con RCV elevado, particularmente en casos con lesión de órgano diana) se indicará inicio simultáneo de modificaciones del estilo de vida y de tratamiento farmacológico. Además, como se expondrá más adelante, se valorará sistemáticamente el inicio de tratamiento farmacológico con una combinación de 2 fármacos a dosis bajas o iniciales. Esta estrategia se aplicará cuando la PA esté 20/10 mmHg o más elevada por encima del objetivo, lo que supone una PA ?150/90 mmHg en la mayoría de los pacientes. El tratamiento farmacológico también se indicará en HTA grado 1 y RCV bajo cuando tras 3-6 meses de tratamiento no farmacológico no se consiga un control adecuado.
Objetivos
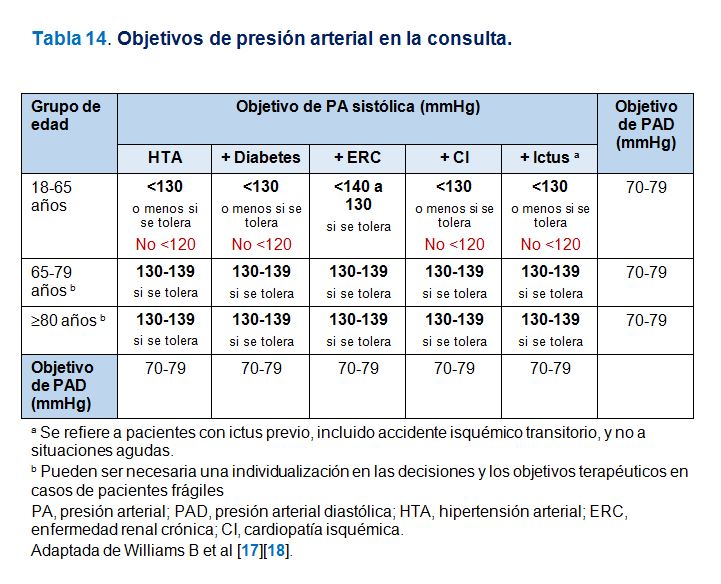
La publicación de nuevos estudios y metanálisis [7][8][9][10][33][37] ha llevado planteamientos de control más estrictos. La guía ACC/AHA 2017) recomienda un objetivo de PA < 130/80 mmHg para todos los pacientes hipertensos [11][12]. Se considera esta recomendación como ‘mandatoria’ para todos los casos de riesgo alto (pacientes con enfermedad cardiovascular establecida o con riesgo de ASCVD > 10%) y ‘razonable’ para pacientes de riesgo menor. La guía ESC/ESH 2018 establece unas recomendaciones más individualizadas con respecto a los objetivos en base principalmente a la edad del paciente. La recomendación general será reducir inicialmente la PA por debajo de 140/90 mmHg para, a continuación y si el tratamiento es bien tolerado, establecer el objetivo de una PA < 130/80 mmHg. En los pacientes de más edad se considera ‘razonable’ mantener el objetivo de PA sistólica entre 130 y 140 mmHg [17][18]. En la (Tabla 14) se exponen los objetivos de control de la HTA de la guía ESC/ESH 2018. El objetivo de control < 140/80 mmHg recomendado para pacientes con ERC puede ser insuficiente. En las próximas guías KDIGO (Kidney Disease: Improving Global Outcomes) muy probablemente se recomiende un control < 130/80 mmHg o incluso más estricto para un amplio espectro de pacientes con ERC [38]. Se ha considerado que las recomendaciones sobre objetivos de las guías ACC/AHA 2017 y ESC/ESH son similares, siendo la perspectiva de la primera más general, pragmática y concisa y la de la segunda más individualizada y prudente para prevenir el posible efecto deletéreo de un exceso de reducción de la PA particularmente en pacientes mayores o frágiles [36].
Tratamiento no farmacológico
El estilo de vida saludable puede prevenir o retrasar la aparición de la HTA y puede reducir en sí el RCV [39]. Las modificaciones en el estilo de vida pueden ser suficientes para retrasar o incluso prevenir el tratamiento farmacológico en pacientes con HTA grado 1 y un perfil bajo de RCV. En los pacientes en los que está indicado el tratamiento farmacológico las modificaciones en el estilo de vida pueden optimizar el efecto antihipertensivo de los fármacos y pueden ser eficaces en la prevención cardiovascular global. La indicación de hábitos de vida saludable debe llevarse a cabo de forma sistemática en todos los pacientes con HTA y el cumplimiento de los mismos debe reforzarse en el seguimiento. Las modificaciones del estilo de vida eficaces para controlar la HTA son la reducción del contenido de sal, el control del exceso de peso, la práctica de ejercicio físico, el seguimiento de una dieta saludable, no fumar y restringir el consumo de alcohol. Estos cambios en el estilo de vida no son sólo eficaces como tratamiento antihipertensivo sino que constituyen medidas de prevención cardiovascular y de enfermedad en general [11][12][17][18][39]. En la (Tabla 15) se exponen y detallan estas modificaciones del estilo de vida.
Tratamiento farmacológico
La mayoría de los pacientes con HTA requieren tratamiento farmacológico además de tratamiento no farmacológico con modificaciones del estilo de vida. Al igual que en recomendaciones precedentes, las guías europeas ESC/ESH 2018 continúan considerando como primera línea para el tratamiento antihipertensivo a cinco tipos de fármacos: 1) inhibidores del enzima de conversión de la angiotensina (IECA), 2) antagonista de los receptores de la angiotensina II (ARA II), 3) beta-bloqueantes (BB), 4) calcioantagonistas (CA), y 5) diuréticos (diuréticos tiazídicos y similares a tiazídicos como clortalidona o indapamida). La eficacia de estos tipos de fármacos para reducir la PA y para reducir la morbimortalidad asociada a la HTA ha sido demostrada de forma indiscutible en múltiples ensayos clínicos [17][18][33][40][41]. El debate acerca de qué tipo concreto de fármaco ha de constituir la primera elección ha ido perdiendo fuerza en base a dos hechos evidentes como son que el beneficio del tratamiento se basa en la reducción en sí de la PA y que una amplia mayoría de pacientes hipertensos necesitan una combinación de fármacos para conseguir el control adecuado.
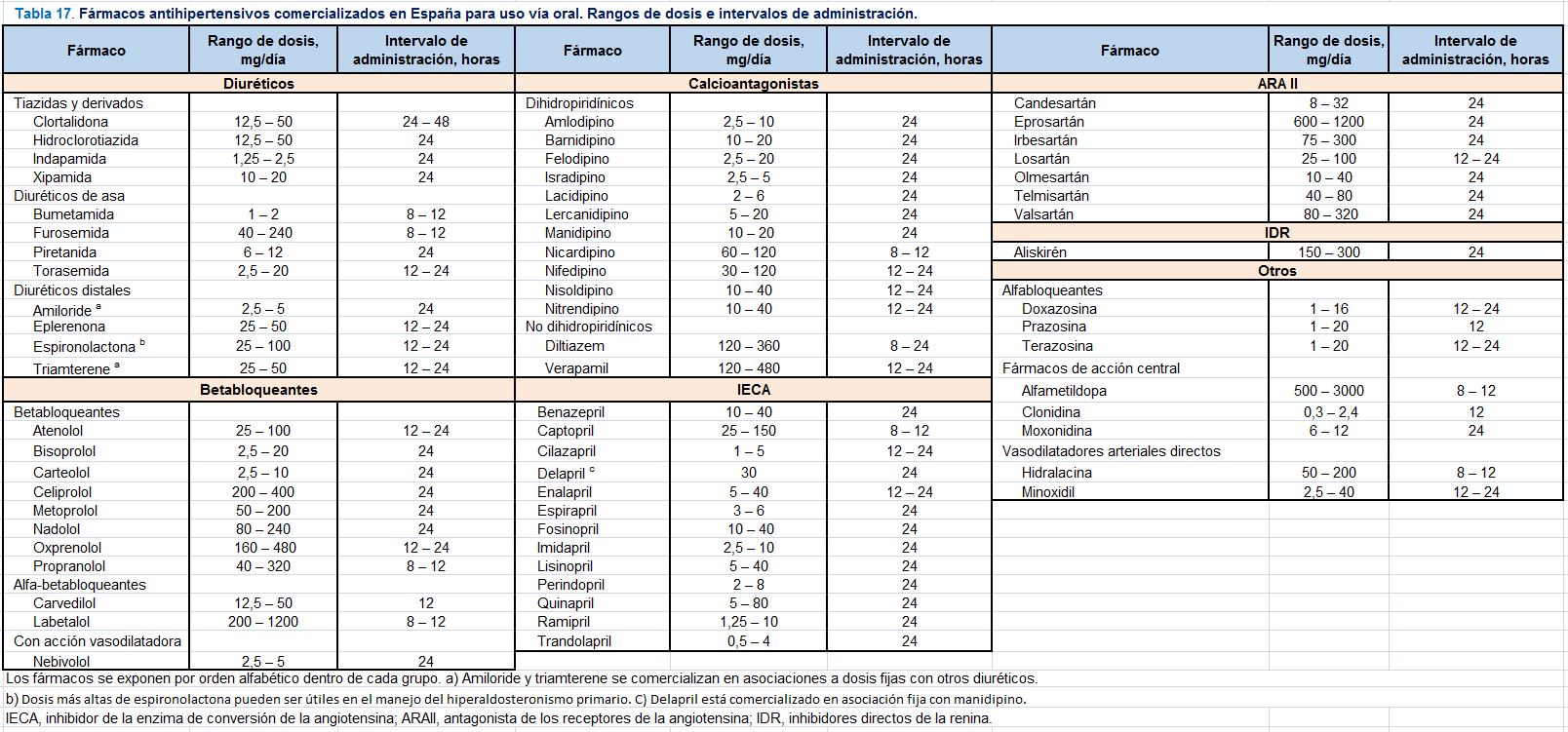
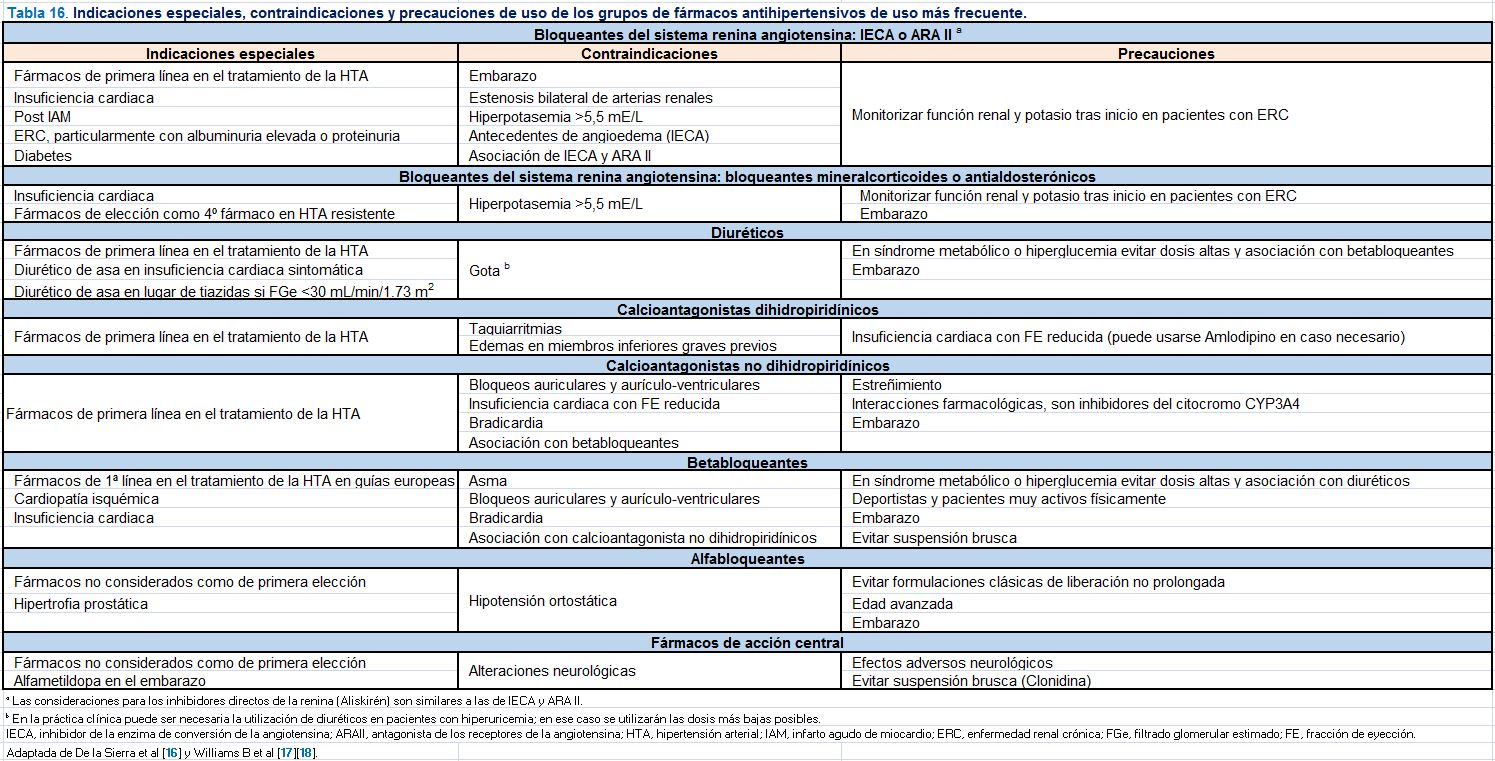
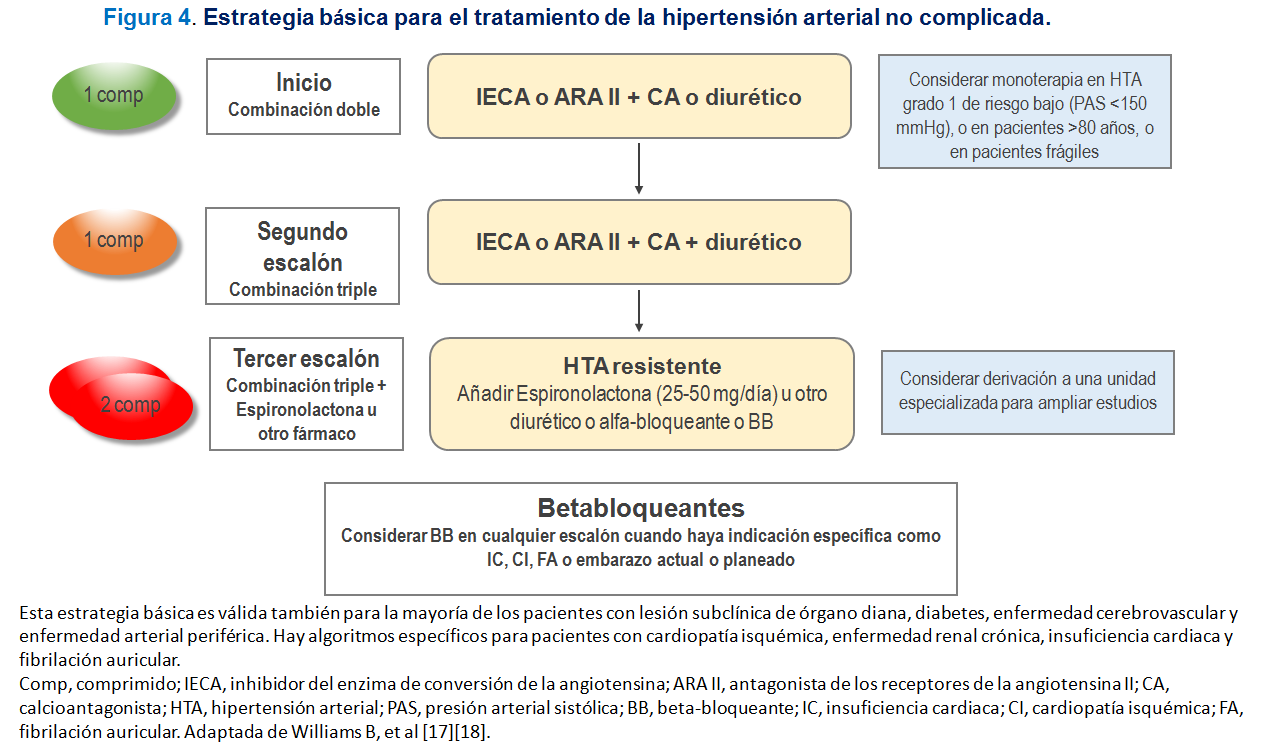
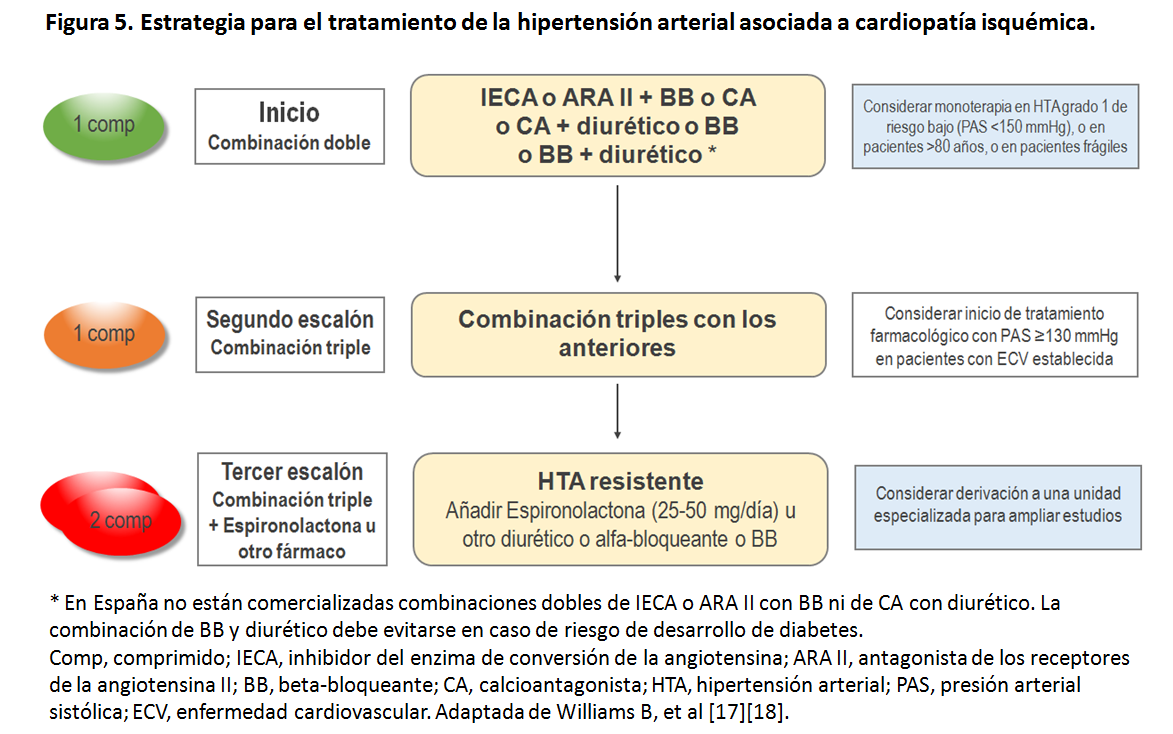
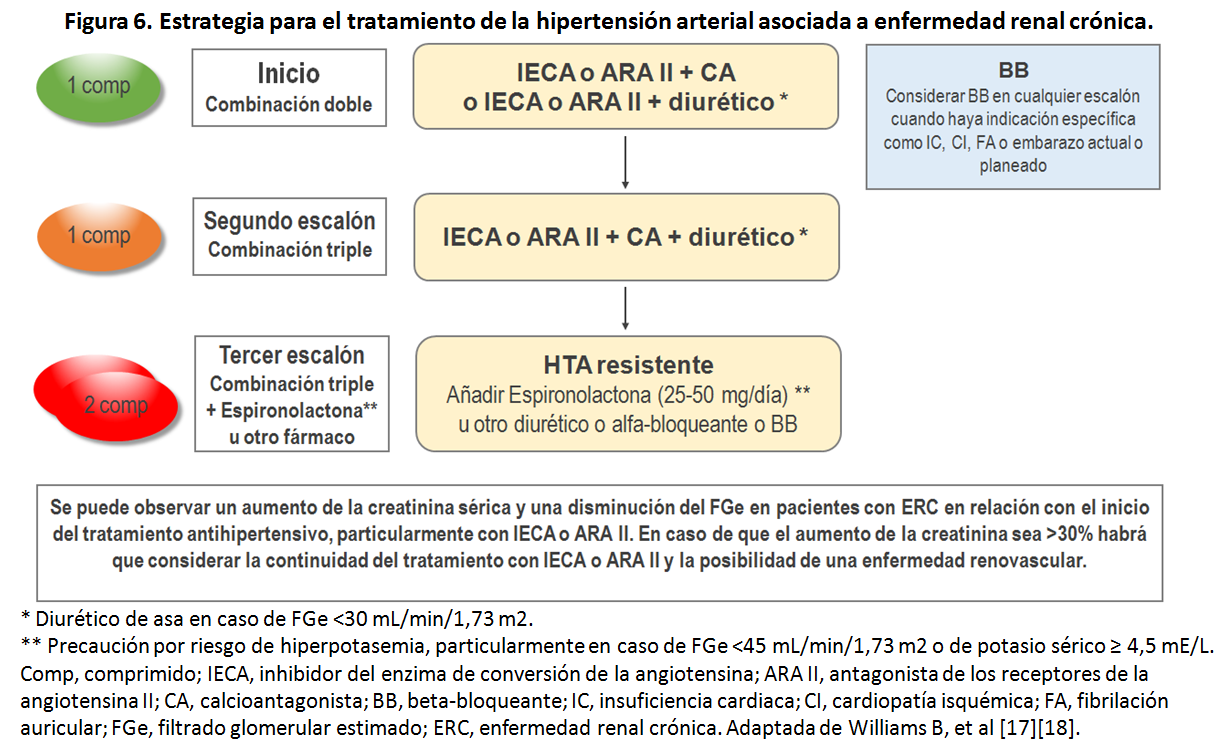
La elección del primer fármaco a utilizar será individualizada y basada en el perfil de indicaciones especiales, contraindicaciones y precauciones a tener en cuenta de los distintos grupos de fármacos antihipertensivos si bien las estrategias básicas para el tratamiento de la HTA incluyen la recomendación del inicio de tratamiento combinado en un amplio número de situaciones clínicas. En la (Tabla 16) se exponen y detallan estas consideraciones y en la (Tabla 17) se exponen los fármacos antihipertensivos comercializados en España con los correspondientes rangos de dosis y periodos de administración. En la (Figura 4) se exponen la estrategia básica para el tratamiento de la HTA no complicada y en la (Figura 5) (Figura 6) (Figura 7) y (Figura 8) se exponen las estrategias para el tratamiento antihipertensivo en pacientes con cardiopatía isquémica, ERC, insuficiencia cardiaca con fracción de eyección reducida y fibrilación auricular, respectivamente. La estrategia básica para el tratamiento de la HTA no complicada (Figura 4) se considera también indicada para la mayoría de los pacientes con lesión subclínica de órgano diana, diabetes, enfermedad cerebrovascular y enfermedad arterial periférica [17][18][42].
Tratamiento combinado como estrategia inicial
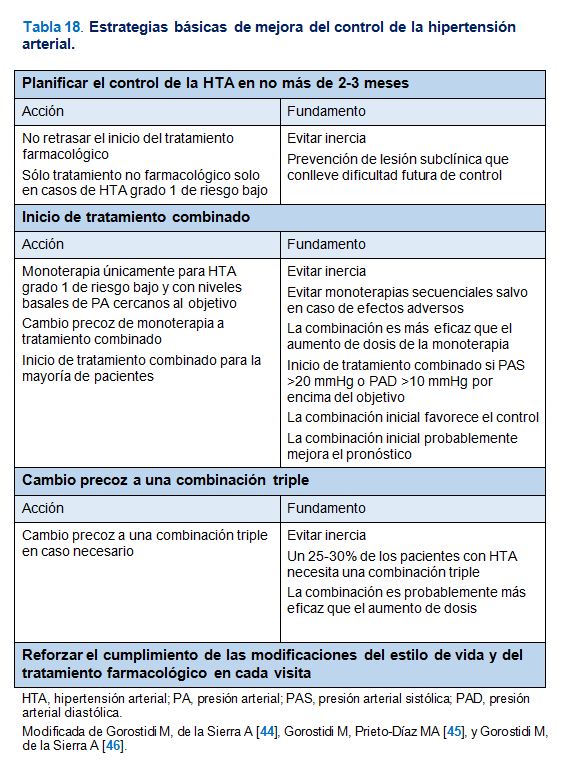
Como se ha comentado, en la mayoría de los pacientes con HTA será necesaria la combinación de dos o más fármacos para conseguir un control adecuado, particularmente teniendo en cuenta la recomendación actual de un objetivo de control < 130/80 mmHg aplicable a un amplio porcentaje de casos. El tratamiento combinado de inicio es más eficaz para conseguir el control, incluso a dosis menores que las utilizadas en monoterapia al implicar a distintos mecanismos fisiopatológicos de acción. Además, el inicio de tratamiento combinado con una combinación de dos fármacos es seguro y bien tolerado [43][44][45][46]. El inicio de tratamiento con una combinación forma parte de las estrategias clave para la mejora del control de la HTA que se resumen en la (Tabla 18).
Hipertensión arterial resistente
La HTA resistente se define como una HTA que no se controla con una pauta de 3 fármacos a dosis óptimas, de acción sinérgica, e incluyendo un diurético. El esquema habitual, o más frecuentemente indicado como se ha expuesto en las (Figuras 4) (Figura 5) (Figura 6) (Figura 7) y (Figura 8) incluye un IECA o un ARA II, un calcioantagonista y un diurético [17][18][47]. El término HTA refractaria se reservará para las situaciones en las que la HTA no se controla con una pauta de 5 fármacos antihipertensivos [48]. En la guía Europea se utiliza en umbral de ? 140/90 mmHg para la definición de falta de control mientras que en la guía Americana se define la HTA resistente con el umbral ? 130/80 mmHg. Se estima que la prevalencia de HTA resistente se sitúa en torno al 15%.
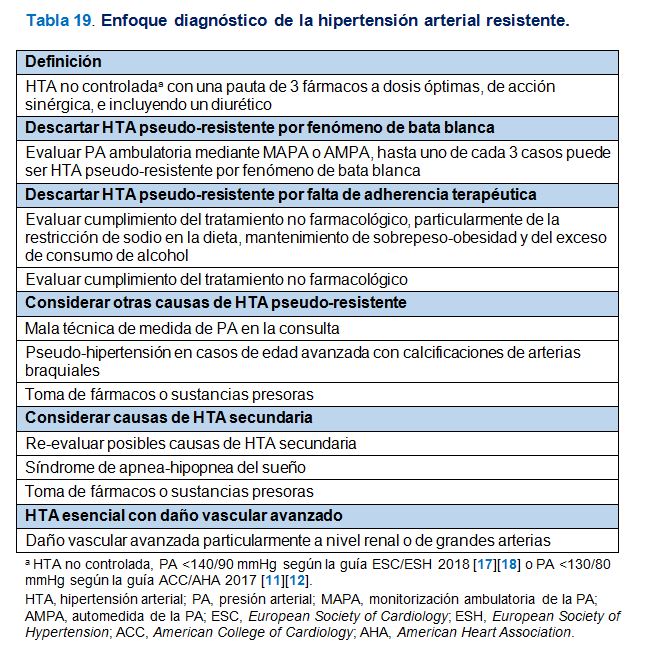
Respecto al enfoque diagnóstico, los primeros pasos se dirigirán a descartar una pseudo-resistencia, particularmente por fenómeno de bata blanca y por falta de adherencia terapéutica. Uno de cada 3 pacientes con HTA resistente y uno de cada 4 pacientes con HTA refractaria puede presentar una PA ambulatoria adecuadamente controlada y ser, por tanto, casos de falsa resistencia al tratamiento [49][50]. La falta de adherencia al tratamiento no farmacológico o farmacológico constituye otra causa frecuente de pseudo-resistencia. Otras causas de pseudo-resistencia son la toma incorrecta de la PA y la pseudo-hipertensión del anciano por calcificación de la arteria braquial. Una vez descartadas situaciones de pseudo-resistencia, se valorará que la HTA sea resistente por una causa de HTA secundaria que hasta ese momento no se haya diagnosticado. En este sentido, las situaciones más frecuentes son la enfermedad renal parenquimatosa, la enfermedad renovascular, el hiperaldosteronismo primario, el síndrome de apnea-hipopnea del sueño y la HTA inducida por fármacos o drogas. Por último, una HTA esencial con daño vascular avanzado, particularmente a nivel renal y de grandes arterias, constituye otra situación frecuente de HTA resistente. En la (Tabla 19) se exponen las principales causas de HTA pseudo-resistente y resistente y el enfoque diagnóstico básico de estas situaciones.
Conclusiones finales
La HTA constituye el principal factor de riesgo de enfermedad y muerte en el mundo pero el control adecuando del paciente hipertenso reduce de forma indiscutible el riesgo relacionado con la PA. Los principales puntos de atención a la HTA se han resumido en el siguiente decálogo [51]:
1) La HTA se define en nuestro medio como unas cifras en la consulta de PA sistólica =140 mmHg o de PA diastólica =90?mmHg de forma persistente, que son equivalentes a una PA media en la MAPA =130/80?mmHg o una PA media en la AMPA =135/85?mmHg.
2) Deben establecerse programas de despistaje para que la PA se mida en adultos al menos cada 5 años y de forma más frecuente en individuos con PA normal-alta. Cuando se detecte HTA se procederá a su confirmación mediante repetición de la medida en la consulta de forma protocolizada o mediante técnicas de medida de la PA ambulatoria, MAPA o AMPA.
3) El tratamiento antihipertensivo farmacológico se indicará en adultos hasta los 80 años con HTA grado 1 con riesgo asociado bajo cuando no se controle con modificaciones del estilo de vida y en casos con HTA grado 1 con riesgo más elevado y en casos de HTA grado =2. Las modificaciones del estilo de vida se indicarán en todos los pacientes con HTA.
4) En pacientes > 80 años o en situaciones de fragilidad el inicio del tratamiento de considerará con PA sistólica =160?mmHg. En pacientes tratados que sobrepasen esta edad no se considerará la retirada del tratamiento únicamente por el criterio edad.
5) El objetivo de control general será una PA < 130/80 mmHg en la mayoría de los pacientes. En pacientes de edad avanzada y en casos de mala tolerancia dichas cifras se considerará el objetivo de PA < 140/80 mmHg. En pacientes jóvenes < 65 años se considerará un objetivo se PA sistólica entre 120 y 130 mmHg.
6) La indicación de modificaciones del estilo será sistemática en todo paciente hipertenso. La restricción del contenido de sal en la dieta, el control del exceso de peso, la dieta saludable, el cese de hábito tabáquico y el consumo restringido de alcohol son medidas con un impacto en la salud que trasciende su capacidad antihipertensiva.
7) Se considerará el inicio de tratamiento antihipertensivo combinado en la mayoría de los pacientes. Únicamente casos con PA basal cercana a los objetivos se controlarán con monoterapia. La monoterapia inicial también se indicará en pacientes frágiles o de edad muy avanzada.
8) El tratamiento antihipertensivo combinado se basará con una estrategia de un solo comprimido tanto cuando se administren 2 o 3 fármacos. La estrategia de tratamiento combinado en un solo comprimido favorece el cumplimiento y el control de la HTA.
9) El algoritmo de tratamiento basado en una combinación de IECA o ARA II con un CA o un diurético es útil para una amplia mayoría de pacientes. En los casos que necesiten 3 fármacos la combinación preferible es la de IECA o ARA II con CA y con diurético. Los BB se utilizarán es casos de indicación específica como cardiopatía isquémica, insuficiencia cardiaca con fracción de eyección reducida o cuando es necesario un control de la frecuencia cardiaca.
10) El tratamiento antihipertensivo forma parte del manejo integral del RCV del paciente hipertenso. Con frecuencia serán necesarios otros fármacos de probada eficacia en prevención cardiovascular como estatinas, fármacos antiagregantes e hipoglucemiantes.