Diagnóstico por Biopsia de Enfermedad de Fabry ante Estudio Genético Dudoso
Palabras clave
Enfermedad hereditaria ligada a X, alfa-galactosidasa A, déficit enzimático
INTRODUCCIÓN
La enfermedad de Fabry (EF) es una enfermedad hereditaria ligada a X, producida por el déficit de alfa-galactosidasa A, que ocasiona el depósito intracelular de glucoesfingolípidos en distintos tejidos y órganos. El déficit enzimático severo cursa con manifestaciones clínicas desde la infancia: acroparestesias, dolor neuropático en pies y manos, angioqueratomas, hipohidrosis, síntomas gastrointestinales, problemas corneales y auditivos, etc. Además, hacia la tercera década de la vida, afecta a corazón, riñón y sistema nervioso central [1].
La existencia de una expresión clínica variable con formas incompletas de la enfermedad hace que muchos pacientes sean difíciles de diagnosticar. Sin embargo, el diagnóstico precoz y la aplicación temprana de un tratamiento sustitutivo enzimático (TSE) son importantes para prevenir el daño orgánico y mejorar la supervivencia [1] [2]. A continuación, se expone el caso clínico de un paciente con diagnóstico de EF por biopsia renal.
Para tema completo Véase Nefropatía por Enfermedad de Fabry
CASO CLÍNICO
Varón de 41 años, sin antecedentes de interés: no hipertenso ni diabético. En mayo-2018, es remitido a cardiología por complejo QRS con onda R de alto voltaje en electrocardiograma. En la ecocardiografía, se objetiva una miocardiopatía hipertrófica apical no obstructiva de 18 mm. En la resonancia magnética nuclear cardíaca: miocardiopatía hipertrófica de distribución asimétrica y sin fibrosis. Su familia está en Marruecos, pero aporta informes de su madre con miocardiopatía hipertrófica. Sin antecedentes de nefropatía familiar.
En analítica de julio-2018, presenta: creatinina 1,3 mg/dl, filtrado glomerular 68 ml/min, proteinuria 1,27 gr/d, albuminuria 1,17 g/d, sin hematuria, resto normal. Ante estos hallazgos de deterioro de la función renal y proteinuria es remitido a nefrología. Previamente, en 2013: creatinina 0,98 mg/dl, sin proteinuria; y en 2015: proteinuria 75 mg/ml. En ecografía renal: riñones normales, sin hidronefrosis. Inmunología y serología normales.
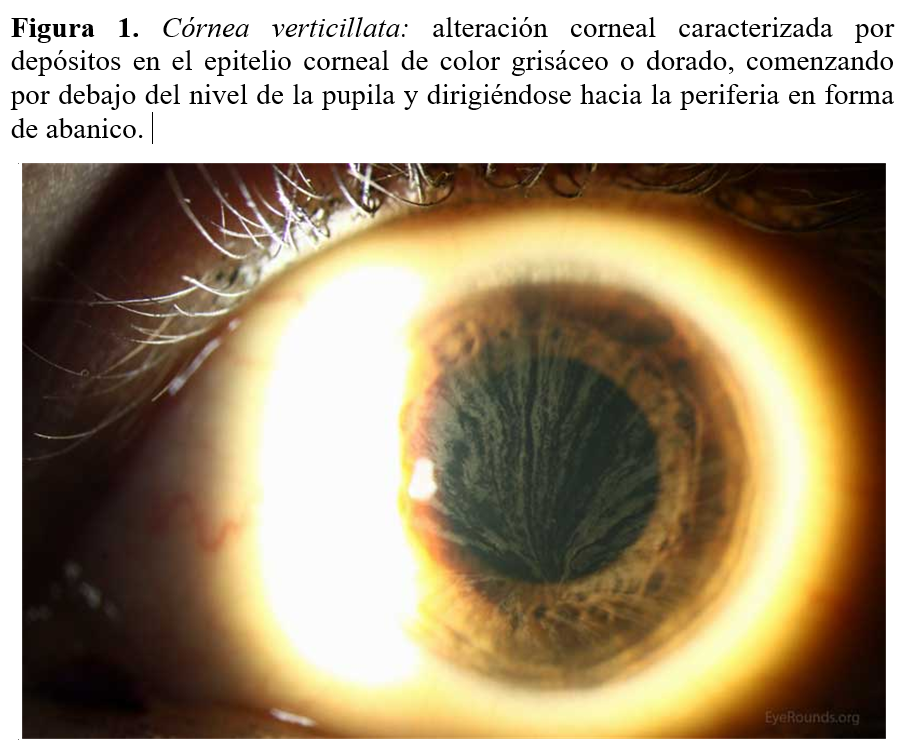
En la anamnesis dirigida destacan: acroparestesias leves desde hace años e hipohidrosis. No presenta lesiones dermatológicas. En la exploración oftalmológica: córnea verticillata (Figura 1).
Ante la sospecha de EF, se solicita alfa-galactosidasa A que fue baja: 0,4 mmol/l/h (VN: 2,4-10,2). En el estudio genético, se encontró una variante de significado clínico incierto del gen GLA no descrita previamente: Tyr200Asn, identificada como posible causa, pero sin poder confirmar el diagnóstico.
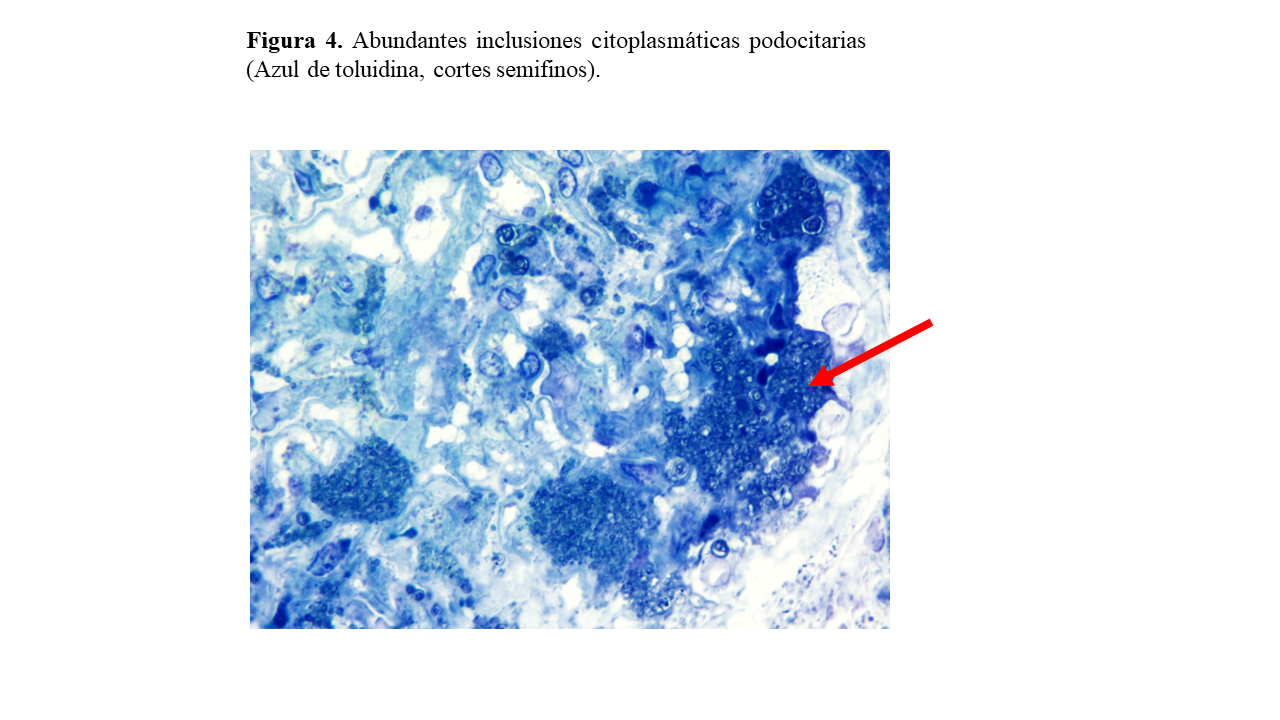
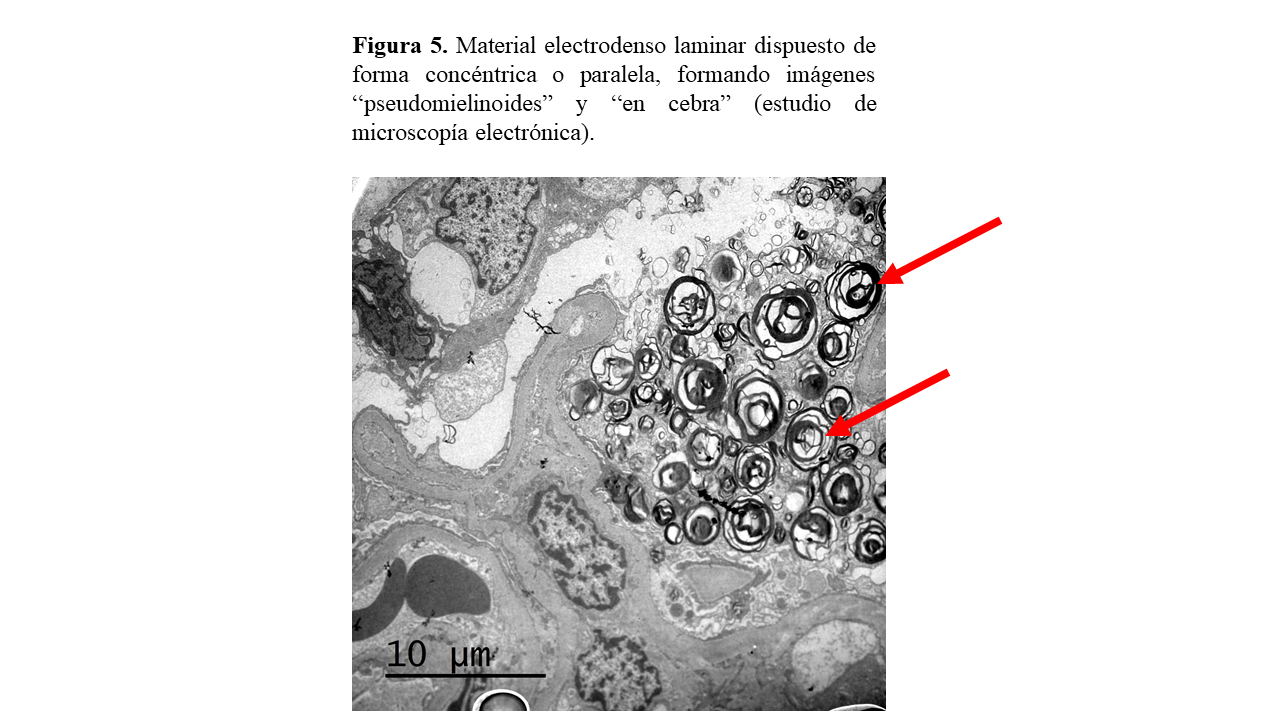
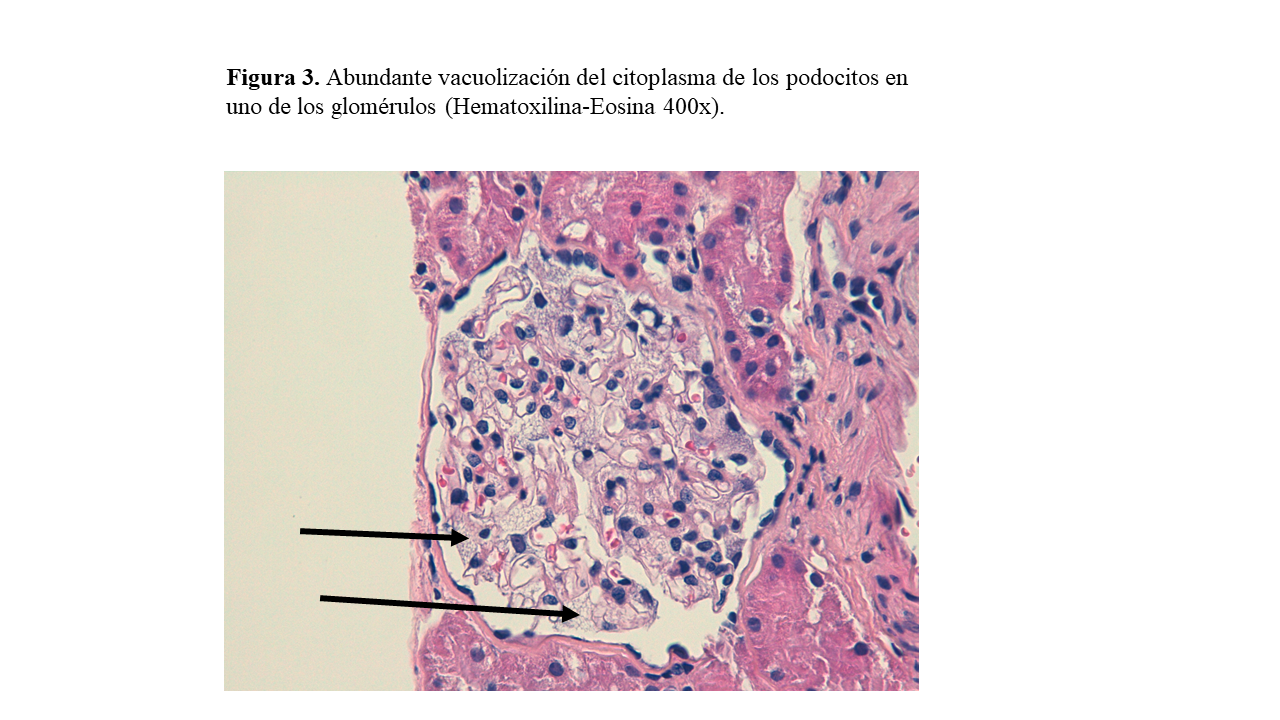
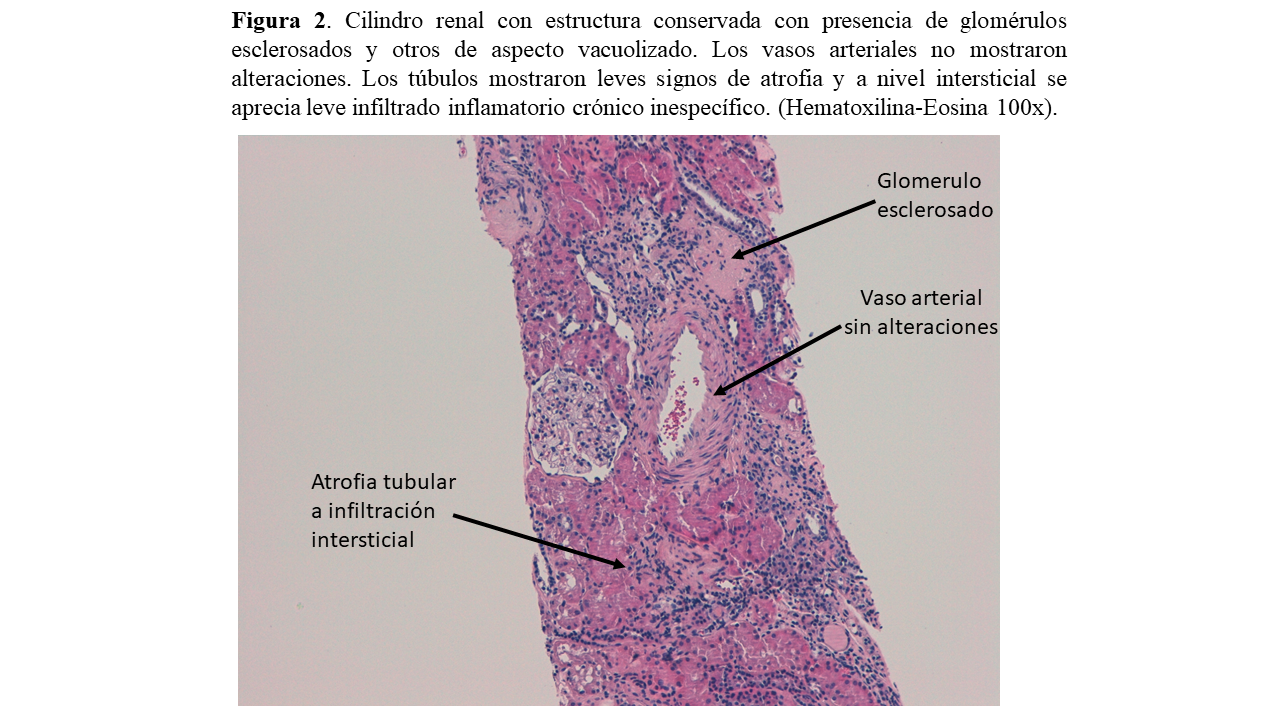
Ante la importancia de un diagnóstico definitivo de enfermedad hereditaria, tanto por las implicaciones para sus hijos como para el paciente por el tratamiento enzimático sustitutivo, se realiza biopsia renal en la que se observó: glomérulos con citoplasmas podocitarios microvacuolados y posible afectación de alguna célula mesangial, además de un glomérulo con esclerosis segmentaria y focal y otros con esclerosis global. No existían datos de daño crónico tubulointersticial (Figura 2) (Figura 3) (Figura 4). En la inmunofluorescencia a nivel glomerular la positividad de C3 e IgM en lesiones de aspecto cicatricial/segmentaria fue débil y focal; IgA, IgG, C1q, kappa, lambda, fibrinógeno y albúmina fueron negativos. En el estudio ultraestructural o de microscopía electrónica se observaron glomérulos con abundantes inclusiones podocitarias, de material electrodenso laminar, dispuesto en forma concéntrica y paralela “en cebra”, compatible con Enfermedad de Fabry (Figura 5).
El paciente inicia tratamiento con lisinopril 5 mg/día y tratamiento enzimático sustitutivo (agalsidasa beta 75 mg iv cada 15 días), con desaparición de las acroparestesias, mejoría de la proteinuria y función renal estable. En analítica de julio-2020: creatinina 1,1 mg/dl, filtrado glomerular 82 ml/min, proteinuria 0,73 g/d, albuminuria 523 mg/d.
COMENTARIOS
La EF es una enfermedad de depósito hereditaria que afecta a diversos tejidos y órganos. En el riñón se encuentran depósitos en podocitos, mesangio y endotelio capilar glomerular, pero también puede haber en epitelio tubular, células endoteliales, capa muscular de arterias y arteriolas y en células intersticiales. De manera progresiva, se produce esclerosis glomerular, lesiones vasculares y fibrosis intersticial. Clínicamente, se manifestará con proteinuria e insuficiencia renal progresiva, acompañadas de hipertensión arterial. Hasta un 20% de los casos, pueden desarrollar proteinuria en rango nefrótico [1].
Debido a una expresión clínica variable, muchos pacientes son difíciles de diagnosticar, existiendo un retraso de varios años desde la presentación de los síntomas hasta el diagnóstico de la enfermedad. Sin embargo, el diagnóstico precoz permitiría la aplicación temprana de TSE, para evitar o retrasar la progresión de la nefropatía y prevenir complicaciones extrarrenales. Aunque la base del diagnóstico se centra en un adecuado enfoque clínico que permita sospechar la enfermedad (identificación del patrón clínico de afectación renal, realización del árbol familiar, así como manejo multidisciplinar) [3]. El método diagnóstico recomendado en la actualidad consiste en detectar una baja actividad enzimática de alfa-galactosidasa A, confirmando posteriormente mediante secuenciación genética del gen de la alfa-galactosidasa A (GLA) [1] [2]. Se han identificado más de mil mutaciones en el gen GLA, existiendo además multitud de variantes genéticas de patogenicidad dudosa [4] [5], tal y como ocurrió en el caso de nuestro paciente, que precisó la realización de una biopsia renal para el diagnóstico definitivo de la enfermedad. La biopsia, además, sería útil para establecer la gravedad de la enfermedad, así como para descartar otras lesiones glomerulares asociadas [1].
La proteinuria mayor de 1 g/d y el descenso del FG en el momento del diagnóstico son factores predictores negativos de progresión y de respuesta al tratamiento. De ahí, la necesidad de iniciar tratamiento precozmente. Existen 2 pilares básicos de tratamiento: 1) Control óptimo de la tensión arterial y tratamiento antiproteinúrico; y 2) TSE.
De acuerdo con las últimas guías (Véase Recommendations for initiation and cessation of enzyme replacement therapy in patients with Fabry disease: the European Fabry Working Group consensus document (nih.gov)), el tratamiento enzimático sustitutivo debe iniciarse tanto en formas clásicas como no clásicas de la enfermedad, tan pronto como aparezcan síntomas o signos de afectación orgánica, tal y como se procedió en el paciente de nuestro caso clínico. Disponemos de 2 formas de sustitución enzimática: 1) agalsidasa alfa, a dosis de 0,2 mg/Kg administrada cada 14 días en infusión de 40 min; y 2) agalsidasa beta, a dosis de 1 mg/Kg administrada cada 14 días en infusión de 120 min.
REFERENCIAS BIBLIOGRÁFICAS
1. Jaurretche S, Antongiovanni N, Perretta F. Fabry nephropathy. Role of nephrologist and clinical variables associated with the diagnosis. Nefrologia (Engl Ed). 2019 May-Jun;39(3):294-300. English, Spanish. doi: 10.1016/j.nefro.2018.10.017. Epub 2019 Mar 16. PMID: 30890379.
2. Mauer, Michael, et al. Fabry disease: Clinical features and diagnosis. UpToDate [Internet]. Waltham (MA): UpToDate Inc (2019).
3. Barbeito-Caamaño, C., Cao-Vilariño, M., Mosquera-Reboredo, J., García-Pavía, P., Monserrat-Iglesias, L., & Barriales-Villa, R. (2018). La variante p. Arg118Cys en el gen GLA no causa enfermedad de Fabry. Más evidencias. Rev. esp. cardiol.(Ed. impr.), 871-873.
4. Barbeito-Caamaño, C., Cao-Vilariño, M., Mosquera-Reboredo, J., García-Pavía, P., Monserrat-Iglesias, L., & Barriales-Villa, R. (2018). La variante p. Arg118Cys en el gen GLA no causa enfermedad de Fabry. Más evidencias. Rev. esp. cardiol.(Ed. impr.), 871-873.
5. Ars E. Nefrología al día. Enfoque Genético de las Enfermedades Renales Hereditarias. Disponible en: https://www.nefrologiaaldia.org/359. Consultado 28 Nov 2021.