Enfermedad Renal en Pacientes con Trasplante de Órgano Sólido No Renal (TOSNR)
AUTORES
Manuel Macía Heras, Natividad Calvo Romero, Verónica López Jiménez, Núria Serra Cabañas, Sheila Cabello Pelegrín, Vanesa Becerra Mosquera, Ainhoa Inza San Salvador del Valle, Domingo Marrero Miranda, Jaqueline del Carpio. Elena Monfá Guix, María Luisa Rodríguez Ferrero, Laura Salanova, Beatriz Sánchez Sobrino, Ángela García Rojas, Ana Coloma López, Francisco Llamas Fuentes
Grupo de Trabajo PROMETEO
INTRODUCCIÓN
El trasplante de órganos sólido no-renal (TOSNR), fundamentalmente hígado, corazón y pulmón, se ha expandido en las últimas décadas, lo que ha dado como resultado que un número sustancial de pacientes con múltiples comorbilidades sobrevivan más tiempo. La enfermedad renal crónica (ERC) es una complicación frecuente en este grupo de pacientes, lo que provoca un aumento de la morbimortalidad y se asocia con resultados adversos [1] [2]. El aumento de la supervivencia global debido a los avances en las técnicas quirúrgicas y el manejo de la inmunosupresión (IS) ha promovido el crecimiento en el número absoluto de pacientes que desarrollan esta complicación [1] [2]. En general, la necesidad de realizar un TOS se produce debido a un proceso de deterioro clínico previo, de duración y consecuencias variables según el órgano afectado y que van a condicionar el desarrollo de diversas complicaciones. Una de las frecuentes y relevantes es el empeoramiento de la función renal, ya sea derivada de un episodio de fracaso renal agudo (AKI) o bien de diversos factores que favorecen la evolución hacia una ERC posterior [1] [2] [3]. Cuantificar la prevalencia de la ERC en esta población de pacientes resulta complejo debido a varios factores como son la falta de homogeneidad en los criterios de clasificación del grado de enfermedad renal y de los métodos de cuantificación de empleados para valorar la tasa de filtración glomerular (TFGe) entre otros. También es importante destacar que tanto las definiciones de la función renal deteriorada como los tipos de IS empleadas han cambiado con el tiempo, lo que dificulta establecer las comparaciones. Así, en una aproximación inicial basada en varios estudios se ha observado una incidencia de ERC en la TOSNR oscila entre el 6% y el 21% [1] [2].
Existen diferencias importantes en la fisiopatología y la patología de la ERC en la población TOSNR en comparación con la población general que presenta ERC, lo que va a condicionar su manejo clínico. Las estrategias para minimizar la ERC en esta población comienzan antes del TOSNR, mediante políticas de asignación de órganos en pacientes seleccionados según su riesgo de ERC y continúan después del trasplante con el control de los factores de riesgo asociados y el tipo de IS empleada. En este sentido cada vez es más necesaria la colaboración multidisciplinar y la atención por parte de los equipos de nefrología, quienes establecerán las estrategias más adecuadas para llegado el momento iniciar terapias sustitutivas de la función renal, ya se mediante diálisis o trasplante renal.
EPIDEMIOLOGIA DE LA ENFERMEDAD RENAL CRÓNICA EN LOS PACIENTES CON TRASPLANTE DE ÓRGANO SÓLIDO NO-RENAL
Para establecer el impacto real de la ERC en los pacientes con TOSNR y su prevalencia hay que tener en cuenta la variedad en las definiciones de ERC en los últimos 20 años, así como la dependencia de ecuaciones de TFGe basadas en la creatinina sérica, de las cuales sus distintas fortalezas/debilidades/limitaciones han dificultado la evaluación de la prevalencia real de la ERC. En una de las primeras aproximaciones a la tasa de ERC postrasplante a 5 años se observó que estas eran de un 18,1% entre los receptores de trasplante hepático, 15,8% entre los receptores de trasplante pulmonar, 10,9% entre los receptores de trasplante cardíaco y 6,9% entre los receptores de trasplante corazón-pulmón. Los datos a 10 años muestran un aumento global de la prevalencia con cifras que superaban el 25% [1]. Si bien este estudio ofrece un punto de referencia, utilizaron una definición estricta de ERC (TFGe < 30 mL/min por 1,73 m2). Debemos tener en cuenta que estos criterios son conservadores por lo que subestiman la prevalencia de ERC (ya que la mayoría de los pacientes con ERC se encuentran en el rango de TFGe entre 30-60 mL/min/1,73m2), además, las características compartidas de los pacientes de baja masa muscular/desnutrición acentúan las ya defectuosas ecuaciones basadas en la creatinina. Estos datos podrían variar en función del tipo de órgano trasplantada, con una incidencia del 10-20% de ERC, y una tasa de necesidad de TRS del 2% al 8%, lo cual tiene un impacto en la mortalidad alcanzando una tasa entre el 25% y el 50% [4]. Es importante destacar que cuando se emplearon métodos de medida de la TFG más precisos, como el aclaramiento de iothalamato o de iohexol, se observó que las ecuaciones Chronic Kidney Disease-Epidemiology Collaboration (CKD-EPI) y Modification Diet Renal Disease (MDRD) se aproximan bastante a los valores reales [5].
Es probable que las tasas de ERC después de la TOSNR hayan aumentado debido al incremento de la prevalencia de comorbilidades como la obesidad y la diabetes en los candidatos a este tipo de trasplantes y a los perfiles de riesgo como la presencia de episodios de fracaso renal agudo (AKI). El impacto de la presencia de ERC en estos pacientes y el aumento de su prevalencia trae como consecuencia un mayor riesgo de mortalidad, con un riesgo relativo de muerte de 4,55 en comparación con aquellos sin ERC [6] [7]. Además, otro aspecto importante que interviene en el desarrollo de ERC es la presencia de proteinuria. En este sentido, como ocurría con la disponibilidad de datos de la TFGe, hay una escasez de mediciones de proteinuria realizadas clínicamente y/o analizadas en estudios, lo que constituye un factor importante que contribuye a la subestimación de la ERC en los receptores de TOSNR.
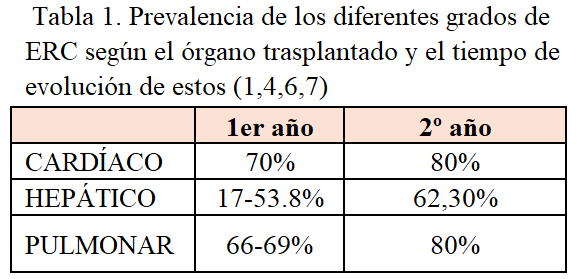
En la (Tabla 1), se representan los porcentajes de los diferentes grados de ERC según el órgano trasplantado y el tiempo de evolución de estos.
ESTIMACIÓN DEL FILTRADO MEDIANTE FORMULAS EN PACIENTES CON TOSNR
Como hemos indicado, una de las principales limitaciones para establecer la prevalencia de ERC en los pacientes con TOSNR la constituye la variedad y diferente grado de precisión de las fórmulas empleadas ara la valoración de la TFGe en estos pacientes. En una revisión donde se identificaron 26 ecuaciones utilizadas 3.622 pacientes con TOSNR (53% de riñón, 35% de hígado y 12% de otros órganos) [5]. El rendimiento de la ecuación de la Chronic Epidemiology Collaboration (CKD-EPI) [8] fue superior o comparable a otras ecuaciones alternativas, y se observó que las ecuaciones del estudio CKD-EPI y la MDRD [9] eran tan precisas en los pacientes de TOSNR como en aquellas otras poblaciones donde se habían empleado. En general, los aspectos que deben tenerse en cuenta con el empleo de estas ecuaciones incluyen la sobreestimación de la TFGe en el contexto de la reducción de la masa muscular y desnutrición, que son comunes en los receptores de NKSOT [10].
Desde un punto de vista práctico, la ecuación de creatinina CKD-EPI, seguida de la ecuación del estudio MDRD, pueden considerarse las estimaciones más adecuadas del TFGe en el TOSNR. En algunas situaciones se podría considerar el uso de la ecuación de cistatina C en combinación con las que emplean creatinina sérica como prueba confirmatoria cuando esté clínicamente indicado, como en el caso de pacientes con disminución de masa muscular o estados de desnutrición de diferente causa [11].
FACTORES ASOCIADOS AL DESARROLLO DE ENFERMEDAD RENAL CRÓNICA
Varios factores contribuyen a la alta prevalencia de ERC después de la TOSNR. Los factores de riesgo importantes incluyen ERC preexistente, presencia de glomerulonefritis (particularmente en candidatos a trasplante de hígado), que en algunos casos se debe a la infección por virus (ej VHB y VHC), y comorbilidades como diabetes e hipertensión. Los candidatos a TOSNR con una alta gravedad de la enfermedad pueden experimentar episodios repetidos de fracaso renal agudo (AKI), lo que también favorece el desarrollo de la ERC. Por último, aunque quizás no sea el único o el principal contribuyente a la ERC, el uso de inhibidores de la calcineurina (CNI) suele estar implicado en la ERC progresiva en los receptores de TOSNR.
1. FRACASO RENAL AGUDO
El fracaso renal agudo (AKI) es una complicación frecuente del TOSNR, con una incidencia reportada que oscila entre el 16,9% y el 46% [12]. Aunque se puede esperar que el AKI pretrasplante sea reversible, su contribución a la ERC futura en los receptores de TOSNR se ve exacerbada debido a las agresiones peri/postrasplante que incluyen, entre otras, el uso de CNI. El entorno perioperatorio es un factor de riesgo compartido crucial que afecta la función renal tanto a corto como a largo plazo. La hipotensión, la hipoperfusión, los desplazamientos de líquidos, los agentes nefrotóxicos, la sepsis en el período perioperatorio estimulan la presencia de AKI [2]. De manera similar a la disfunción orgánica previa al trasplante que conduce a la insuficiencia renal, la función marginal del aloinjerto genera deterioro de la función renal y viceversa [2].
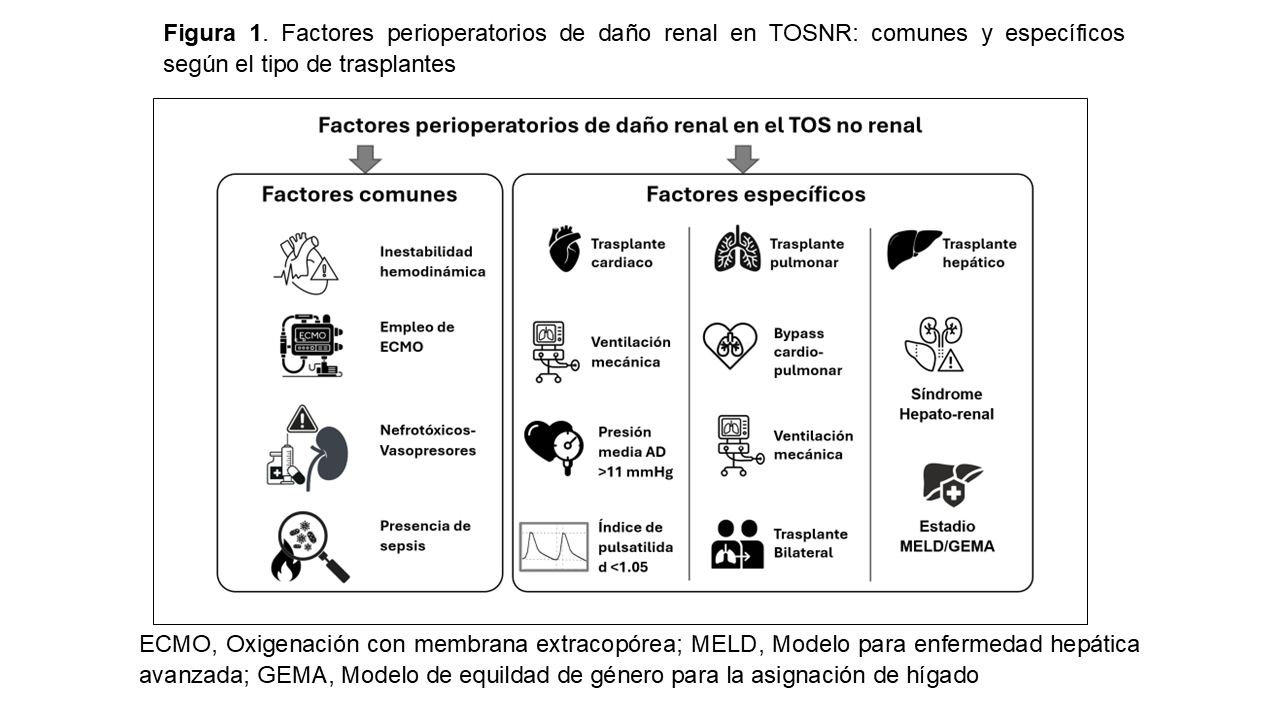
El daño renal peritrasplante se relaciona significativamente con el desarrollo de ERC [1] [13] [14] [15]. Así, los factores de riesgo fueron similares en el trasplante de corazón e hígado, atribuidos a las complicaciones quirúrgicas y a la hipovolemia secundaria a la cirugía (necesidad de fármacos vasoactivos y transfusiones), así como al uso de fármacos nefrotóxicos y a la sobredosis de ICN [13] [15]. Para aquellos pacientes con trasplante pulmonar, el riesgo de desarrollo de AKI podría ser aún mayor, pues en ello se enfatiza el uso de agentes antimicrobianos nefrotóxicos como aminoglucósidos y anfotericina, la necesidad de ICN en dosis altas debido a un mayor riesgo de rechazo agudo del injerto y el uso de ventilación mecánica [16] [17]. Al analizar los resultados del período peritrasplante, factores como la necesidad de ventilación mecánica se asociaron con el desarrollo de ERC y un aumento del 50% de la creatinina sérica. Las pautas con altas dosis de ICN también favorecieron el desarrollo de ERC, un aumento de la creatinina basal y la necesidad de TRS. Al examinar estas variables dentro de cada grupo de trasplante, se observó mayor riesgo en los receptores de trasplante pulmonar que no cambiaron a everolimus y en aquellos donde no hubo cambios en la IS. También, el empleo de contraste iodado intravenoso fue determinante en el desarrollo de ERC y el aumento en un 50% de la creatinina. En la (Figura 1) se indican los factores asociados al daño renal en el periodo peritrasplante.
En relación con la incidencia de AKI y su impacto sobre la mortalidad [4], los datos varían según el tipo de TOS, la tasa de AKI oscila entre 17-95% con una tasa de mortalidad del 25% al 74% en aquellos que recibieron TRS frente al 52% que no requirió TRS [18]. Otras series observaron valores algo mayores, al incluir todo tipo de TOSNR, con unas tasas de mortalidad no ajustada para aquellos con AKI que requirieron diálisis en comparación con aquellos que no la necesitaron fue de 49-50% frente al 2-27%, respectivamente [19].
Los factores de riesgo de AKI incluyeron retraso en la función del injerto (disfunción grado II-IV en el caso del trasplante hepático), enfermedad renal pretrasplante, niveles de albúmina sérica, duración del tratamiento con dopamina, reintervención, infección bacteriana, índice de masa corporal y uso de ciclosporina-A [20]. Como ya hemos indicado, el desarrollo de esta complicación favorece la evolución hacia ERC, junto a la presencia de otros factores de riesgo: necesidad de hemodiálisis, síndrome hepatorrenal (en el caso del trasplante hepático), uso de ICN, diabetes mellitus, hepatitis C y edad [21] [22].
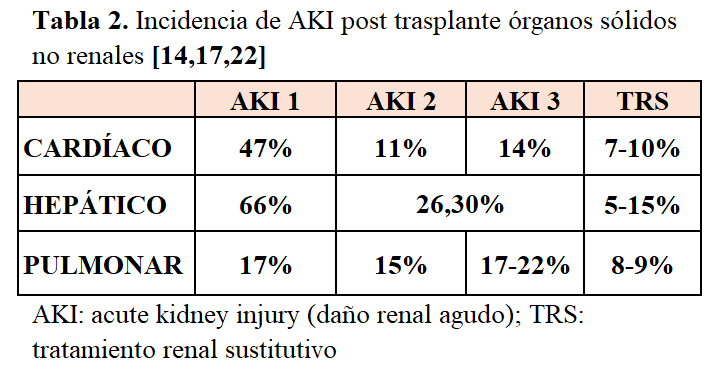
En resumen, el AKI es común después de un TONR. Su incidencia/prevalencia es elevada en los tres órganos, aunque variable debido a los criterios de definición empleados. La etiología del AKI es multifactorial. El empleo de ICN desempeña un papel importante en su desarrollo, debido a su efecto nefrotóxico. Su presencia después de un TOSNR se asocia con una mayor estancia hospitalaria, una menor supervivencia del injerto y del paciente, así como riesgo de desarrollo de ERC. Un porcentaje variable de pacientes (2.5-25%) precisa tratamiento mediante diálisis. Los pacientes más afectados los de trasplante cardiaco, seguidos de los de trasplante hepático y pulmonar. En la tabla 2, se indican los datos de incidencia de AKI según sus grados en cada tipo de trasplante.
2. INHIBIDORES DE LA CALCINEURINA
Los ICN están implicados en la lesión vascular crónica de los riñones nativos cuando se utilizan para el tratamiento de enfermedades glomerulares crónicas y en los receptores de TOS [23]. Las lesiones asociadas con el uso de ICN incluyen hialinosis focal de pequeñas arterias renales y arteriolas, que afectan de manera uniforme progresiva y progresan hasta obliterar la luz vascular, cada vez más asociada con glomeruloesclerosis global o segmentaria, atrofia tubular y fibrosis intersticial. Los mecanismos de esta enfermedad arteriolar sugieren daño endotelial, tal vez relacionado con la promoción del factor de crecimiento transformante β a través de una variedad de mecanismos.
El uso de ICN y su impacto en la función renal después de la TOSNR es un tema controvertido. Si bien el uso de ICN es una razón citada a menudo para la enfermedad renal posterior al TOS ya que constituye la mayoría de las lesiones histológicas observadas en la biopsia renal, oscilando entre el 46% y el 60% de los casos [24]. En el caso de los trasplantes de corazón, además de los ICN, el desarrollo de factores de riesgo cardiovascular y nefrotoxicidad también contribuyeron al desarrollo de ERC. En el caso de los trasplantes hepáticos, donde se estima que en aproximadamente el 50% de los pacientes que desarrollan ERC, la principal causa es la nefrotoxicidad por ICN. El efecto nefrotóxico de los ICN es más evidente en los trasplantes pulmonares, en estos constituye la principal causa de disfunción renal debido a las mayorees dosis de IS que precisan [17] [25].
3. INFECCIONES VIRICAS
Históricamente, las infecciones virales, como el VHB y el VHC, han contribuido significativamente al riesgo de ERC en el trasplante de hígado en particular. Sin embargo, con la introducción de terapias antivirales supresoras (para el VHB) y curativas (para el VHC), el papel de la infección viral en la enfermedad renal postrasplante ha disminuido. Esto ha sido reemplazado por factores metabólicos, como la obesidad y la diabetes, inherentes al aumento de incidencia del hígado graso no alcohólico como causa de insuficiencia hepática después del trasplante de hígado. Aunque la reactivación del virus BK es común en los receptores de trasplante renal, esto no se ha manifestado como un riesgo significativo en los receptores de TPSNR, y solo los informes de casos respaldan algún papel y los estudios de detección demuestran una tasa baja de reactivación del virus BK [26].
4. FACTORES TRADICIONALES ASOCIADOS A ERC
Los factores de riesgo tradicionales asociados a la ERC, como la hipertensión y la diabetes, juegan un papel importante en la ERC progresiva tras el NKSOT [7]. Las cifras de presión arterial y su grado de control en el primer año post-TOSNR se ha descrito recientemente como un factor de riesgo independiente para la disminución de la TFGe entre 1 y 5 años tras el trasplante hepático y cardíaco [27]. En el caso de los pacientes con trasplante hepático se identificaron asociaciones independientes entre la presencia de diabetes previa al trasplante, las infecciones del tracto urinario y la hipercolesterolemia en el primer año con el riesgo de progresión a ERC a los 3, 5 y 10 años. En los receptores de trasplante cardíaco, los factores asociados a esta progresión del daño renal fueron: edad, sexo femenino, reducción de la función renal antes y después del trasplante, diabetes e hipertensión [28]. Además de los mecanismos compartidos, observaron la aterosclerosis sistémica y la hipoperfusión renal de la enfermedad cardiorrenal como factores de riesgo específicos que conducen a la disfunción renal [24]. En los receptores de trasplante pulmonar, la variable dislipidemia se asoció con el desarrollo de ERC. Además, la hipertensión se asoció con un aumento del 50% en la creatinina basal. También el número de ingresos se asoció significativamente con el desarrollo de ERC, un aumento del 50% en la creatinina y de mortalidad [29].
PAPEL DE LA BIOPSIA RENAL EN LA EVALUACIÓN DEL DAÑO RENAL EN PACIENTES CON TOSNR
La biopsia renal facilita información diagnóstica, pronóstica y terapéutica. Se deberá establecer de manera coordinada entre el equipo de nefrología junto con los responsables del seguimiento del paciente la indicación y necesidad de realizar una biopsia renal [30]. Es importante destacar que los hallazgos histológicos deben interpretarse con cautela, ya que estas biopsias estaban sujetas a múltiples patrones histológicos concurrentes [31]. El que más se repite es corresponde con alteraciones que concuerdan con la toxicidad crónica de la ICN, aunque en muchas ocasiones el diagnóstico más común fue la nefropatía hipertensiva. Le siguen variedad de patrones que incluyen desde necrosis tubular aguda, glomerulonefritis mesangioproliferativa, glomerulonefritis postinfecciosa y nefropatía membranosa [31].
En la serie de biopsias renales más grande hasta la fecha, entre una población diversa de receptores de TOSNR, la evaluación histológica evidenció diferencias en las patologías observadas entre los receptores de trasplantes de pulmón, corazón e hígado [32]. La hialinosis arteriolar fue mucho más prevalente en los receptores de trasplante de pulmón y corazón que en los receptores de trasplante de hígado, mientras que la enfermedad glomerular primaria (en particular, la nefropatía por IgA) fue más común en los pacientes con trasplante de hígado. Se proporcionaron pruebas adicionales de toxicidad renal no relacionada con el ICN en la población de pacientes con trasplante hepático. Este hallazgo fue también observado en una reciente revisión [33], donde se describieron las características clínicas y la histología de la enfermedad renal comprobada por biopsia después de un trasplante de hígado, pulmón y corazón. Cabe destacar que la glomerulonefritis primaria fue del 26% en los receptores de trasplante hepático y la necrosis tubular aguda fueron los patrones histológicos más comúnmente observados en los receptores de pulmón y corazón.
En general, estas series de biopsias resaltan el hecho de que los diagnósticos distintos a la nefrotoxicidad por ICN son comunes y diferentes entre los diversos tipos de trasplante de órganos, con muchas características similares a la ERC nativa. Las advertencias a estos hallazgos incluyen el sesgo de selección, dada la variabilidad en los criterios de inclusión para la biopsia de cada centro, también el empleo y eficacia de los agentes antivirales de acción directa frente al VHC podría reducir el hallazgo de patología glomerular asociada estas entidades, junto la evolución de los criterios patológicos para el diagnóstico de nefrotoxicidad por ICN [34] [35].
Los criterios para la realización de una biopsia renal en los pacientes con TOCNR debe ser individualizada tras la valoración del riesgo-beneficio en cada caso [30]. Estará especialmente indicada en los siguientes casos: deterioro de la función renal y/o proteinuria y/o hematurias asociadas o no a HTA; sospecha de una patología de base distinta de la disfunción renal crónica en el contexto de un trasplante no renal (glomerulonefritis, nefroangioesclerosis, etc.); para confirmar la sospecha de nefrotoxicidad por ICN; como estrategia previa a la modificación de la IS, como el cambio a inhibidor del m-TOR; y permitir detectar lesiones que desaconsejen el inicio de tratamiento con inhibidores de m-TOR.
ACCIONES PARA PREVENIR O CONTROLAR LA ERC
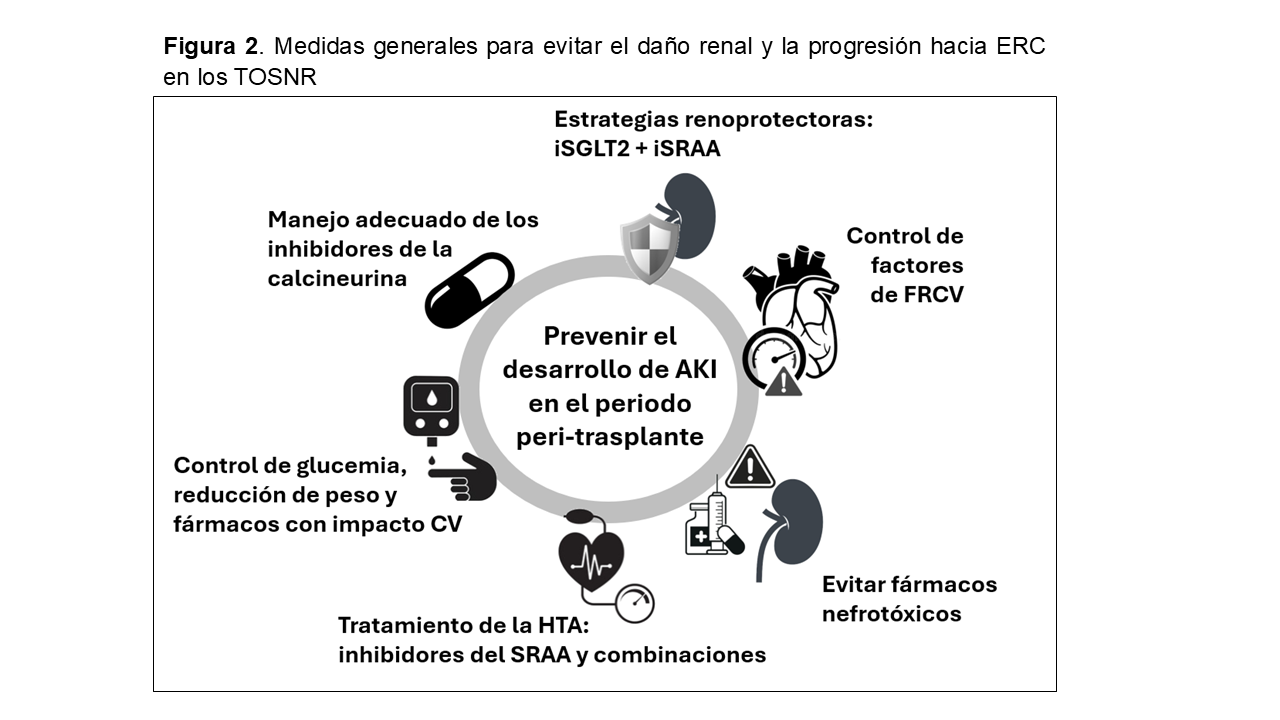
Como consideración inicial se debe asumir que el tratamiento de la ERC después de la NKSOT se basa en los mismos principios del tratamiento de la ERC en la población general [3]. En la (Figura 2), se resumen las medidas generales de protección del daño renal.
Fundamentalmente para la prevención y tratamiento de la ERC en pacientes después de TOSNR sería establecer estrategias generales frente a la ERC y otras dirigidas al empleo de ICN y su adecuada prescripción o sustitución en los casos necesarios. Es importante considerar que los mismos procesos de la enfermedad que afectan la función renal nativa siguen siendo relevantes después de la TOSNR. La literatura/guías que describen el manejo de la ERC incluyen todas las acciones con un impacto demostrando en situaciones de enfermedad renal de diferente grado [33] [36] [37]. Aunque de manera específica no se ha estudiado suficientemente el impacto de las terapias y las estrategias de tratamiento de los factores de riesgo que conducen a la ERC en la población de TOSNR [30]. Las áreas más destacadas donde se han establecido medidas serían:
1. CONTROL DE LA PROTEINURIA
La presencia de proteinuria es común en la mayoría de las enfermedades renales, en enfermedades glomerulares como en enfermedades sistémicas, diabetes mellitus e hipertensión arterial, relacionadas con el daño y progresión de la enfermedad renal. Su presencia constituye un factor de progresión hacia ERC por lo que es necesario alcanzar su control mediante diferentes estrategias que permitan enlentecer o detener el avance del daño renal. En este sentido, el empleo de fármacos dirigidos a bloquear el sistema renina-angiotensina-aldosterona (SRAA) para el tratamiento de la proteinuria en pacientes con TOSNR se extrapola de los estudios y datos referidos a pacientes no trasplantados con ERC [38] Aunque el tratamiento de la proteinuria en este grupo de pacientes está poco estudiado, el bloqueo del SRAA parece ser un enfoque razonable no solo para el tratamiento de la proteinuria, sino también para aquellos otros factores de riesgo significativos de enfermedad cardíaca (ej. HTA) debido a su beneficio cardioprotector [39].
En los últimos años se ha extendido la indicación de fármacos inhibidores del cotransportador sodio-glucosa tipo 2 (iSGLT2), conocidos como glifozinas, debido a su demostrado efecto cardio y renoprotector, en parte atribuidos a su efecto reductor de la proteinuria, tanto en pacientes diabéticos como no-diabéticos con TFGe mayores de 30 ml/m/ 1.72 m2 (y <20 ml/m/ 1.72m2 en pacientes con insuficiencia cardíaca y fracción de eyección disminuida [40]. En pacientes con trasplante renal también se han empezado a utilizar con buenos resultados y una tasa asumible de efectos secundarios (ej. infecciones génitourinarias). En una revisión que incluyo 15 estudios con receptores de trasplante renal (n=2417) y 2 estudios con receptores de trasplante cardíaco (n=122 pacientes) [41]. Se evidenció que los estudios fueron heterogéneos en cuanto a su diseño, el tamaño de la muestra, la duración de la diabetes, el tiempo hasta el inicio del tratamiento con iSGLT2 después del trasplante y el seguimiento. En general, los estudios no pudieron confirmar los beneficios clínicos cardiovasculares y renales en la población trasplantada. Los hallazgos sugirieron que los inhibidores de SGLT2 pueden mejorar el control glucémico; sin embargo, se asocian con infección del tracto urinario. Como aspectos a considera en la población de pacientes con TOSNR, estarían la necesidad de controlar los factores precipitantes de infección (ej, antecedentes de infecciones de repetición) y el riesgo de AKI asociado a episodios de depleción de volemia (ej, si está en tratamiento diurético concomitante). Sin embargo, los iSGLT2 son agentes prometedores con indicaciones cada vez mayores en la población trasplantada, pero es esencial un seguimiento estrecho. Son necesarios más ensayos controlados aleatorios a largo plazo para evaluar el efecto de los iSGLT2 en protección cardiorrenal y reducción de la mortalidad.
2. ESTRATEGIAS REDUCCION O SUSPENSIÓN DE ICN
Con los ICN como posibles potenciadores de la ERC, se han propuesto regímenes de inmunosupresión de mantenimiento que preservan/minimizan el ICN como estrategia de tratamiento renoprotector. Con el advenimiento del tacrolimus y los resultados de ELITE-SYMPHONY, el tacrolimus desplazo a la ciclosporina en cuanto al ICN de elección, ya que tiene un perfil menos nefrotóxico [42].
En el contexto del trasplante hepático, existe una amplia bibliografía que apoya el uso de la terapia de conservación o minimización del ICN con sirolimus y micofenolato. Para los receptores de trasplantes de corazón, se ha demostrado que la minimización/conservación del ICN es un enfoque de inmunosupresión viable. En una amplia revisión y metaanálisis de ocho estudios sobre minimización ICN [43] se observó que el aclaramiento de creatinina se conservaba en aquellos pacientes función renal deteriorada a los 6 meses posTOSNR (eGFR < 60 mL/min). Aunque no se demostró un beneficio a largo plazo, las estrategias de minimización del ICN no se asociaron con un aumento del rechazo, mortalidad o los eventos adversos en comparación con el enfoque del régimen estándar de ICN. El empleo de algunas estrategias de inducción ha proporcionado una cobertura inmunosupresora óptima que ha permitido: retraso en la introducción de los ICN y disminución de su dosis mientras la función renal se recupera después del trasplante [44].
Los enfoques para minimizar el uso de ICN a través de estrategias de IS de inducción/mantenimiento parecen prometedores en términos de preservación de la función renal. Si bien estos a menudo incurren en efectos adversos relacionados con terapias específicas, por ejemplo, inhibidores de mTOR, en varios casos, no han conducido a una pérdida del aloinjerto o de la supervivencia del paciente. Es posible lograr una adecuada y suficiente IS que permita optimizar la dosis de ICN para preservar la función renal y evitar el rechazo mediante la colaboración multidisciplinaria entre los expertos en trasplantes de los sistemas de órganos no renales y la nefrología de trasplantes. En este sentido se han desarrollado diversos protocolos de reducción de dosis y los cambios en la IS con resultados satisfactorios. Las dosis bajas de everolimus asociadas con ICN en dosis bajas en combinación con micofenolato y esteroides se han asociado con una mejor función renal, menos enfermedad vascular y una función cardíaca similar al año de estudios de seguimiento [45] [46]. En la (Tabla 3) se resumen las medidas preventivas del daño renal asociado a los ICN en TOSNR
TRASPLANTE RENAL EN PACIENTES CON TOSNR
Las decisiones sobre la realización de un trasplante renal riñón después de un trasplante de órgano sólido o incluso una combinación de riñón y TOS, presenta serios desafíos tanto técnicos, clínicos como éticos. Como primera aproximación todo paciente que desarrolle ERC, incluido aquel con TOSNR debe prepararse para el inicio de TSR, mediante una estrategia que determine la mejor opción de tratamiento de acuerdo con las guías de consenso KIGO [47].
La población de TOSNR constituye una cohorte de rápido crecimiento de pacientes en la lista de espera de trasplante de riñón, lo podría generar condicionantes respecto a la equidad y el acceso al trasplante de riñón para la población nativa con ERC. Un análisis de registro de 2010 comparó los resultados de pacientes con NKSOT previo (pulmón, corazón o hígado) con los candidatos a trasplante de riñón primario y con los candidatos a trasplante de riñón repetidos [48]. Los hallazgos mostraron: la mortalidad en la lista de espera fue de 2 a 4 veces mayor para los pacientes con trasplante previo de corazón, hígado y pulmón; el trasplante de riñón proporcionó una ventaja de supervivencia significativa para los receptores de TOSNR en comparación con aquellos en lista de espera, comparable al beneficio de supervivencia en los receptores de retrasplante de riñón, pero aún inferior a los receptores de trasplante de riñón primario; y la población de riñón después del trasplante de pulmón tenía un riesgo de mortalidad significativamente mayor que otras cohortes, tanto en la lista de espera como en la fase de atención posterior al trasplante. Estos hallazgos han sido corroborados por análisis más recientes [49]. En la última década se ha producido un aumento en la edad y las comorbilidades de la población con TOSNR, por lo que también ha sido objeto de estudio la evolución y resultados en los receptores ancianos de TOSNR con ERC avanzada después del trasplante renal [50]. Por tanto, dada la comorbilidad y la IS previa acumuladas de esta población, y en general de todos los portadores de TOSNR, sería conveniente realizar estudios cardiovasculares y metabólicos exhaustivos para una adecuada valoración del riesgo-beneficio en estos pacientes [29] [30].
DERIVACION Y SEGUIMIENTO POR NEFROLOGIA
La atención multidisciplinaria temprana y el tratamiento conjunto entre los servicios implicados y nefrología del trasplante son vitales para la selección adecuada de los pacientes y el tratamiento continuo de la enfermedad renal en los receptores de TOSNR [29] [47]. Tras la sospecha clínica y analítica de disfunción crónica del injerto, es muy aconsejable la remisión del paciente trasplantado no renal al equipo de nefrología dedicada al trasplante [30]. Entre los principales criterios de derivación cabe citar los siguientes: paciente que tenía una función renal deteriorada previamente al trasplante (CK-EPO >60 ml/m); paciente con varios factores de riesgo de insuficiencia renal previo al trasplante; situaciones donde existe un deterioro progresivo de la función renal tras el trasplante; y la aparición de una proteinuria superior a 0,5 g/24 h, especialmente si se asocia a HTA de reciente instauración o agravación de una hipertensión previamente estable.
CONCLUSIONES Y MENSAJES
El AKI y la ERC son altamente prevalente en el paciente con trasplante de órgano sólido no renal y su etiología es multifactorial.
Es muy importante la prevención y el adecuado manejo del AKI peri-trasplante, juntO al control de la PA y la DM a largo plazo.
Recomendamos seguir las guías de prevención cardiovascular y ERC. Valorar el empleo de nuevos fármacos (ej, iSGLT2) junto con estrategias antiproteinúricas.
Es conveniente el ajuste adecuado de los niveles de ICN, si bien su suspensión no ha demostrado beneficios en supervivencia a medio y largo plazo.
Es necesario un seguimiento nefrológico precoz de los pacientes con trasplante no renal y daño renal.
Se establecerán criterios para la realización de una biopsia renal y en aquellos casos que sea necesario para optimizar la causa del daño renal y establecer la mejor estrategia de tratamiento.
Los resultados del trasplante renal después de un trasplante no renal son excelentes teniendo en cuenta la complejidad médica y las comorbilidades de esta población de pacientes.
El trasplante renal representa una opción de tratamiento renal sustitutivo muy válida para la ERCT en receptores de trasplante no renal.
Referencias bibliográficas
1
.
Ojo AO, Held PJ, Port FK, Wolfe RA, Leichtman AB, Young EW, Arndorfer J, Christensen L, Merion RM. Chronic renal failure after transplantation of a nonrenal organ. N Engl J Med 2003; 349: 931-940.
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
2
.
Bloom RD, Reese PP. Chronic kidney disease after nonrenal solid-organ transplantation. J Am Soc Nephrol 2007; 18: 3031-3041.
http://www.ncbi.nlm.nih.gov/pubmed/?term=J+Am+Soc+Nephrol+2007%3B+18%3A+3031-3041
3
.
Clajus C, Hanke N, Gottlieb J, Stadler M, Weismüller TJ, Strassburg CP, Bröcker V, Bara C, Lehner F, Drube J, Kielstein JT, Schwarz A, Gueler F, Haller H, Schiffer M. Renal comorbidity after solid organ and stem cell transplantation. Am J Transplant 2012; 12: 1691-1699.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Am+J+Transplant+2012%3B+12%3A+1691-1699
4
.
Wilkinson A, Pham PT. Kidney dysfunction in the recipients of liver transplants. Liver Transpl 2005; S47-S51.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Liver+Transpl+2005%3B+S47-S51
5
.
Shaffi K, Uhlig K, Perrone RD, Ruthazer R, Rule A, Lieske JC, Navis G, Poggio ED, Inker LA, Levey AS. Performance of creatinine-based GFR estimating equations in solid-organ transplant recipients. Am J Kidney Dis 2014; 63: 1007-1018.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Am+J+Kidney+Dis+2014%3B+63%3A+1007-1018
6
.
Valapour M, Lehr CJ, Skeans MA, et al. OPTN/SRTR 2018 annual data report: lung. Am J Transplant. 2020;20(suppl 1): 427-508)
http://www.ncbi.nlm.nih.gov/pubmed/?term=2020%3B20%28suppl+1%29%3A+427-508%29%C2%A0
7
.
Colvin M, Smith JM, Hadley N, et al. OPTN/SRTR 2018 annual data report: heart. Am J Transplant. 2020;20(suppl 1):340- 426
http://www.ncbi.nlm.nih.gov/pubmed/?term=2020%3B20%28suppl+1%29%3A340-+426
8
.
Levey AS, Stevens LA, Schmid CH, Zhang YL, Castro AF, Feldman HF, Kusek JW, Eggers P, Van Lente F, Greene T, Coresh J; CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration). A new equation to estimate glomerular filtration rate. Ann Intern Med 2009; 5; 150: 604-612)
http://www.ncbi.nlm.nih.gov/pubmed/?term=Ann+Intern+Med+2009%3B+5%3B+150%3A+604-612%29%C2%A0
9
.
Levey AS, Bosch JP, Lewis JB, Greene T, Rogers N, Roth D. A more accurate method to estimate glomerular filtration rate from serum creatinine: a new prediction equation. Modification of Diet in Renal Disease Study Group. Ann Intern Med 1999; 130: 461-70
http://www.ncbi.nlm.nih.gov/pubmed/?term=Ann+Intern+Med+1999%3B+130%3A+461-70
10
.
Kolsrud O, Ricksten SE, Holmberg E, et al. Measured and not estimated glomerular filtration rate should be used to assess renal function in heart transplant recipients. Nephrol Dial Transplant. 2016;31(7):1182-1189.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2016%3B31%287%29%3A1182-1189
11
.
White C, Akbari A, Hussain N, et al. Estimating glomerular filtration rate in kidney transplantation: a comparison between serum creatinine and cystatin Cbased methods. J Am Soc Nephrol 2005; 16: 3763-70).
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
12
.
Rossi AP, Vella JP. Acute kidney disease after liver and heart transplantation. Transplantation. 2016;100(3):506-51.
http://www.ncbi.nlm.nih.gov/pubmed/?term=2016%3B100%283%29%3A506-51
14
.
Kim NE, Kim CY, Kim SY, Kim HE, Lee JG, Paik HC, Park Ml. Risk factors and mortality of acute kidney injury within 1 month after lung transplantation Sci Rep. 2021; 11: 17399
http://www.ncbi.nlm.nih.gov/pubmed/?term=2021%3B+11%3A+17399%C2%A0
15
.
Fortrie, G.; Manintveld, O.C.; Caliskan, K.; Bekkers, J.A.; Betjes, M.G. Acute Kidney Injury as a Complication of Cardiac Transplantation: Incidence, Risk Factors, and Impact on 1-year Mortality and Renal Function. Transplantation 2016, 100, 1740¿174.
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
16
.
Pacheco, M.P.; Carneiro-D¿Albuquerque, L.A.; Mazo, D.F. Current aspects of renal dysfunction after liver transplantation. World J. Hepatol. 2022, 14, 45¿61
http://www.ncbi.nlm.nih.gov/pubmed/?term=2022%2C+14%2C+45%E2%80%9361
17
.
Atchade, E.; Barour, S.; Tran-Dinh, A.; Jean-Baptiste, S.; Tanaka, S.; Tashk, P.; Snauwaert, A.; Lortat-Jacob, B.; Mourin, G.; Mordant, P.; et al. Acute Kidney Injury After Lung Transplantation: Perioperative Risk Factors and Outcome. Transplant. Proc. 2020; 52: 967¿97
http://www.ncbi.nlm.nih.gov/pubmed/?term=2020%3B+52%3A+967%E2%80%9397
18
.
Boyle JM, Moualla S, Arrigain S, Worley S, Bakri MH, Starling RC, Heyka R, Thakar CV. Risks and outcomes of acute kidney injury requiring dialysis after cardiac transplantation. Am J Kidney Dis 2006; 48: 787-796
http://www.ncbi.nlm.nih.gov/pubmed/?term=Am+J+Kidney+Dis+2006%3B+48%3A+787-796
19
.
Pham PT, Slavov C, Pham PC. Acute kidney injury after liver, heart, and lung transplants: dialysis modality, predictors of renal function recovery, and impact on survival. Adv Chronic Kidney Dis 2009; 16: 256-267).
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
20
.
Cabezuelo JB, Ramírez P, Ríos A, Acosta F, Torres D, Sansano T, Pons JA, Bru M, Montoya M, Bueno FS, Robles R, Parrilla P. Risk factors of acute renal failure after liver transplantation. Kidney Int 2006; 69: 1073-1080.
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
21
.
Gonwa TA, Mai ML, Melton LB, Hays SR, Goldstein RM, Levy MF, Klintmalm GB. End-stage renal disease (ESRD) after orthotopic liver transplantation (OLTX) using calcineurin-based immunotherapy: risk of development and treatment. Transplantation 2001; 72: 1934-1939).
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
22
.
Durant F, Francoz C, Asrani SK, Khemichian S, Pham TA, Sung RS, Genyk YS, Nadrim MK. Acute Kidney Injury After Liver Transplantation. Transplantation 2018; 102: 1636-1649.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Transplantation+2018%3B+102%3A+1636-1649
23
.
Naesens M, Kuypers DR, Sarwal M. Calcineurin inhibitor nephrotoxicity. Clin J Am Soc Nephrol. 2009;4(2):481-508).
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
24
.
Ojo AO. Renal disease in recipients of nonrenal solid organ transplantation. Semin Nephrol 2007; 27: 498-507.sem nephrol.2007.03.010].
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
25
.
Rocha, P.N.; Rocha, A.T.; Palmer, S.M.; Davis, R.D.; Smith, S.R. Acute Renal Failure after Lung Transplantation: Incidence, Predictors and Impact on Perioperative Morbidity and Mortality. Am. J. Transplant. 2005, 5, 1469¿1476).
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
26
.
Viswesh V, Yost SE, Kaplan B. The prevalence and implications of BK virus replication in non-renal solid organ transplant recipients: a systematic review. Transplant Rev. 2015;29(3):175- 180).
http://www.ncbi.nlm.nih.gov/pubmed/?term=2015%3B29%283%29%3A175-+180%29
27
.
Morath C, Opelz G, Dohler B, Zeier M, Süsal C. In ¿ fluence of blood pressure and calcineurin inhibitors on kidney function after heart or liver transplantation. Transplantation. 2018;102(5):845-852
http://www.ncbi.nlm.nih.gov/pubmed/?term=2018%3B102%285%29%3A845-852
28
.
Lachance K, White M, de Denus S. Risk factors for chronic renal insufficiency following cardiac transplantation. Ann Transplant. 2015; 20: 576-587
http://www.ncbi.nlm.nih.gov/pubmed/?term=2015%3B+20%3A+576-587
29
.
Viejo-Boyano I, López-Romero LC, D¿Marco L, Checa-Ros A, Peris-Fernández M, Garrigós-Almerich E, Ramos-Tomás MC, Peris-Domingo A, Hernández-Jaras J. Role of the Nephrologist in Non-Kidney Solid Organ Transplant (NKSOT). Healthcare 2023; 11: 1760-1764)
http://www.ncbi.nlm.nih.gov/pubmed/?term=Healthcare+2023%3B+11%3A+1760-1764%29
30
.
Guirado L, Almenar L, Alonso A, Castroagudín JF, Hernández D, Morales JM, Usetti P, Varo E. Nefropatía crónica en trasplante no renal: prevención, diagnóstico precoz y manejo. Nefrología 2009; 29 (Supl 5): 1-16.
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
31
.
Kubal C, Cockwell P, Gunson B, Jesky M, Hanvesakul R, Dronavalli V, Bonser RS, Neil D. Chronic kidney disease after nonrenal solid organ transplantation: a histological assessment and utility of chronic allograft damage index scoring. Transplantation 2012; 93: 406-411.
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
32
.
Schwarz A, Haller H, Schmitt R, et al. Biopsy-diagnosed renal disease in patients after transplantation of other organs and tissues. Am J Transplant. 2010;10(9):2017-2025.
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
33
.
Wiseman AC. CKD in Recipients of Nonkidney Solid Organ Transplants: A Review. Am J Kidney Dis 2022; 80: 108-118,
http://www.ncbi.nlm.nih.gov/pubmed/?term=Am+J+Kidney+Dis+2022%3B+80%3A+108-118%2C%C2%A0
34
.
Tsapenko M, El-Zoghby ZM, Sethi S. Renal histological lesions and outcome in liver transplant recipients. Clin Transplant. 2012;26(1): E48-54)
http://www.ncbi.nlm.nih.gov/pubmed/?term=2012%3B26%281%29%3A+E48-54%29%C2%A0
35
.
Pinney SP, Balakrishnan R, Dikman S, et al. Histopathology of renal failure after heart transplantation: a diverse spectrum. J Heart Lung Transplant. 2012;31(3):233-237).
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
36
.
Stevens PE, Levin A; Kidney Disease: Improving Global Outcomes Chronic Kidney Disease Guideline Development Work Group Members. Evaluation and management of chronic kidney disease: synopsis of the kidney disease: improving global outcomes 2012 clinical practice guideline. Ann Intern Med 2013; 158: 825-830
http://www.ncbi.nlm.nih.gov/pubmed/?term=Ann+Intern+Med+2013%3B+158%3A+825-830%C2%A0
37
.
Kasiske BL, Zeier MG, Chapman JR, Craig JC, Ekberg H, Garvey CA, Green MD, Jha V, Josephson MA, Kiberd BA, Kreis HA, McDonald RA, Newmann JM, Obrador GT, Vincenti FG, Cheung M, Earley A, Raman G, Abariga S, Wagner M, Balk EM; Kidney Disease: Improving Global Outcomes. KDIGO clinical practice guideline for the care of kidney transplant recipients: a summary. Kidney Int 2010; 77: 299-311
http://www.ncbi.nlm.nih.gov/pubmed/?term=Kidney+Int+2010%3B+77%3A+299-311%C2%A0
38
.
Toto RD. Transplantation: The role of RAAS blockade in kidney transplantation. Nat Rev Nephrol 2016; 12: 129-131
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nat+Rev+Nephrol+2016%3B+12%3A+129-131
39
.
Ponticelli C, Cucchiari D. Renin-angiotensin system inhibitors in kidney transplantation: a benefit-risk assessment. J Nephrol 2017; 30: 155-15)
http://www.ncbi.nlm.nih.gov/pubmed/?term=J+Nephrol+2017%3B+30%3A+155-15%29
40
.
DeFronzo R, Norton L, Abdul-Ghani M. Renal, metabolic and cardiovascular considerations of SGLT2 inhibition. Nat Rev Nephrol 2017; 13: 11-26
http://www.ncbi.nlm.nih.gov/pubmed/?term=Nat+Rev+Nephrol+2017%3B+13%3A+11-26
41
.
Lin Y, Mok M, Harrison J, Battistella M, Farrell A, Leung M, Cheung C. Use of sodium-glucose co-transporter 2 inhibitors in solid organ transplant recipients with pre-existing type 2 or post-transplantation diabetes mellitus: A systematic review. Transplant Rev 2023; 37: 100729.
http://www.ncbi.nlm.nih.gov/pubmed/?term=Transplant+Rev+2023%3B+37%3A+100729
42
.
Ekberg H, Tedesco-Silva H, Demirbas A, Vítko S, Nashan B, Gürkan A, Margreiter R, Hugo C, Grinyó JM, Frei U, Vanrenterghem Y, Daloze P, Halloran PF; ELITE-Symphony Study. Reduced exposure to calcineurin inhibitors in renal transplantation. N Engl J Med 2007; 357: 2562-2575
http://www.ncbi.nlm.nih.gov/pubmed/?term=N+Engl+J+Med+2007%3B+357%3A+2562-2575
43
.
Cornu C, Dufays C, Gaillard S, Gueyffier F, Redonnet M, Sebbag L, Roussoulières A, Gleissner CA, Groetzner J, Lehmkuhl HB, Potena L, Gullestad L, Cantarovich M, Boissonnat P. Impact of the reduction of calcineurin inhibitors on renal function in heart transplant patients: a systematic review and meta-analysis. Br J Clin Pharmacol 2014; 78: 24-32
http://www.ncbi.nlm.nih.gov/pubmed/?term=Br+J+Clin+Pharmacol+2014%3B+78%3A+24-32%C2%A0
44
.
Zuckermann A, Schulz U, Deuse T, Ruhpawar A, Schmitto JD, Beiras-Fernandez A, Hirt S, Schweiger M, KoppFernandes L, Barten MJ. Thymoglobulin induction in heart transplantation: patient selection and implications for maintenance immunosuppression. Transpl Int 2015; 28: 259-269),
http://www.ncbi.nlm.nih.gov/pubmed/?term=Transpl+Int+2015%3B+28%3A+259-269%29%2C%C2%A0
45
.
Nevens, F.; Pirenne, J. Renal disease in the allograft recipient. Best Pract. Res. Clin. Gastroenterol. 2020, 46¿47, 101690)
http://www.ncbi.nlm.nih.gov/pubmed/?term=2020%2C+46%E2%80%9347%2C+101690%29
46
.
Andreassen, A.K.; Andersson, B.; Gustafsson, F.; Eiskjær, H.; Rådegran, G.; Gude, E.; Jansson, K.; Solbu, D.; Karason, K.; Arora, S.; et al. Everolimus Initiation with Early Calcineurin Inhibitor Withdrawal in De Novo Heart Transplant Recipients: Three-Year Results from the Randomized SCHEDULE Study. Am. J. Transplant. 2016, 16, 1238¿1247)
http://www.ncbi.nlm.nih.gov/pubmed/?term=2016%2C+16%2C+1238%E2%80%931247%29
47
.
Guías KIGO 2024 en español para Enfermedad Renal Crónica (ERC). En: Lorenzo V, López Gómez JM (eds). Nefrología al día. IN: 2659-2606. dDisponible en: https://nefrologiaeldia.org/644).
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
48
.
Cassuto JR, Reese PP, Sonnad S, et al. Wait list death and survival benefit of kidney transplantation among nonrenal transplant recipients. Am J Transplant. 2010; 10: 2502-2511).
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
49
.
El-Husseini A, Aghil A, Ramirez J, et al. Outcome of kidney transplant in primary, repeat, and kidney-after-nonrenal solid organ transplantation:15-year analysis of recent UNOS database. Clin Transplant. 2017; 31: e13108).
http://www.ncbi.nlm.nih.gov/pubmed/?term=%C2%A0
50
.
Haugen CE, Luo X, Holscher CM, et al. Outcomes in older kidney transplant recipients after prior non kidney transplants. Transplantation. 2019; 103: 2383-2387).
http://www.ncbi.nlm.nih.gov/pubmed/?term=2019%3B+103%3A+2383-2387%29