Hemodiálisis Pediátrica
Palabras clave
Diálisis pediátrica, acceso vascular pediatría, hemodiálisis domiciliaria, hemodiálisis intensiva
INTRODUCCIÓN Y DATOS DEMOGRÁFICOS
La hemodiálisis (HD)con sus diferentes variedades constituyen técnicas de depuración extra-renal de implantación casi universal actualmente indispensables en el manejo del daño renal agudo en la infancia y una alternativa eficaz para el tratamiento de la enfermedad renal crónica avanzada en niños, que en manos especializadas y en centros de tercer nivel, sirven de apoyo a otras terapias de reemplazo renal crónico en la infancia como son la diálisis peritoneal domiciliaria y el trasplante renal. El hecho de que en el momento actual la hemodiálisis sea la modalidad de depuración más eficaz a corto plazo ha contribuido a una progresiva implantación de diferentes variedades de la misma técnica, en especial las basadas en la terapia convectiva o de reemplazo de fluidos, en las unidades de cuidados intensivos pediátricos y neonatales, así como en las reanimaciones quirúrgicas infantiles. Hoy en día, la en otro tiempo tan utilizada diálisis peritoneal es casi testimonial en nuestro medio como parte del tratamiento del fallo renal agudo en el que se requiere una regulación rápida del medio interno o un alivio sintomático del edema o de la sobrecarga de volumen hídrico asociado. Además, también conocemos su eficacia en la eliminación de tóxicos y fármacos de forma eficaz.; así su implantación en dichas unidades ha contribuido a la disminución de la morbilidad y mortalidad del paciente crítico.
En cuanto a la terapia de reemplazo del niño con enfermedad renal crónica avanzada, es obvio y las grandes cohortes de niños en terapia renal sustitutiva de reemplazo así lo demuestran que pese a que la mejor opción terapéutica es el trasplante renal, tan solo un 40% de los pacientes incidentes en nuestro medio lo reciben como primera modalidad de tratamiento sustitutivo y si bien la diálisis peritoneal, especialmente en lactantes, es una excelente opción terapéutica en espera de un trasplante renal, un 9% de los pacientes pediátricos españoles con terapia renal sustitutiva reciben tratamiento con hemodiálisis periódica frente a un 4 % con diálisis peritoneal y afortunadamente un 87 % con trasplante renal. En Europa, en general por una menor actividad trasplantadora en niños, la implantación total de la hemodiálisis en menores de 14 años corresponde a un 13% de todos los niños con terapia renal sustitutiva.
Es un hecho que el trasplante renal es la única modalidad de tratamiento sustitutivo que rehabilita totalmente al niño con enfermedad renal terminal y son muchas las limitaciones que tradicionalmente han sido atribuidas a la hemodiálisis hospitalaria en niños y adolescentes. En este sentido, la hemodiálisis crónica en niños se ha asociado por una parte con problemas físicos como alteraciones del crecimiento, nutrición y desarrollo; con alteraciones óseas y vasculares; con una disminución de la calidad de vida relacionada con procedimientos invasivos, hospitalizaciones, separación de los padres y de su ambiente familiar y finalmente con limitaciones escolares, sensación de pérdida de la independencia y de la identidad e integridad corporal. Encuestas realizadas a adolescentes en hemodiálisis reflejan una disminución en la participación en actividades recreativas y en la asunción de responsabilidades en relación con su proceso madurativo; sin embargo, en el momento actual, podemos decir que las nuevas modalidades de tratamiento con hemodiálisis han acabado prácticamente con los problemas físicos, mientras que la hemodiálisis domiciliaria y las nuevas unidades infantiles hospitalarias con dotación social y escolar mitigan en alguna medida las de calidad de vida y las limitaciones sociales.
CONCEPTOS BÁSICOS DE LA DIÁLISIS Y SU APLICACIÓN A LOS PACIENTES PEDIÁTRICOS.
Intercambio de solutos a través de una membrana. Difusión y convección
La diálisis es el proceso físico-químico mediante el cual se produce un intercambio molecular entre dos soluciones separadas por una membrana semipermeable. El comportamiento del agua, iones y otras moléculas a través de un sistema integrado por una membrana semipermeable, un compartimiento hemático y un baño de diálisis depende de dos diferentes propiedades: la dializancia o capacidad de difusión y la ultrafiltración. La primera depende a su vez de las características de la membrana [producto permeabilidad-área de superficie o KOA)] y se mide en ml/min. y la segunda de los gradientes de presiones hidráulicas y coloidosmóticas y de la permeabilidad hidráulica de la membrana empleada o coeficiente de ultrafiltración (KUF). El transporte difusivo o difusión expresa el movimiento de solutos siguiendo un gradiente de concentración (por ejemplo, laurea de la sangre al dializado). El transporte convectivo o convección, o simplemente ultrafiltración, expresa la cantidad de agua y solutos disueltos que pasan a través de una membrana, en este caso la membrana del dializador, provocado por un gradiente de presión (presión transmembrana). De estos dos mecanismos que regulan el fenómeno depurativo a través de una membrana, es decir de la difusión y de la convección; podríamos decir que la diálisis emplea exclusivamente el transporte difusivo, mientras que la hemofiltración o ultrafiltración emplearía exclusivamente el transporte convectivo; en realidad las técnicas depurativas actuales utilizan los dos mecanismos y la cada vez más utilizada en pacientes crónicos y también en niños, la hemodiafiltración en línea, a su vez con diferentes modalidades, se basa en la utilización combinada de ambas, lo cual intensifica el fenómeno depurativo. Por su interés en el entendimiento de estas técnicas describimos someramente las bases del transporte difusivo y convectivo.
Véase Principios Físicos de diálisis
TRASPORTE POR DIFUSIÓN
Consiste en el trasporte pasivo de solutos a través de la membrana del dializador y se produce por la diferencia de concentración entre ambos Compartimentos. La cantidad de un soluto que difunde a través de la membrana depende de dos factores:
1. Coeficiente de transferencia de masas del dializador (KoA): Es el producto de la permeabilidad de dializador (Ko) por su superficie (A).
2. Gradiente de concentración: Es la diferencia de concentración de un soluto entre el compartimento sanguíneo y el del dializado
TRASPORTE POR CONVECCIÓN O ULTRAFILTRACIÓN
Consiste en el paso simultáneo a través de la membrana de diálisis del solvente (agua plasmática) acompañado de solutos siempre bajo el efecto de un gradiente de presión hidrostática. Depende de tres factores:
UF = SC × Cs × FUF, donde
• SC es el coeficiente de cribado (sieving-coefficient) de la membrana para un soluto determinado, y corresponde a la relación entre la concentración de un soluto en el ultra filtrado y en el plasma. Para solutos de bajo peso molecular (sodio, potasio y urea) es próximo a 1 (esto es, igual en el ultra filtrado y en el plasma).
• Cs es la concentración sanguínea del soluto.
• FUF es el flujo de ultrafiltración. A su vez
FUF = QUF × PTM,
Siendo QUF el coeficiente de ultrafiltración o de permeabilidad hidráulica de la membrana del dializador y PTM el potencial transmembrana o gradiente de presión entre el compartimiento hemático y el del dializado.
En la hemodiálisis, la membrana del dializador permite el transporte bidireccional de agua y moléculas de pequeño y mediano peso molecular (menores de 50.000 Dalton), pero impide el paso de pequeñas proteínas como la albúmina (70 000 Dalton) y de los elementos formes. La práctica clínica ha hecho que diferenciemos dos modalidades de tratamiento en función de la preponderancia del fenómeno difusivo (hemodiálisis convencional) o convectivo (modalidades de hemodiafiltración y hemodiafiltración en línea [HDFOL]).
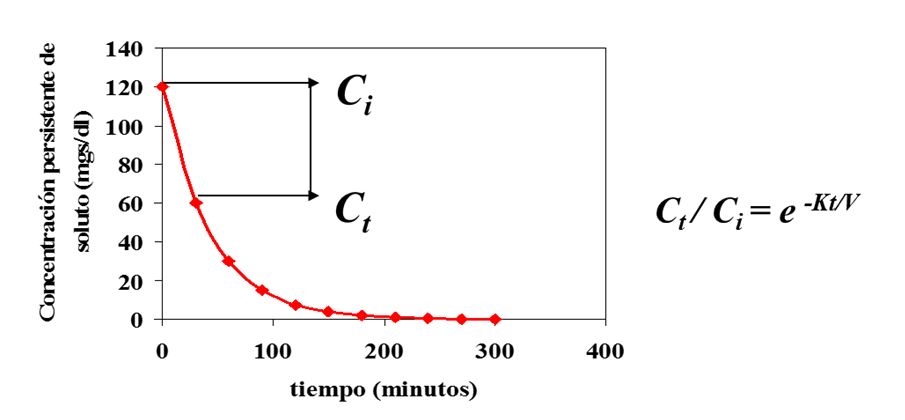
El aclaramiento de un soluto (KD) se expresa como la cantidad de sangre totalmente depurada del mismo en una unidad de tiempo (habitualmente ml/min) y depende del KOA del dializador, del flujo sanguíneo (QB) y del flujo del baño de diálisis (QD). Este concepto es virtual puesto que lo que realmente apreciamos es la disminución de la concentración del soluto. Considerando al individuo con un volumen de distribución uniforme, la fracción del soluto que permanece en la sangre en un tiempo determinado la podemos averiguar mediante la siguiente fórmula:
Ct / Ci = e-Kt/V
Donde Ct es la concentración del soluto en un tiempo t y Ci es la concentración inicial del mismo. Esta fórmula implica una tasa de desaparición del soluto de un modo logarítmico y la eficacia de la diálisis puede ser hallada según la fórmula:
Kt/V = Ln [Ci/Ct]
Donde K es el aclaramiento de urea para el dializador (mililitros/minuto), t el tiempo de duración de la sesión de HD (minutos) y V el volumen de distribución de la urea (en mililitros).
En la práctica clínica diaria Kt/V y dosis de diálisis tienen el mismo significado, volumen de plasma aclarado de urea respecto al volumen total de plasma del organismo. La
prescripción de HD se realiza sobre la base de criterios de Kt/V de urea (Figura 1), si bien, para el cálculo exacto del fenómeno depurativo hay que tener en cuenta el proceso convectivo o eliminación del soluto asociado a la ultrafiltración, así como, la existencia de una distribución no uniforme de solutos por lo que para el cálculo de la dosis de diálisis son necesarias fórmulas más complejas como veremos más adelante.
El suero urémico
La uremia o azoemia o síndrome urémico es el término medico tradicional que define un conjunto de síntomas sistémicos, fundamentalmente digestivos, cardiocirculatorios, neurológicos y respiratorios asociados a la acumulación plasmática de toxinas acumuladas por un fracaso renal terminal. Las toxinas urémicas se clasifican según su tamaño molecular y su unión a proteínas. Las pequeñas moléculas (Peso molecular inferior a 500 Dalton) se eliminan preferentemente por transporte difusivo, mientras que las moléculas de mediano tamaño (500 a 60.000 Dalton) se eliminan por transporte convectivo. En el momento actual ya existe evidencia suficiente en adultos para asegurar que la HDFOL con volúmenes convectivos superiores a 20 litros disminuye la mortalidad en pacientes crónicos.; si bien estos estudios no han sido validados en niños. Finalmente, la investigación en uremia se basa en un tercer grupo de toxinas urémicas que en realidad son moléculas unidas a proteínas de bajo peso molecular como la homocisteína o el P-Cresol sulfato y que son muy poco depuradas por técnicas de hemodiálisis convencional o HDFOL. Estas moléculas especialmente su fracción libre no unida a proteínas se asocia con mayor mortalidad o eventos cardiovasculares en población adulta y parece que la eliminación de la fracción libre estaría más favorecida por el fenómeno convectivo que el difusivo. La (Tabla 1) nos muestra una clasificación de las toxinas urémicas, así como su reducción por sesión de HDFOL y la depuración que es favorecida por la combinación del transporte convectivo.
Objetivos de la diálisis
El tratamiento de la enfermedad renal crónica incluye la corrección de todas las anomalías o alteraciones observadas: alteraciones hidroelectrolíticas o del metabolismo ácido base, alteraciones del metabolismo mineral, prevención y tratamiento de la enfermedad ósea, de la anemia, de la malnutrición, del fracaso de crecimiento y por supuesto de la integración social del niño y su familia. Aunque estas premisas permanecen cuando existe un fallo renal que precisa diálisis, son tres los objetivos que nos planteamos para tratar el síndrome urémico y que derivan directamente de la propia técnica: depuración, regulación del medio interno y eliminación de la sobrecarga de fluidos.
La depuración o la detoxificación tendría por objeto la eliminación de las toxinas urémicas. Aunque es la urea la molécula que utilizamos como medida de la eficacia de la intensidad depurativa, sabemos, como hemos comentado previamente que en realidad no es la responsable por si misma del síndrome urémico.
La regulación del medio interno tiene por objeto corregir las alteraciones iónicas y del pH sanguíneo asociadas a la uremia; así en una única sesión de hemodiálisis se pueden normalizar los niveles de bicarbonato plasmático, modificar el PH sanguíneo y corregir la hiperpotasemia, hiperfosfatemia, hipocalcemia, hiponatremia asociadas.
La regulación del peso seco del individuo mediante la eliminación del agua y sodio corporal sobrante mediante la ultrafiltración programada tiene por objeto prevenir el edema y la hipertensión arterial del niño oligúrico o anúrico.
INDICACIONES Y CONTRAINDICACIONES DE LA HEMODIÁLISIS EN PACIENTES PEDIÁTRICOS
El trasplante renal anticipado es la terapia renal sustitutiva de elección en la infancia y debe ser ofrecido a todos los niños y adolescentes que desarrollan una insuficiencia renal crónica terminal y no presentan contraindicaciones específicas. Es un tratamiento óptimo y muchas veces definitivo, si bien las diferentes modalidades de diálisis nos ayudan a mantener al niño en una situación favorable hasta recibir un órgano cuando las condiciones clínicas y analíticas no permiten que continúe exclusivamente con tratamiento conservador.
Hay otras razones que impiden la realización de un trasplante renal anticipado como son la enfermedad renal terminal de comienzo súbito, la infección activa, la necesidad de reparación quirúrgica de la vía urinaria, completar el calendario de vacunaciones, la necesidad del control clínico de la enfermedad subyacente, o la minimización del riesgo quirúrgico del trasplante asociado a la corta edad, especialmente el riesgo de trombosis vascular.
No hay estudios comparativos que hayan apoyado de forma absoluta la elección de uno u otro método de diálisis: diálisis peritoneal o hemodiálisis, contribuyendo a su elección múltiples factores (edad, localización geográfica, médicos, composición familiar, soporte social, cumplimiento del tratamiento, función residual…). En general, las limitaciones de la HD están relacionadas con la dificultad para la obtención de un acceso vascular o con la intolerancia a cambios rápidos del volumen plasmático, lo que es especialmente importante en lactantes o niños pequeños en los que existe un consenso casi universal que la terapia con diálisis peritoneales sería la más idónea hasta poder recibir un trasplante. En la (Tabla 2) mostramos las contraindicaciones para la realizar diálisis peritoneal y por tanto indicaciones de hemodiálisis.
Por otro lado, la HD se prefiere como técnica de depuración crónica en niños con malformaciones que afecten a la pared abdominal o requieran derivaciones intestinales o cirugía abdominal reiterada; también en procesos como hernias diafragmáticas congénitas o enfermedad pulmonar grave. Además, está indicada siempre que exista incapacidad difusiva o de ultrafiltración del peritoneo. La (Tabla 3) nos muestra las ventajas e inconvenientes del tratamiento con Diálisis Peritoneal y Hemodiálisis en niños según la situación del paciente.
Hay además una serie de enfermedades entre las que está la hiperoxaluria primaria en la que la necesidad de un alto rendimiento depurativo antes, durante, e incluso después de un trasplante combinado hepático y renal obligan a realizar un tratamiento protocolizado con hemodiálisis como soporte transitorio del trasplante para asegurar el correcto funcionamiento renal y la prevención del depósito en el injerto del oxálico acumulado.
En opinión de los autores la diálisis peritoneal debería ser la segunda opción de tratamiento en pediatría por sus ventajas, tanto en los niños más pequeños, como en niños mayores y adolescentes en los que esperamos una mejor integración social y escolar derivado de las bondades de esta técnica, sin embargo, reconocemos la gran eficacia de la hemodiálisis como tratamiento de reemplazo renal y su indicación prioritaria en muchos pacientes.
Finalmente debemos reconocer que en los procesos agudos la hemodiálisis es con mucho más eficaz que la diálisis peritoneal y debe ser de elección cuando es necesaria una corrección rápida del medio interno, o un alivio sintomático de la sobrecarga hidro salina, especialmente si existe repercusión cardiocirculatoria. Además, como técnica rápida, la HD es de elección en estados hipervolémicos, hiperamonemia, lisis tumoral e intoxicaciones por metanol, etilenglicol, fenobarbital, etanol, litio o salicilatos.
EL ACCESO VASCULAR PARA HEMODIÁLISIS EN PEDIATRÍA
Hoy en día podemos afirmar que el éxito de un programa de hemodiálisis guarda una estrecha relación con el acceso vascular empleado [1]. En general los accesos vasculares empleados en pediatría los podemos dividir en tres tipos: La fístula arteriovenosa, el catéter venoso central y las fístulas protésicas. Actualmente, según datos del Registro Español Pediátrico de Insuficiencia Renal Terminal (REPIR-1): http://www.aenp.es/,el 92% de los niños con HD prolongada realizan su tratamiento a través de un catéter venoso central de doble luz, tunelizado, con cuff subcutáneo y colocado preferentemente en la vena yugular interna derecha, con la punta situada en la unión cava-aurícula o en la aurícula derecha.
Catéter venoso central
Un catéter de hemodiálisis está hecho de un material blando, flexible y biocompatible, en general silicona o poliuretano modificado. Se inserta en la vena del paciente de tal forma que garantiza un flujo sanguíneo adecuado para la hemodiálisis. Hay dos tipos de catéteres de hemodiálisis: agudo y crónico. Los catéteres agudos se han diseñado para una diálisis durante un periodo corto de tiempo, usualmente menos de 30 días. Los catéteres crónicos están diseñados para una diálisis a largo plazo y pueden permanecer indefinidamente dependiendo de las complicaciones: trombosis, obstrucción, extrusión e infección pero en general garantizan un funcionamiento superior a un año o más, tiempo suficiente la mayoría de las veces para la realización de un trasplante renal [2] [3].
Catéter venoso para hemodiálisis aguda
Este catéter tiene un diseño típico para una rápida colocación, no necesariamente en un servicio de radiología intervencionista, sino que puede ser colocado en un área crítica del hospital (cuidados intensivos pediátricos, neonatología, reanimaciones o quirófano). La característica fundamental es que está desprovisto de manguito o cuff de sujeción y tiene mayor rigidez que los catéteres de hemodiálisis crónica, con un extremo que acaba en punta, permitiendo la inserción del catéter sobre la vía sin la necesidad de dilatador (la punta del catéter actúa como dilatador). Al no tener cuff y al no estar tunelizado hay un riesgo de extrusión y de infección incrementado, en especial, si el catéter se deja en el sitio más de 30 días. La inserción preferente, mediante la técnica Seldinger, es en la vena yugular interna derecha, si bien en ocasiones hay que recurrir a la vena femoral. La inserción en la vena subclavia debe ser evitada por el riesgo que tiene de estenosis posterior.
Catéter venoso para hemodiálisis crónica
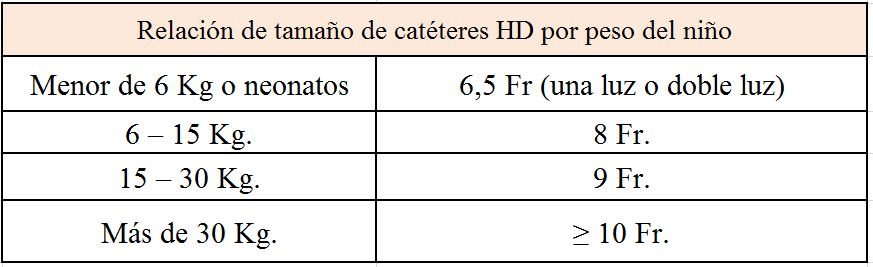
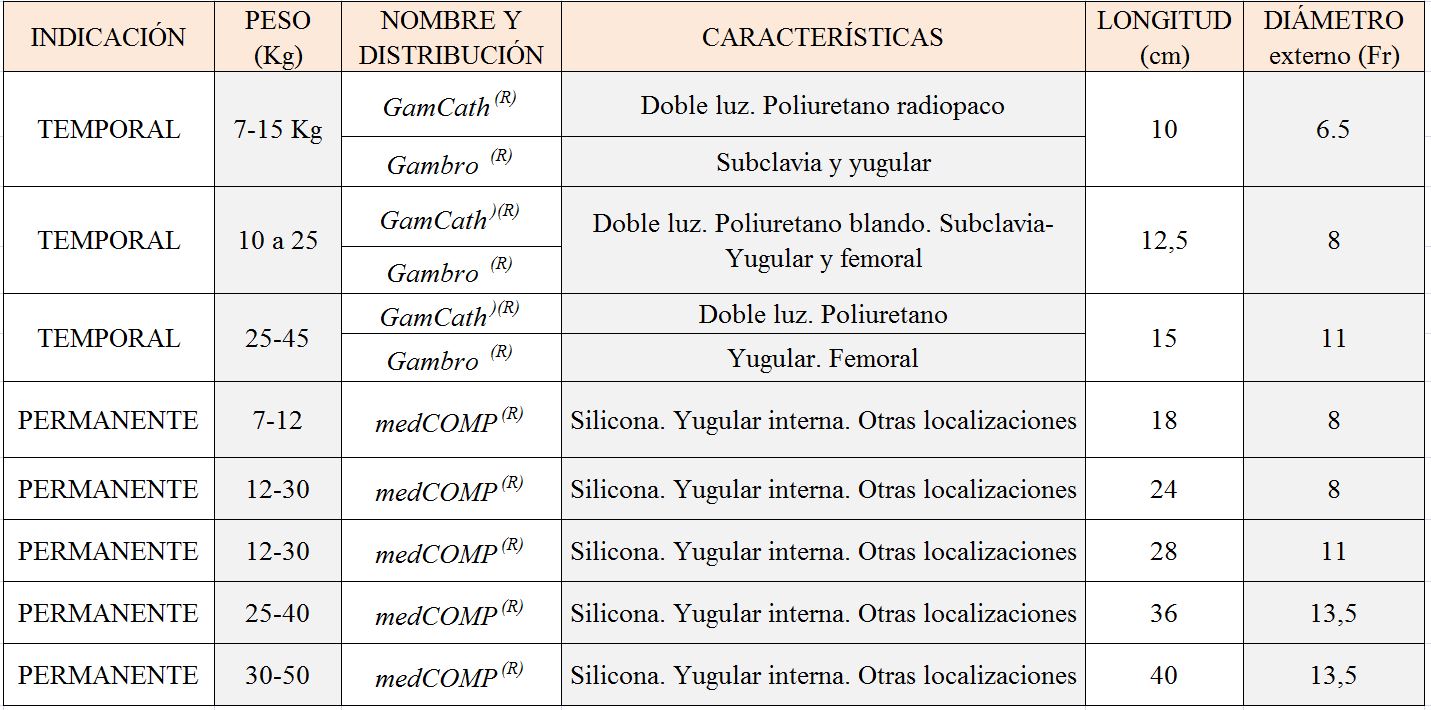
Este tipo de catéteres, ampliamente utilizados en la práctica clínica en adultos y especialmente en niños, son de silicona (en ocasiones poliuretano modificado) a los que se les ha añadido un manguito. El manguito fija el catéter en su posición dentro del túnel subcutáneo y a la vez previene la infección al impedir la entrada o migración de bacterias a la luz vascular tras su paso por el túnel subcutáneo. Este tipo de catéter es más blando (lo que permite la realización de un túnel subcutáneo) y tiene punta roma. Su colocación cuesta más que la de los catéteres agudos y en la práctica su inserción se suele realizar en un servicio de radiología intervencionista. Están diseñados de tal forma que consigan un flujo sanguíneo aceptable y que a su vez mantengan una presión venosa mínima. El flujo alto de sangre a través del dializador maximiza el potencial para la adecuación de la diálisis. La unidad de medida estándar de la industria que mide el diámetro externo del catéter son los French (F). Hay catéteres que oscilan el más pequeño 6 F y el más grande 16 F. Las (Tabla 4) (Tabla 5) muestran los tamaños y diámetros utilizados en niños de diferentes edades, tanto agudos como crónicos.
Los requerimientos de un buen catéter de hemodiálisis son:
1. Que proporcionen un flujo sanguíneo elevado sin necesidad de realizar una presión negativa o de succión importante, de forma consistente a lo largo de muchas diálisis sin una disminución de la volemia del paciente.
2. Que produzcan un trauma mínimo a la íntima de la vena con objeto de atenuar el riesgo de estenosis o trombosis venosa.
3. Que tengan una resistencia a la oclusión por la fibrina generada.
4. Que tengan resistencia a la contaminación bacteriana.
5. Que impidan la coagulación en la punta del catéter o en el interior del mismo.
6. Que no produzcan una activación de los leucocitos o las plaquetas.
La silicona es tradicionalmente el material estándar para los catéteres de hemodiálisis crónica. Es resistente a la mayoría de los agentes químicos de limpieza y muy blando y flexible. El poliuretano es el único material del mercado que es comparable a la silicona en lo que respecta a la biocompatibilidad para el acceso vascular. Su gran ventaja sobre la silicona es que un catéter de poliuretano mostrará mejores flujos que uno de silicona con el mismo diámetro interno.
El cuidado del orificio de salida de los catéteres debe adecuarse al material del que está hecho. Los catéteres de poliuretano no se deben limpiar con alcohol ni clorhexidina sino con povidona iodada, aunque un nuevo material derivado del poliuretano, el Carbothane permite la cura con aplicación tópica de alcohol. Los catéteres de silicona actuales toleran la limpieza con alcohol, aunque no todas las siliconas son compatibles con la povidona yodada.
Los catéteres de hemodiálisis deben tener la punta dentro de la aurícula derecha, sin quedar apoyadas contra la pared venosa.
Fístula arterio-venosa (FAV)
Cuando pensemos en la realización de un acceso vascular en un niño, debemos tener en cuenta, por encima de todo, la preservación del acceso vascular; así en un niño con enfermedad renal crónica conocida la preservación del árbol venoso debería iniciarse tan pronto como el diagnóstico se ha realizado, incluso en un estadio uno de enfermedad renal. Una simple extracción de sangre o la colocación de un gotero para fluido-terapia en la vena cefálica de un niño de dos años puede ser suficiente para hacer dicha vena impracticable para la realización de una futura fístula arteriovenosa. Lo ideal es que un catéter venoso de ser necesario se debe poner en el dorso de la mano para proteger la vena cefálica, particularmente en la muñeca o en el antebrazo. En caso de necesitarse un acceso venoso central el abordaje de la vena subclavia debe desaconsejase por la alta frecuencia que asocia estenosis de la misma. Debe instruirse al paciente y a la familia y la protección del brazo no dominante incluso en estadios iniciales de enfermedad crónica evitando la venopunción en dicho brazo. Por otra parte, el acceso vascular en una vena femoral puede tener futuras implicaciones para la realización de un trasplante renal dada su confluencia en el sistema iliaco donde habitualmente se realiza la anastomosis vascular y el riesgo de trombosis asociada a un catéter.
Conocido todo lo anterior, y lejos de la práctica habitual, la fístula arteriovenosa es el mejor acceso vascular para la hemodiálisis a largo plazo debido a la baja tasa de complicaciones que presenta en comparación con el catéter venoso central. En las guías clínicas KDOQI del 2006 se recomendaba la creación de una fístula en niños de más de 20 kilos en los cuales el trasplante no se va a realizar a corto plazo. Se debe usar los vasos más distales posibles en el brazo no dominante, preservando los vasos más proximales para accesos futuros. Aunque estas consideraciones son ciertas, debemos tener siempre en cuenta nuestro entorno y el rápido acceso al trasplante de los niños españoles, casi siempre inferior a los 6 meses, por lo que en el momento actual este acceso vascular, idóneo para tratamiento prolongados ha caído casi en lo anecdótico. Experiencia similar se tiene en los registros americanos y australiano; es decir nunca una guía clínica estuvo tan alejada de la práctica clínica.
Fístula protésica arterio-venosa
Este procedimiento, cada vez más en desuso, se propone cuando una fístula nativa ha fallado o es técnicamente imposible de realizar. De forma quirúrgica el procedimiento consiste en interponer entre una arteria y una vena superficial del antebrazo, generalmente en la flexura del codo, una prótesis de polytetrafluoroetileno –Gore-Tex®- Aunque puede utilizarse más pronto una fístula arteriovenosa y tiene tasas de permeabilidad primaria superiores a la fístula arteriovenosa nativa, a largo plazo tienen más complicaciones infecciosas, estenosis y fallo de permeabilidad. No es una buena primera opción como acceso vascular en pediatría.
Finalmente, y como conclusión en la elección del catéter como acceso vascular en la infancia influyen dos factores: el pequeño tamaño de los vasos, lo que favorece la trombosis de las fístulas arterio-venosas, y la oferta a corto plazo de un trasplante renal; ambos han determinado el abandono de dichas fístulas como acceso permanente en la población pediátrica española. Si tenemos en cuenta que el niño con enfermedad renal crónica necesitará varios accesos a lo largo de su vida porque requerirá con mucha probabilidad nuevos periodos de hemodiálisis, el intentar hacer una FAV proximal, con una alta probabilidad de fracaso en manos no expertas condiciona un acceso menos para un futuro. Como excepción, también es cierto que en Europa hay centros de hemodiálisis pediátrica con mucha actividad en la creación de FAV, con una filosofía “fistula first” como se hace en adultos. En segundo lugar, sabemos que normalmente la estancia de los niños en hemodiálisis suele ser corta hasta que se hace el trasplante, un motivo más para la colocación de un catéter venoso central y dejar la FAV para etapas posteriores de la vida.
EQUIPOS DE DIÁLISIS PEDIÁTRICA: DIALIZADORES, MONITORES Y LÍNEAS
El dializador
El dializador es el elemento básico del tratamiento con hemodiálisis. De sus características depende su rendimiento o capacidad de depuración.
Hay tres característi¬cas del mismo que determinan su rendimiento (eficacia con que purifica la sangre) y biocompatibilidad (propiedad por la que, al contacto con la sangre, no provoca reacciones adversas clínicamente importantes): Membrana, diseño y proceso de esterilización.
Membrana
Es el componente esencial del dializador; se¬gún su tipo, posee diferente capacidad de ultrafiltración (KUF) y depuración (KOA), influyendo su espesor y el área de superficie como determinantes más importantes de la eliminación difusiva de solutos. Actualmente se utilizan fundamentalmente de dos clases: membranas derivadas de la celulosa modificada y membranas sintéticas; estas últimas tienen distintas composiciones químicas (Co-polímeros) y a su vez pueden ser de alto o bajo flujo según su mayor o menor permeabilidad hidráulica por cada unidad de presión aplicada (mayor de 20 mililitros por hora y milímetro de mercurio de presión generada por metro cuadrado: [ml/h/mmHg/m2] o menor de 10ml/h/mmHg/m2 respectivamente). Si el uso de las de membranas de alto flujo-permeabilidad se asocia a una modalidad de tratamiento basado en convección o recambio como la HDFOL se precisa agua altamente purificada (ultrapura) y monitores de diálisis con control del volumen de ultrafiltración.
Las membranas más utilizadas en pediatría son las derivadas de la polisulfona como la helixona u otras que poseen un alto índice KoA y KUF, dotando de un alto rendimiento a la técnica, en especial si nuevamente se asocia a un alto transporte convectivo o de recambio hídrico; para ello además de la membrana es necesario que el líquido de diálisis generado en la propia unidad posea unos índices adecuados de contaminación química y bacteriana. La (Tabla 6) muestra los mínimos necesarios de contaminación química (conductividad) y bacteriana (endotoxinas y recuento bacteriano) para definir agua pura, empleada en hemodiálisis convencional, o ultra pura empleada en HDFOL.
Diseño
Los dializadores actuales utilizados en pedia¬tría son dializadores capilares, en los que la sangre fluye a través de fibras huecas de mem¬branas semipermeables, en tanto que el líqui¬do de diálisis fluye alrededor y generalmente, aunque no siempre, en sentido inverso. El número y longitud de estas fibras determina la superficie total de membrana del dializador requiriendo un volu¬men de sangre determinado para su cebado que habrá que tener en cuenta según el tama¬ño del niño al prescribir la hemodiálisis. En la (Tabla 7) podemos encontrar diferentes dializa¬dores utilizados en niños; su volumen de ceba¬do, el área total de superficie, la capacidad de aclaramiento para diferentes flujos de sangre y la capacidad de ultrafiltración.
En la prescripción del dializador y las líneas pediátricas hay que tener en cuenta el volumen extracorpóreo total que no debe ser superior a un 12% de la volemia del paciente asimismo debemos considerar que el aclaramiento obtenido con diferentes flujos hemáticos depende también del tamaño y características del dializador. La actual (Tabla 7) incorpora estos datos con dializadores de polisulfona Fresenius® de alta permeabilidad [CorDiax]y kit de líneas:
a) Neonatal A-V NATUR LINE T.M de 50mililitros;
b) Pediátrico A-V Paed de 111 mililitros y
c) Adulto FML (FA 204 C/FV 204) de 143 mililitros
para utilizar en monitores 4008S (hemodiálisis convencional y HDFOL).
Además, hay disponibles dos kits para HDFOL en monitores Fresenius 5008:
d) Pediátrico AV-Set ONLINE plus Paed 5008-R de 110 mililitros y
e) Adulto AV-Set ONLINE plus BVM 5008-R de 136 mililitros.
Los aclaramientos de urea reflejados a diferentes flujos están obtenidos a través de: 1) las gráficas de aclaramiento proporcionadas por Fresenius (R) y 2) Experiencia personal del autor en pacientes de diferentes edades en los que la velocidad de baño no ha sido constante dependiendo si la modalidad ha sido hemodiálisis convencional HDFOL.
Proceso de fabricación y método de esterilización
Es de gran importancia que el dializador sea y se mantenga estéril, dado su contacto directo con la sangre. Suelen esterilizarse con autocla¬ve de vapor o irradiación gamma, evitándose ahora el gas bactericida óxido de etileno, por su mayor producción de reacciones anafilácti¬cas.
Las líneas del circuito de sangre
Las líneas o “tabuladuras” permiten dirigir la sangre del paciente al dializador (línea arterial) y retornarlo nuevamente al paciente (línea venosa).
La línea arterial dispone de un segmento modificado que encaja en el rodillo impulsor del monitor y permite impulsar la sangre a una velocidad determinada o velocidad de flujo que en definitiva es directamente proporcional a la depuración deseada y que se modifica en función de las necesidades depurativas y el tamaño del paciente. Dispone asimismo de una línea adicional para la administración de fármacos o heparina.
La línea venosa de retorno al paciente tiene algunos elementos de seguridad de los cuales el más importante es la cámara venosa conectada a un sistema de medición de presión de retorno y un detector de aire en el sistema, dispone además de varias líneas accesorias para medicación.
Finalmente, los nuevos monitores para HDFOL tienen líneas y rodillos accesorios para regular, medir e impulsar el fluido de reposición que sustituye al suero urémico del paciente eliminado previamente en la cámara de ultra-filtrado del dializador. La reposición del fluido, que en esta modalidad es el propio líquido o baño de diálisis, puede hacerse antes del dializador (pre-dilucional), después del dializador (post-dilucional) o en ambos. Ser biocompatibles.
Las características fundamentales que deben tener las líneas de diálisis en pediatría son que no deben estar esterilizadas con óxido de etileno y deben ser de un tamaño con un volumen de cebado adecuado según el peso del niño (neonatal: 20-30 ml; lactantes: 70-80 ml; o pediátricas: 100-150 ml),
En la (Tabla 7) se puede ver las líneas del circuito hemático correspondiente a cada dializador y el volumen extracorpóreo total (suma del volumen de cebado del dializador y las líneas) para hemodiálisis convencional.
El monitor
El monitor de diálisis es un sistema integrado que consta de mezclador de concentrado de baño de diálisis con agua tratada (entre 17 y 34 litros de agua por cada litro de concentrado)y de control de flujo hemático. La sangre y el baño son impulsados hacia el dializador mediante rodillos o bombas. La bomba de sangre crea una presión negativa en la línea arterial y transforma esta presión en positiva para impulsar la sangre, tras pasar por el dializador, a través de la línea venosa de regreso al paciente. El monitor controla la composición, temperatura y flujo de sangre y baño de diálisis en el dializador, así como la ultrafiltración programada. Los monitores utilizados en pediatría son esencialmente los mismos que en los adultos, a los que se ha incorporado un software pediátrico. Además de los controles de seguridad obligatorios (fugas de aire y sangre, temperatura, control de ultrafiltración y conductividad) los modernos monitores incorporan módulos capaces de medir en tiempo real cambios en el volumen plasmático del paciente, recirculación y dializancia lo que permiten obtener cálculos muy aproximados de la dosis de diálisis durante la sesión y poder modificar la programación inicial según los cambios obtenidos, así como ajustar la ultrafiltración a los cambios de volumen plasmático del paciente. Cuando realizamos HDFOL los nuevos monitores son capaces de ajustar el volumen de recambio plasmático en línea a la presión transmembrana del monitor lo que permite fundamentalmente dos cosas: conseguir la mayor cantidad de suero urémico removido sin riesgo de coagulación del sistema por hemoconcentración por una parte y ahorrar la mayor cantidad de baño de diálisis que no va a ser utilizado.
CARACTERÍSTICAS DE LA UNIDAD DE DIÁLISIS PEDIÁTRICA
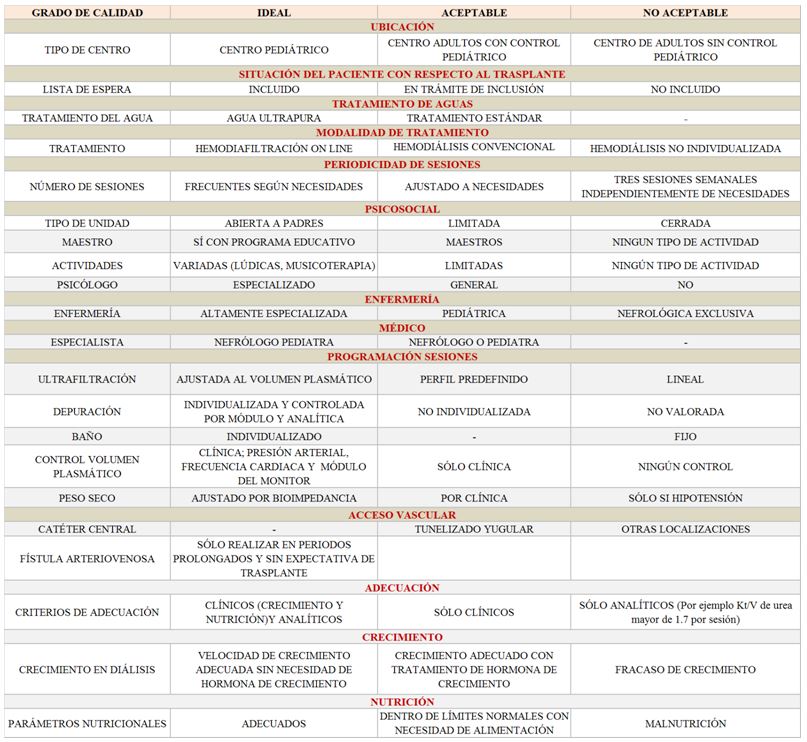
Las unidades de diálisis infantiles deberían estar situadas en hospitales con especialidades pediátricas, siendo muy importantes las de neonatología, nutrición, cuidados intensivos, cardiología, psiquiatría, radiología intervencionista, cirugía y urología pediátricas. Lo ideal, es que el hospital sea trasplantador, pero en caso que no lo fuere debería estar estrechamente conectado con el de referencia, estando los pacientes incluidos en lista de espera o programados para recibir trasplante de vivo salvo contraindicaciones. Asimismo, la unidad de diálisis infantil debe contar con enfermería especializada y apoyo de psicólogos, maestros, pedagogos y grupos de voluntarios. Las unidades deben ser de puertas abiertas para padres y familiares y estar integradas en un proyecto escolar docente. La (Tabla 8) muestra los criterios mínimos y óptimos de calidad de una unidad de diálisis pediátrica.
PRESCRIPCIÓN INDIVIDUALIZADA DE UNA SESIÓN DE HEMODIÁLISIS. HEMODIÁLISIS CONVENCIONAL Y HDFOL
Tres son los elementos básicos que tenemos que tener en cuenta en la programación de una hemodiálisis:
• ¿Qué depuración deseamos?
• ¿Qué ultrafiltración por sesión requiere nuestro paciente?
• ¿Es necesario algún ajuste especial para regular el medio interno?
Cuando pensamos en depuración, purificación o detoxificación, hasta hace pocos años la prescripción de la hemodiálisis en adultos era una prescripción empírica, y si bien en pediatría la necesidad de una programación individualizada hacía necesario ajustar los flujos de sangre, el tamaño del dializador y el baño de diálisis al tamaño y necesidades del paciente los ajustes en términos de depuración estaban exclusivamente basados en fenómenos difusivos aplicados a la urea. La aparición de la HDFOL como tratamiento ya casi universal ha variado significativamente la forma de pensar, de tal forma que cuando programamos una diálisis convencional, hablamos especialmente de cantidad de urea removida o eliminada mientras que cuando pensamos en HDFOL hablamos de cantidad o volumen de suero urémico eliminado y reemplazado.
Programación de flujo sanguíneo y de baño en hemodiálisis difusiva convencional y en HDFOL
Programación en hemodiálisis convencional
En la (Tabla 7) se puede observar el aclaramiento de urea obtenido con diferentes dializadores de polisulfona mediante flujos hemáticos crecientes durante una hemodiálisis convencional. La programación del flujo de sangre depende del aclaramiento de urea deseado y de la duración de la sesión y en condiciones normales oscilará entre 4 ml/Kg/min en lactantes y 5 ml/Kg/min en adolescentes para sesiones de hemodiálisis difusiva de 4 horas de duración. El flujo de baño de diálisis debería ser al menos el doble del flujo hemático. El cálculo del volumen de distribución de la urea puede hacerse a través de fórmulas convencionales o de estudios con bioimpedancia, pero si no disponemos de ella recomendamos utilizar un volumen de distribución uniforme de 600 ml/Kg. El siguiente ejemplo, de una forma orientativa, nos permitiría programar una sesión de hemodiálisis en cualquier niño:
Ejemplo:¿Qué valores de flujo plasmático y de baño necesitaría un niño de 12 kilogramos al que queremos prescribir una dosis de diálisis de 1,5 por sesión de 4 horas de duración?
En aras de simplificar y prescindiendo del aclaramiento convectivo ligado a la ultrafiltración para obviar fórmulas complejas como la de Daugirdas podríamos asumir que:
• Kt/V ~ Ln (BUN1/BUN2)
• Si Kt/V programado = 1,5
• 1,5 = K*240 min/12*600
• K = (1,5 * 7200 ml) /240 min = 45 ml/min (± 3.75 ml/Kg/min)
Una vez definido el aclaramiento de urea deseado buscaremos qué flujo de sangre proporcionará dicho aclaramiento que en este caso es de 45 ml/min. En la mayoría de los dializadores pediátricos será de 50 ml/min. El flujo de baño de diálisis sería al menos de 2 a 3 veces el valor obtenido; es decir 150 ml/min. Durante las primeras sesiones de hemodiálisis y con objeto de evitar un desequilibrio asociado a la rápida eliminación de urea (véase complicaciones) estaría indicado un régimen progresivo de sesiones diarias con flujos progresivamente crecientes, partiendo de Kt/V muy bajos (0.5 ó 0,6 por sesión) hasta llegar al deseado. Asimismo, durante la primera sesión estaría recomendado la administración de manitol a dosis de 0,5 a 1 gramo por kilogramo para evitar el edema cerebral asociado al paso de agua a la neurona por cambios bruscos en la osmolalidad plasmática.
Hemodiafiltración en línea (HDFOL)
Antes de nada, deberíamos decir que la hemodiálisis convencional, especialmente en un régimen intensificado de sesiones, consigue en la mayoría de las ocasiones una buena situación del paciente hasta el trasplante y aunque no hay estudios suficientes que permitan extrapolar estos hallazgos al tratamiento con HDFOL es de suponer que la mayor depuración alcanzada pueda suponer en el futuro la modalidad de elección de tratamiento con hemodiálisis en la infancia. De las tres modalidades existentes (post-dilucional, pre-dilucional y mixta) la más utilizada es la primera. Pues bien, el volumen total recomendado de intercambio debe aproximarse a 10 litros por metro cuadrado y sesión en modo post-dilucional y aproximadamente el doble en pre-dilucional. La (Tabla 9) nos muestra los valores de programación en modo post-dilucional en niños y adolescentes de diferentes edades.
En la presente Tablase señala de forma orientativa cómo programar una sesión de HDFOL en modo post-dilucional en niños y adolescentes de diferentes edades: volumen total de intercambio por hemofiltración, flujos de intercambio (QHDFOL ml/min) y de sangre (QB ml/min), dializador y rendimiento obtenido de forma aproximada para una diálisis de 4 horas expresados en forma de Aclaramiento de urea (Kurea) y Kt/V total durante la sesión en un monitor Fresenius 4008S. Hay que tener en cuenta que en los nuevos monitores 5008 el QHDFOL (flujo de reposición en línea) es calculado directamente por el software del monitor a partir de los valores de QB y presión transmembrana con objeto de evitar hemoconcentración excesiva; asimismo el QD se ajustaría automáticamente a los valores anteriores con objeto de evitar gasto innecesario de baño de diálisis. En cualquier caso, la ratio QHDFOL/QB se aproxima a 0,25 por cualquier procedimiento, si bien en condiciones óptimas puede llegar a un 0,33 con el monitor 5008.
Debemos insistir que para realizar una HDFOL son necesarias algunas condiciones:
• Acceso vascular apropiado para conseguir flujos de extracción e infusión suficientes.
• Agua de diálisis ultra pura y con ausencia de endotoxinas (Tabla 6)
• Peso superior a 15 kilogramos
• Dializadores de alta permeabilidad
• Personal médico y de enfermería formado
Ultrafiltración y perfil de sodio.
La programación exacta de la ultrafiltración en cada sesión es imprescindible en lactantes y niños por lo que recomendamos monitores con control automático ajustado al volumen plasmático, que permiten conseguir tasas de ultrafiltración adecuadas sin provocar hipotensión. No es inhabitual que durante las primeras sesiones de niños con poliuria tengamos que infundir sueros salinos isotónicos para prevenir cambios en el volumen plasmático; además debemos ajustar la concentración de sodio del baño a lo largo de la sesión; más alto inicialmente y más bajo en la última hora. El puesto de hemodiálisis (cama o cuna) debe incorporar un sistema de control de peso. Es necesario, además, un control riguroso por parte de la enfermería de la ingesta sólida y líquida del niño durante la sesión. La ganancia de peso ínterdiálisis no debería exceder del 5% del peso seco establecido. Las modificaciones del peso seco se realizan con carácter semanal en los niños mayores y diario en los lactantes y siempre que no exista variación del estado clínico.
Anticoagulación.
Cada vez es menos frecuente la administración de heparina sódica horaria o en bomba de infusión que ha sido sustituida por heparinas de bajo peso molecular (HBPM) que tienen la ventaja de poseer una mayor biocompatibilidad, no alterar los tiempos de coagulación y disminuir el riesgo de sangrado. Sus principales desventajas radican en la permanencia del efecto anticoagulante una vez finalizada la sesión de diálisis y el mayor coste económico. Si se decide este tipo de anticoagulación, recomendamos la administración de enoxaparina a dosis de 0,5 a 1 mg/kg (50 a 100 unidades/kg) en la línea arterial al inicio de la sesión. Aunque no está recomendado sistemáticamente, en algunos pacientes con hemodiálisis diaria en el que las dosis acumuladas de HBPM puede inducir riesgo de hemorragia por acumulación se puede determinar actividad anti factor Xa con objeto de dosificar las heparinizaciones sucesivas.
Sellado y cuidado del catéter
La casi sistemática utilización del catéter central como acceso vascular en niños deriva en una atención específica que incluye vigilancia del aspecto del orificio de salida, control bacteriológico del mismo, cura diaria o semanal según el estado y finalmente sellado de las luces con citrato, heparina o uroquinasa. Diferentes soluciones comerciales ofrecen una combinación de uroquinasa con taurolidina y /o citrato para el sellado del catéter durante las sesiones.
Adecuación
Los criterios de adecuación no serán nunca exclusivamente numéricos, sino que también serán valorados parámetros clínicos como la nutrición y el crecimiento. Aunque las guías de práctica clínica recomiendan que el Kt/V mínimo por semana sea superior a 4.5 (1.5 por sesión en hemodiálisis convencional de tres sesiones semanales) hoy sabemos que el incremento de estos valores hasta alcanzar valores de Kt/V de 8, 9 o incluso más como resultado de un incremento del número de sesiones semanales, duración de las mismas o ambas, se asocia con una espectacular mejoría de los parámetros de nutrición y crecimiento así como un mejor control de la acidosis y del fosfato sérico. Con dos limitaciones básicas: social y económica, la intensificación del régimen de diálisis debería ser planteado en todos los pacientes. Para el cálculo del Kt/V utilizaremos la fórmula de Daugirdas de segunda generación:
Kt/V = Ln [(BUN1/BUN2)-0,008* Tdh] + (4-3,5*[BUN1/BUN2]) * (UF/peso seco)
Donde Tdh sería la duración en horas de la sesión de diálisis y UF la ultrafiltración en litros. El peso seco post diálisis se expresaría en kilogramos. Esta fórmula permite un cálculo más exacto de la dosis de diálisis y tiene una excelente correlación con las obtenidas a través de los cambios en la dializancia de los modernos monitores de diálisis.
HEMODIÁLISIS INTENSIVA Y HEMODIÁLISIS DOMICILIARIA EN NIÑOS
Hemodiálisis intensiva. Nomenclatura
Con el término “hemodiálisis intensiva” nos referimos a aquellas pautas o modos de realizar la hemodiálisis en las que se aumentan el número de horas por sesión, el número de sesiones a la semana, o ambos parámetros. Este término surge en contraposición al de “hemodiálisis convencional” que hoy en día se refiere a la pauta de hemodiálisis clásica de sesiones de cuatro horas realizadas tres días por semana. La nomenclatura utilizada en la literatura médica es muy variable, y para su estandarización utilizaremos la reflejada en las últimas guías KDOQI sobre adecuación en hemodiálisis, publicadas en el año 2015 [4]. Todas las prescripciones de diálisis deben especificar la duración de la sesión, el número de tratamientos por semana, el flujo de sangre y de dializado, donde se realiza el tratamiento, y el nivel de asistencia.
Denominamos hemodiálisis convencional aquella que tiene una duración de la sesión entre tres y cinco horas, tres o cuatro veces por semana. A partir de esta hemodiálisis convencional, podemos incrementar el número de horas de diálisis a la semana de tres formas: la primera de ellas es incrementando la duración de las sesiones. La segunda incrementando el número de sesiones a la semana y una tercera forma que sería unir ambas circunstancias.
Se denomina hemodiálisis frecuente aquella que se realiza más de cuatro veces por semana, entre cinco y siete veces. Dentro de ella tendremos la hemodiálisis frecuente corta si la duración de la sesión es menor de tres horas, estándar si la duración de la sesión está entre tres y cinco horas y larga si la duración es superior a cinco horas.
Se denomina hemodiálisis larga aquella cuya duración es superior a cinco horas por sesión. En ellas incluimos la hemodiálisis larga tres veces por semana, la hemodiálisis larga a días alternos y por último la hemodiálisis larga y frecuente entre cinco y siete días por semana.
Según donde se realice la sesión de hemodiálisis tendremos la hemodiálisis en el centro o en domicilio.
Según el nivel de asistencia hablaremos de asistencia completa si la hemodiálisis se realiza por un sanitario, parcialmente asistida si el paciente realiza algunos aspectos de la hemodiálisis él mismo mientras que otros son realizados por un sanitario, y la auto asistida en la cual el paciente realiza todos los aspectos del tratamiento él mismo sin asistencia de ningún sanitario.
Desde el punto de vista del flujo sanguíneo para un adulto se considera que el flujo estándar es mayor o igual a 300 ml por minuto y un flujo bajo sería menor a 300 ml por minuto. Y por último según el flujo del dializado hablaríamos de una sesión estándar si el flujo es mayor o igual a 500 ml por minuto y bajo flujo si es menor de 500 ml por minuto.
Medición de la dosis de diálisis con técnicas intensivas
En la hemodiálisis convencional la dosis de diálisis se mide con el Kt/V de urea por sesión, que es el aclaramiento de urea del dializador multiplicado por la duración de la sesión y referenciado al volumen de distribución de la urea del sujeto.
Con el fin de medir y comparar distintas pautas de diálisis entre sí e incluso poder comparar la dosis de diálisis con el aclaramiento renal de referencia normal, F.A. Gotch propone el término de Kt/V estándar (stdKt/V) [5]. Gracias a este parámetro, distintas técnicas de diálisis: hemodiálisis y peritoneal, técnicas mixtas, o distintas pautas de diálisis: hemodiálisis estándar frente a diaria corta, larga intermitente, incluso técnicas de depuración extra renal continuas, se pueden comparar entre sí. Sirve también como un convertidor de dosis de diálisis de forma intermitente a su equivalente continuo.
Asimismo, se establece el patrón de referencia del aclaramiento renal de urea del riñón sano. Para un flujo urinario normal de 1.5 ml/min y un filtrado glomerular de 100 ml/min, el aclaramiento de urea normal es de 45 ml/min. Si normalizamos este valor a un volumen de referencia de 35 litros, este valor servirá como un estándar de referencia para la función renal normalizada para evaluar la dosis de diálisis relativa a la función renal normal.
De esta forma la referencia del aclaramiento renal de urea será ref. Kt/V = 45 ml/min x 1440 minutos/día /35 l = 1.85 al día ó 12.96 semanal.
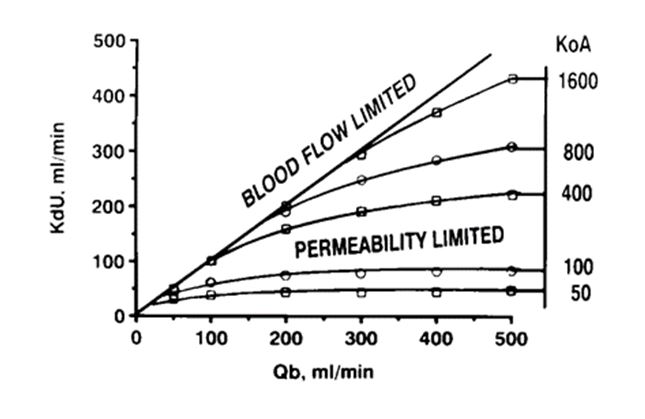
Podemos representar gráficamente estos conceptos, de tal forma que el aclaramiento de urea de un dializador (KdU, ml/min) esté en función del flujo sanguíneo (Qb, ml/min) y en función de las características de permeabilidad del dializador en cuestión (KoA). Cuando tenemos un dializador de poca eficiencia (KoA bajo), que no es capaz de aclarar toda la sangre que le llega, este actúa como factor limitante del aclaramiento. Cuando en cambio, tenemos un filtro que es capaz de aclarar de urea la sangre con mucha eficiencia, alcanzando un KoA máximo con Qb y Qd infinito, el flujo de sangre es el que hará de factor limitante como puede verse en la Figura 2.
Valoración del stdkt/v, como representante del aclaramiento continuo semanal, en función del spktv de cada sesión y el número de sesiones a la semana
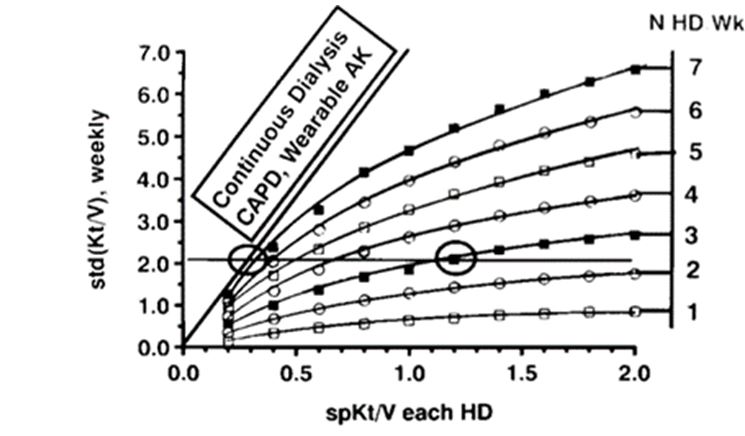
Podemos representar en una gráfica, en el eje de abscisas el spKt/V de cada sesión de hemodiálisis, y en el eje de ordenadas el aclaramiento semanal en su equivalente continuo, stdKt/V trazando varias líneas que representen el número de sesiones a la semana. El riñón sano es capaz de aclarar 45 ml/min de urea. Esto se traduce, para un paciente con un volumen de distribución de urea de 35 litros, en un Kt/V en un día de 1.85 y en una semana un stdKt/V de 13. (Figura 3)
Derivado de las consideraciones anteriores podemos incrementar el aclaramiento semanal de urea de dos formas o en dos direcciones.
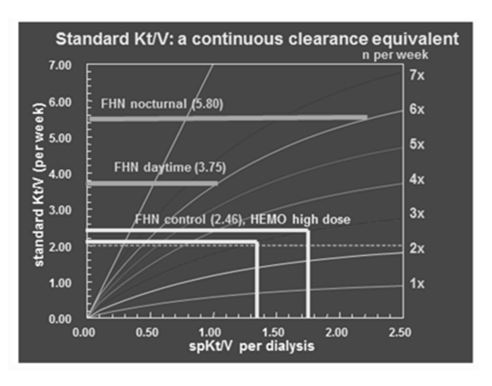
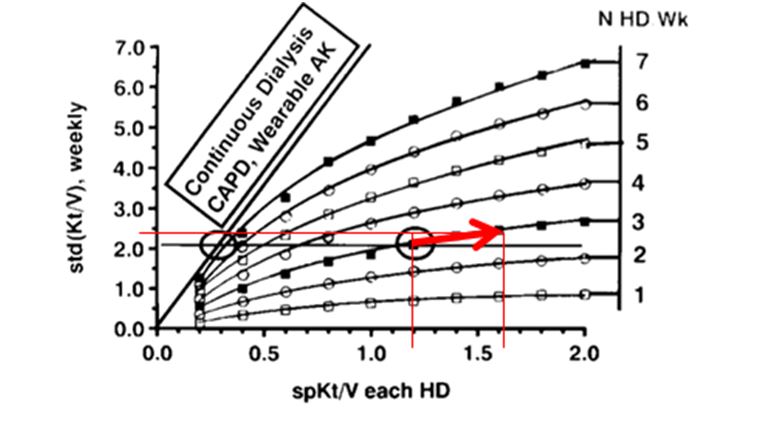
La primera (Figura 4) es incrementando el Kt/V por sesión. Nos desplazamos en una escala logarítmica, hacia la derecha. Vemos que, para un esquema de diálisis convencional, de tres sesiones a la semana, con un spKt/V de 1,2 y un stdKt/V de 2.0 como marcan las guías, si incrementásemos el Kt/V por sesión de 1.2 a 1.6, un incremento significativo de un 33%, se traduce en un std Kt/V de 2.0 a 2.3, un incremento de un 15%.
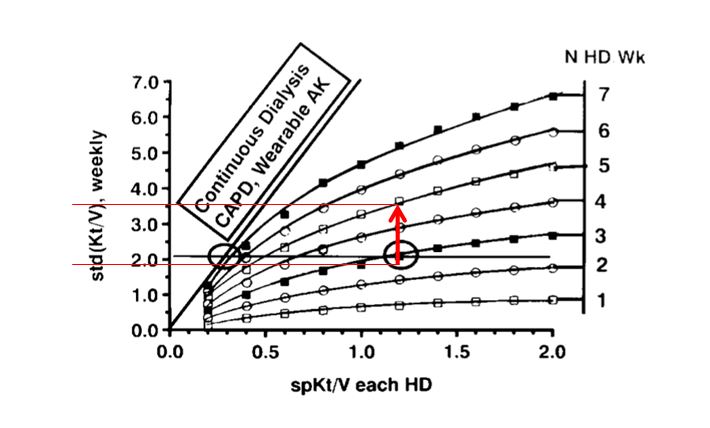
Pero si nos desplazamos en un sentido vertical hacia arriba, por ejemplo, manteniéndonos en un spKt/V de 1.2 pero pasando de 3 a 5 sesiones a la semana, incrementamos el std Kt/V de 2.0 a 3.5, un incremento del 75% (Figura 5).
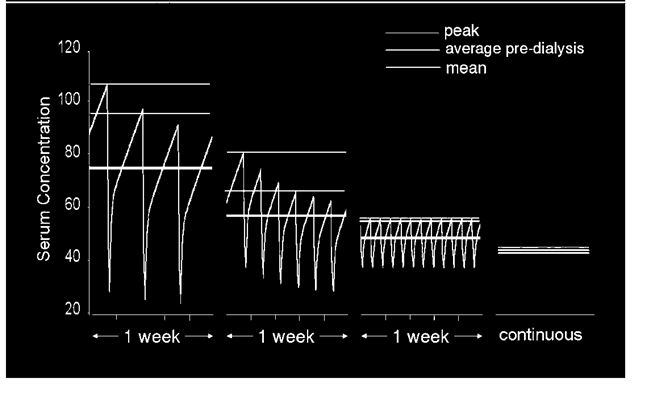
¿A qué se debe esta diferencia? Pues bien, debemos destacar que la capacidad de aclaramiento de urea de los filtros actuales es muy alta, superando la eficiencia del propio riñón sano. En un régimen de diálisis discontinuo, la generación de urea es el factor limitante que impide un mayor aclaramiento, al igual que en el apartado anterior un Qb bajo actúa como factor limitante del aclaramiento. A lo largo de la sesión de diálisis el aclaramiento de urea tiene tendencia a disminuir porque el gradiente de urea con el dializado va descendiendo. Para incrementar la eficiencia tengo que aumentar el número de horas a la semana en forma de más sesiones. A medida que aumenta la frecuencia de las sesiones a la semana, tendiendo a una sesión continua, el BUN (área bajo la curva o “time averaged BUN”) va disminuyendo y el pico de BUN en la primera sesión semanal y la media de BUN pre-diálisis se igualan (Figura 6).
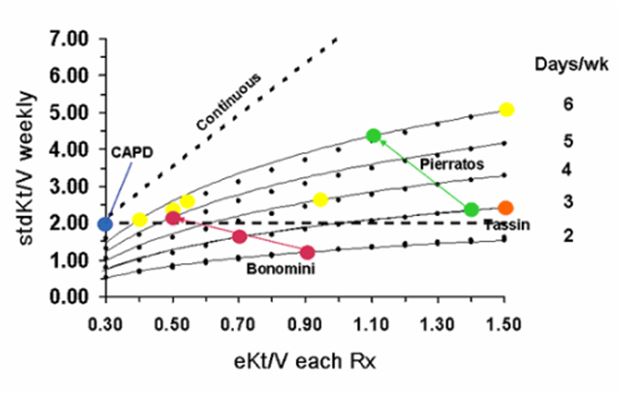
Analizando bajo esta perspectiva las diversas pautas de hemodiálisis que se han publicado con resultados, el primer estudio es de Bonomini y colaboradores [6] [7]. Que realizan varias pautas de hemodiálisis. Partiendo de dos sesiones a la semana con un eKt/V de 0,90, incrementan el número de sesiones a tres y cinco, a la vez que disminuyen el eKt/V a 0,70 y 0,50. El efecto en la gráfica está en la línea roja. Incluso con eKt/V de 0,5, si se realizan 5 días por semana se alcanzan las recomendaciones actuales. El grupo de Tassin en Francia aparece en naranja. Sesiones de 8 horas en el centro, 3 días por semana superan las recomendaciones de alcanzar un stdKt/V de 2 (Figura 7).
En cuanto a las publicaciones en adultos, ha habido 5 grandes ensayos clínicos acerca de la dosis de diálisis adecuada en pacientes adultos. El primero de ellos fue el “National Cooperative Dialysis Study” (NCDS) que surgió de una reunión de expertos sobre adecuación en diálisis en 1975 y patrocinado por el “National Institutes of Health” publicado en 1981 [8].
El segundo estudio destacado, también patrocinado por el “National Institutes of Health” fue el “estudio HEMO” publicado en el año 2002 [9]. Tras estas dos iniciales se han realizado tres más: The Frequent Hemodialysis Network (FHN) Daily Trial [10] [11]. The Frequent Hemodialysis Network (FHN) Nocturnal Trial [10] [12] , [13] y The Alberta Nocturnal Hemodialysis Trial [14].
El estudio randomizado HEMO muestra como con un incremento de la dosis de diálisis del 35% medida por spKt/V, que en un principio parece una magnitud relevante, se traslada a un incremento semanal del stdKt/V menor de la mitad. Un stdKt/V de una persona con un volumen de distribución de la urea de 35 litros representa 7 ml/min de aclaramiento de urea expresado en forma de aclaramiento continuo. Volviendo al estudio HEMO, el incremento en forma spKt/V se tradujo en un incremento de stdKt/V x 1,18; así, en esta persona ejemplo, el aclaramiento pasaría de 7.0 a 8.3 ml/min. En este sentido, no es sorprendente que la comparación de ambos brazos de tratamiento no fuera significativa (Figura 8).
Al darse cuenta de estos aspectos el grupo FHN decidió diseñar dos ensayos clínicos randomizado y controlados, los más importantes realizados hasta la fecha. Uno de ellos, llamado “Daily Trial” fue concebido para aportar el equivalente a 14 ml/min de aclaramiento continuo, un stdKt/V de 3.75, y el otro, el “Nocturnal Trial” se pensó para aportar 20 ml/min, en torno a 5,8 de stdKt/V. Un segundo efecto que se buscó fue ver si se podía controlar mejor el volumen extracelular con estos esquemas más frecuentes. Los datos sugieren tanto ventajas como inconvenientes de las hemodiálisis frecuentes y ambos ensayos clínicos pueden dar una guía potencial en cuanto a los pacientes que podrían beneficiarse de los esquemas más frecuentes que serían los que tienen hipertrofia de ventrículo izquierdo o hipertensión arterial grave, así como bajos niveles de función renal residual. Los resultados también sugieren que no hay que cambiar a los pacientes a un esquema de mayor frecuencia intentando mejorar la anemia o la nutrición.
Estudios de hemodiálisis intensivas en niños
En cuanto al campo Pediátrico no hay ningún ensayo clínico de dosis de hemodiálisis ni de hemodiálisis frecuente, teniendo que recurrir a los artículos publicados por los grupos de hemodiálisis pediátrica con experiencia en este campo [15]. Son fundamentalmente tres, el de Berlín, el de Toronto y el de Estrasburgo que resumimos a continuación:
GRUPO DE BERLIN. Charité-University Medicine Berlin. J. Thumfart, U. Querfeld, D. Müller. Realizan hemodiálisis larga en el centro de diálisis, tres veces por semana. Establecieron el programa de hemodiálisis larga nocturna en el año 2005 al que posteriormente añaden hemodiafiltración. Han publicado varios artículos. Uno de ellos es un estudio prospectivo observacional con 16 pacientes en el que se aprecia una mejoría en el control de las cifras de tensión arterial, de la hipertrofia ventricular izquierda, mejor control del fósforo, calidad de vida. No hallazgos significativos en cuanto a la mortalidad [16].
GRUPO DE TORONTO. Hospital for Sick Children. D.F Geary. Tienen un programa de hemodiálisis larga y frecuente, 8 horas, 6-7 días a la semana, en casa, Qb 150 ml/min, Qd 200-300 ml/min. Son un grupo de referencia para la hemodiálisis domiciliaria pediátrica. En una de sus publicaciones en el 2005, una serie de casos, 4 pacientes en programa de hemodiálisis larga nocturna frecuente en domicilio. Encuentra una mejoría en el control del fósforo y calidad de vida, no siendo significativos los hallazgos para la tensión arterial, hipertrofia ventricular izquierda y mortalidad [17].
GRUPO DE ESTRASBURGO Fischbach. Aplica un programa de hemodiafiltración online frecuente corta en el centro. En las publicaciones que hace en NDT año 2004 [18] y 2010 [19], series de casos. En su trabajo observacional prospectivo con 5 pacientes en hemodiafiltración frecuente corta aprecia una mejoría en el control de las cifras de tensión arterial, hipertrofia ventricular izquierda, mejor control del fósforo. Hubo un incremento significativo en la velocidad de crecimiento. No muestra hallazgos significativos en cuanto a la calidad de vida y mortalidad.
Guías clínicas y hemodiálisis intensiva en niños y adultos
GUÍA EUROPEA DE HEMODIÁLISIS PEDIÁTRICA, AÑO 2005
Aunque no tiene un apartado como tal para la hemodiálisis intensiva, sí se reconoce como un arma terapéutica, asumiendo que la reducción de la prescripción de diálisis a tres sesiones semanales de tres horas basado en la cinética de la urea debería ser abandonada para los niños que son de dializados a largo plazo y ser reemplazadas para una diálisis óptima que se obtiene con diálisis más largas o más frecuentes. La hemodiálisis diaria es una aproximación, quizá la única para alcanzar una buena depuración de fósforo y mantener el producto calcio fósforo en el rango óptimo [20].
GUÍA EUROPEA ADULTOS AÑO 2007
El grupo de trabajo en hemodiálisis de la European Dialysis and Transplantation (EDTA) publicaba en el año 2007 las European Best Practice Guidelines en estrategias de diálisis. Hace referencia a la “cantidad de diálisis” en los siguientes puntos:
Las ventajas potenciales sería una menor ganancia de peso interdialítica; mejor tolerancia a la sesión; mejor control de las cifras de tensión arterial; disminución de la hipertrofia ventricular izquierda; mejoría de la situación nutricional; mejor control del fósforo y mejoría en la calidad de vida. Las desventajas: Limitaciones para la organización; coste; y manipulación más frecuente del acceso vascular [21].
Existe además una reflexión sobre la hemodiálisis larga nocturna cuyas ventajas fundamentales son el incremento en stdKt/V semanal como en otras pautas de diálisis intensiva y específicamente para esta pauta de hemodiálisis ase aprecia un incremento en el aclaramiento de beta 2 micro globulina, un mejor control del fósforo así como una disminución de los episodios de hipotensión intradiálisis y de las complicaciones cardiovasculares, mostrando como limitaciones la depleción de calcio y fósforo.
Como conclusiones de esta guía la hemodiálisis debe ser proporcionada al menos 3 veces por semana, y la duración total debe ser al menos de 12 horas por semana, a no ser que haya una función renal residual significativa. Se debería considerar un aumento en la duración y/o frecuencia en pacientes con inestabilidad hemodinámica o cardiovascular, en pacientes que permanecen hipertensos a pesar de la máxima tasa posible de UF o con mal control del fósforo o malnutridos.
KDOQI AÑO 2015
Incluye a su vez 5 guías [22]. La guía 2 específicamente habla de este tema: “Guideline 2: frequent and long duration hemodialysis”. Las guías 2.1 y 2.2 concernientes a hemodiálisis frecuente en el centro se basan fundamentalmente en los resultados obtenidos del The Frequent Hemodialysis Network (FHN) Daily Trial, hemodiálisis frecuente, corta en el centro y quedan así:
Guía 2.1. Sugiere que a los pacientes con enfermedad renal terminal se les ofrezca la hemodiálisis frecuente corta como una alternativa a la hemodiálisis convencional en el centro tres veces por semana, después de considerar las preferencias individuales del paciente, la calidad de vida potencial y los beneficios fisiológicos y el riesgo de esta terapia. (2C).
Guía 2.2. Recomienda que los pacientes que consideren la hemodiálisis frecuente corta en el centro sean informados sobre los riesgos de este tratamiento incluyendo un posible aumento en los procedimientos sobre el acceso vascular (1B) y en los potenciales episodios de hipotensión durante la diálisis. (1C).
Las guías 2.3 y 2.4 concernientes a hemodiálisis larga en domicilio se basan en los dos ensayos mencionados The Frequent Hemodialysis Network (FHN) Nocturnal Trial, y The Alberta Nocturnal Hemodialysis Trial. Dados los datos no conclusivos sobre su eficacia y el riesgo de mortalidad no hay recomendaciones firmes acerca de la hemodiálisis frecuente larga en domicilio, quedando así:
Guía 2.3. Se debe considerar la hemodiálisis larga en domicilio (6-8 horas, 3-6 noches a la semana) para los pacientes con enfermedad renal terminal que prefieren este tratamiento por su estilo de vida.
Guía 2.4. Recomienda que los pacientes que consideren este tipo de tratamiento sean informados sobre los riesgos de la técnica, incluyendo un posible aumento en las complicaciones relacionadas con el acceso vascular, y una posible pérdida de función renal residual acelerada. (1C).
Hemodiálisis en domicilio
La hemodiálisis intensiva en sus dos vertientes –frecuente corta y larga nocturna- puede realizarse en domicilio en los pacientes pediátricos, como así lo muestra el programa establecido en Toronto en el año 2000 con buenos resultados.
Se deben cumplir unos criterios estrictos para inclusión de los pacientes en este programa: En primer lugar, hay unos criterios que dependen de la propia unidad de hemodiálisis pediátrica (UHP) que prescribe el tratamiento como es tener incluida en su cartera de servicios la hemodiálisis en domicilio y poder proporcionar a los padres una adecuada formación con personal apropiado para ello, además de tener un sistema establecido de teleasistencia que garantice estar en comunicación con el paciente. Estos criterios son condición “sine qua non”, de tal forma que si no se cumplen, la UHP no debería ofrecer esta modalidad de tratamiento; además, el segundo criterio va dirigido a la elección del paciente que puede beneficiarse de la inclusión en este programa: pacientes que viven lejos del centro, que tienen una afectación cardiovascular derivada de una sobrecarga crónica de volumen con hipertensión arterial mal controlada o afectación cardiaca como hipertrofia ventricular izquierda; también serían subsidiarios aquellos con un mal control metabólico, alteraciones del metabolismo calcio-fósforo o mal crecimiento.
Normalmente estos pacientes vienen de estar varios años en situación de enfermedad renal crónica estadio V en tratamiento sustitutivo, bien trasplantados renales, o en programa de hemodiálisis convencional o en diálisis peritoneal. De entrada, esta modalidad de tratamiento no se ofrece al paciente que viene de una ERC estadio 4, en el que el orden habitual de sustitución de la función renal es trasplante anticipado, diálisis peritoneal y hemodiálisis en el centro.
Otro criterio a cumplir es que se prevea un periodo de estancia en hemodiálisis largo por no estar en condiciones de ser trasplantados a corto plazo. Este sería el caso de hipersensibilizados durante el estudio, afectación del estado de salud cardiovascular importante o dificultades anatómicas para el trasplante.
Es deseable tener un peso mínimo 18 a 20 kg, para que la volemia sea tal que el riesgo de complicaciones hemodinámicas durante la técnica sea mínimo.
Se debe tener un acceso vascular con un funcionamiento adecuado, sea fístula arteriovenosa o catéter venoso central.
Debe estar garantizado un soporte familiar psicosocial adecuado para llevar a cabo la técnica.
Hay pacientes en los cuales es especialmente interesante la asistencia a sus actividades diarias, como el escolar mayor o los adolescentes.
Una vez que hemos cumplido todos los criterios anteriores, se valora el domicilio y la habitación que será acondicionada para la técnica. Se evaluará la infraestructura de la vivienda, sobre todo, en el sistema eléctrico y agua. Es imprescindible una fuente eléctrica constante y fiable, y disponer de un sistema electrógeno.
Cuando decidimos poner en marcha la técnica, el esquema a utilizar es muy versátil. Dependiendo de los horarios del paciente, su asistencia al instituto, optaremos por una hemodiálisis frecuente corta, al llegar a casa, o bien una hemodiálisis larga nocturna, o una larga y frecuente. Principalmente la duración de las sesiones estará acorde con la necesidad de ultrafiltración según la ganancia interdialítica. Se intentará realizar una ultrafiltración lo más fisiológica posible, de tal forma que la tasa de ultrafiltración no debe exceder 1,5 + 0,5% del peso corporal por hora (no más del 5% del peso por sesión)
Las principales ventajas de la hemodiálisis en el domicilio son: la flexibilidad de horario que permite la asistencia escolar completa, la disminución de la sensación de mareo e hipotensión que tienen muchos pacientes la tarde de la diálisis, la liberalización de la dieta, y los efectos derivados de la frecuencia de las sesiones como son el mejor control de la tensión arterial y de la nutrición. Los mayores inconvenientes son: la dependencia de los cuidadores, en general de los padres, con la consiguiente carga para los mismos y riesgo de burnout; asimismo puede haber un Incremento de las complicaciones del acceso vascular y emergencias inesperadas.
Como conclusiones globales de este apartado de hemodiálisis intensiva diremos que hay cada vez más aportaciones al conocimiento en el campo de la hemodiálisis que indican que para mejorar la morbimortalidad de los pacientes en hemodiálisis hay que abandonar la pauta convencional de tres sesiones semanales y si necesitamos incrementar la dosis de diálisis debemos desplazarnos a esquemas de hemodiálisis intensiva.
Estas nuevas pautas permitirán un mejor control del volumen extracelular, hipertensión arterial e hipertrofia ventricular izquierda.
En el área pediátrica esta práctica hace que podamos proporcionar incrementar de manera sustancial la sustitución de la función renal, mejorando la situación global del paciente e incluso el crecimiento.
Debemos individualizar la pauta de hemodiálisis a cada paciente, teniendo en cuenta sus circunstancias: edad, distancia al Centro, circunstancias familiares, grado de función renal residual, situación cardiovascular, control de la tensión arterial y regulación del metabolismo calcio-fósforo.
HEMODIÁLISIS EN SITUACIONES ESPECIALES
Pacientes con hipoalbuminemia y edemas
La hemodiálisis en situaciones en las que hay una potencial disminución del volumen circulante efectivo pueden ser complicadas de realizar. Tal es el caso que se nos presenta por ejemplo en el síndrome nefrótico, cirrosis e insuficiencia cardíaca. La disminución del volumen circulante efectivo (VCE) pone en marcha el sistema fisiológico de retención de agua y sal con lo que se incrementa el volumen extracelular (VEC) y el sodio corporal total. Este mecanismo no es capaz de restaurar el VCE, con lo cual se genera un círculo que perpetúa la expansión del VEC. Como resultado, en la sesión de hemodiálisis debemos mantener una estabilidad hemodinámica que permita la realización de la técnica de forma adecuada y que permita prevenir la hipotensión derivada de la disminución del VCE, realizando una ultrafiltración individualizada para conseguir normalizar progresivamente la situación clínica de expansión del VEC.
Hay que tener en cuenta que, durante la sesión de hemodiálisis en un paciente renal, nosotros podemos actuar sólo en el compartimento vascular., de tal forma que a medida que se va retirando agua y sal de este compartimento, éste se va rellenando de agua y sal del espacio intersticial. Nuestra tarea es hacer coincidir la tasa de ultrafiltración con la de relleno del espacio vascular para que no haya una situación de hipotensión.
En situación de edema con hipoalbuminemia la tasa de relleno del compartimento intravascular puede verse comprometida y en tales circunstancias puede ser útil (por supuesto aparte de la valoración clínica, control de tensión arterial y frecuencia cardíaca) lo siguiente:
Monitorización de la volemia
La mayoría de los monitores disponen de un sistema de monitorización de volumen sanguíneo (BVM). A medida que la sesión avanza el monitor representa el volumen de sangre relativo (VRS) respecto a al volumen inicial que se establece en el 100%. De tal forma que podemos ajustar la UF deseada adecuándola al estado de volemia efectiva del paciente hasta un VRS crítico que establecemos previamente a partir del cual la ultrafiltración se detiene [23].
Ajuste del sodio del baño
Otra herramienta útil es modificar la concentración de sodio del baño diálisis, de tal forma que si aumentamos la concentración por encima de la natremia del paciente se producirá un incremento de la osmolalidad plasmática y como consecuencia una mayor tasa de relleno del espacio intravascular. Al principio de la sesión estableceremos un sodio base (“time averaged ”) calculado de tal forma que no se produzca una ganancia neta de sodio por difusión durante la sesión. A su vez se programará un perfil de más a menos en el tiempo, introduciendo el sodio máximo que deseamos al principio de la misma. Al tener una concentración de sodio base prefijada, automáticamente el software calculará el sodio mínimo a alcanzar al final de la sesión.
Perfusión de albúmina
En otro tiempo más utilizada, esta práctica está siendo abandonada debido a que los resultados a medio plazo pueden no ser los deseados; en efecto, aunque la albúmina tiene un efecto extensor rápido del espacio vascular y es eficaz combinada con ultrafiltración para el alivio sintomático del edema, su administración reiterada puede contribuir al mantenimiento del mismo, dada su difusión tardía al espacio intersticial.
En la primera y segunda hora durante las primeras sesiones se puede administrar a dosis orientativa 10 gramos de una solución al 20% (50 ml), lentamente. El incremento de presión oncótica que se obtiene mejora la tasa de relleno del espacio intravascular.
Pacientes con cardiopatía
Distinguimos, por un lado, la sesión de hemodiálisis a realizar en el paciente con cardiopatía congénita y por otro la hemodiálisis el paciente afecto de cardiopatía en el contexto de la enfermedad renal crónica.
Hemodiálisis en niños con cardiopatía congénita
Es fundamental la colaboración del cardiólogo pediátrico con quién se debe establecer la pauta de diálisis más adecuada y donde se debe prestar especial atención al manejo de la ultrafiltración más que la depuración, requiriendo en ocasiones diálisis cortas y frecuentes (véase diálisis intensiva) en especial cuando existe una insuficiencia cardiaca congestiva.
Hemodiálisis en niños con cardiopatía adquirida propia del enfermo renal
Los pacientes con enfermedad renal crónica avanzada estadio 4 y los que están en diálisis presentan varios factores de riesgo para la afectación cardiovascular: sobrecarga crónica de volumen e hipertensión arterial con repercusión cardiaca: hipertrofia ventricular izquierda o trastorno crónico de la contractilidad. En casos de mal control la afectación mantenida en el tiempo puede ser muy grave. A esto se puede añadir la afectación miocárdica en el contexto de un medio urémico y la calcificación vascular de la media de las arterias.
Estos pacientes son los que más se benefician de una hemodiálisis intensiva, entendiendo como tal la que aumenta el número de horas a la semana, bien incrementando la frecuencia de las sesiones o incrementado el número de horas por sesión. De hecho, en los tres ensayos clínicos realizados hasta la fecha, los dos del grupo FHN (Frequent hemodialysis Newark) y el realizado en Alberta, Canadá, se objetiva una mejoría de la hipertrofia ventricular izquierda.
Los beneficios de estas técnicas vienen dados por un mejor control del VEC, de hecho, el incremento del número de sesiones a la semana permite que la ganancia inter dialítica sea menor, así como un mejor control de la tensión arterial. Las sesiones largas permiten una tasa de UF más fisiológica, disminuyendo el riesgo de hipoperfusión miocárdica “stuning” que se asocia a las tasas muy elevadas de UF. No hay que olvidar, además, que un paciente mal dializado está en riesgo de afectación cardiaca derivada del ambiente urémico. En este sentido, la mejoría de la depuración es beneficiosa para el miocardio.
ASPECTOS ESPECÍFICOS DE LA HEMODIÁLISIS PEDIÁTRICA
En este punto vamos a hablar de aspectos concretos del manejo del paciente con ERC, pero enfocados específicamente a hemodiálisis.
Nutrición y hemodiálisis
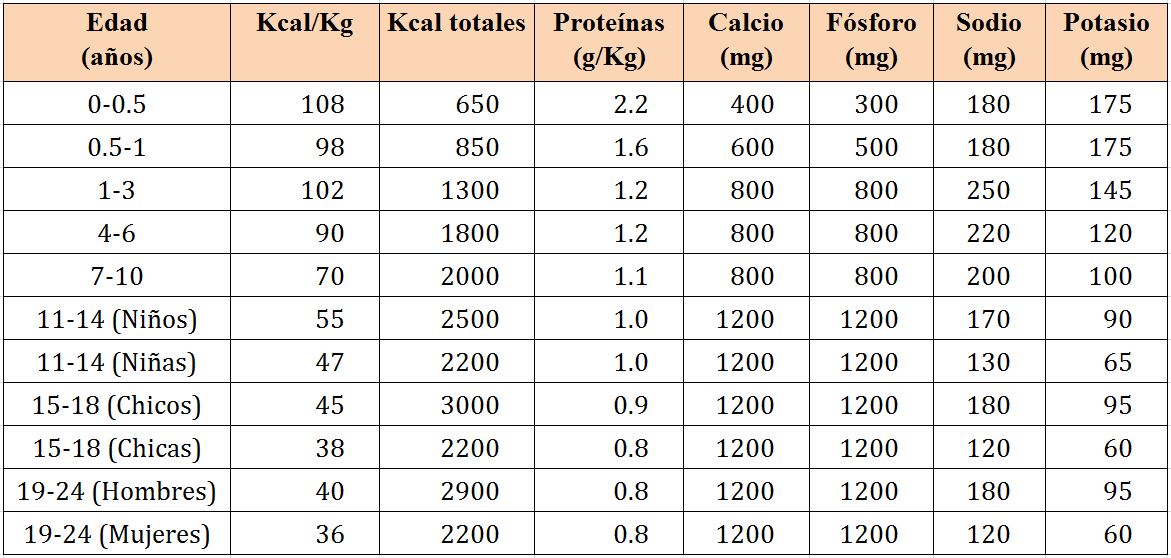
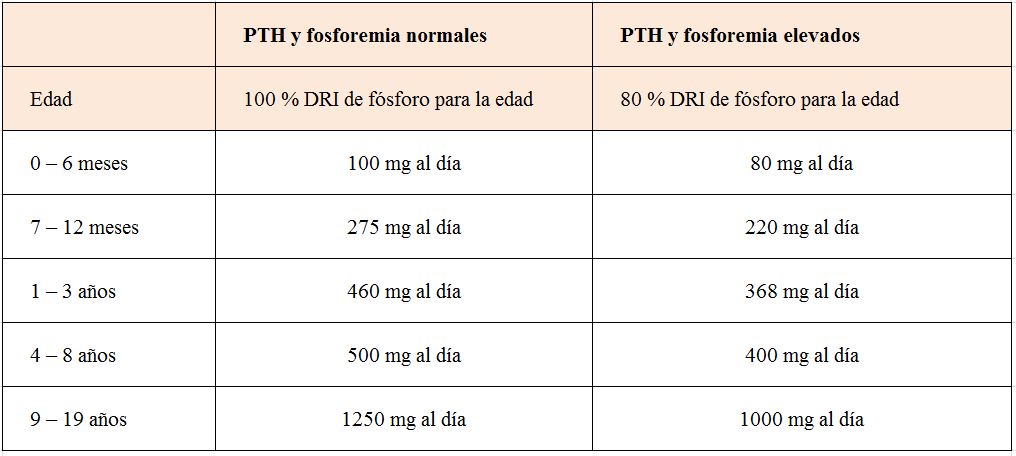
La nutrición es un aspecto fundamental de la enfermedad renal crónica y en especial de la hemodiálisis [24] [25] [26] [27]. Además, la dieta; al igual que la medicación y la dosis de diálisis debe ser un elemento prescriptivo; es decir debemos prescribir nutrición en niños en hemodiálisis. El aporte calórico al niño en hemodiálisis debe ser superior al 100% de la DRI para edad y sexo ajustados a su actividad física. Con frecuencia, sobre todo en lactantes y niños de corta edad, el estado de hiporexia por la insuficiencia renal hace necesario el empleo de sonda nasogástrica o de gastrostomía para asegurar la consecución de estos requerimientos. La distribución de las calorías entre hidratos de carbono, lípidos y proteínas no debería ser diferente al del resto de la población pediátrica. Los carbohidratos deberían comprender entre 45 - 65% del total de la ingesta calórica (DRI). Las grasas deberían comprender entre 25 - 35% de las calorías totales. El resto de calorías deberían ser proporcionadas en forma de proteínas.
La ingesta proteica no debería ser excesiva por su potencial contribución a la génesis de metabolitos nitrogenados y la hiperfosfatemia a la que siempre va ligado. Así pues, se recomienda que los niños en hemodiálisis reciban del 100 al 150% de las de DRI (Tabla 10). Las necesidades de electrolitos y agua pueden verse en la (Tabla 11).
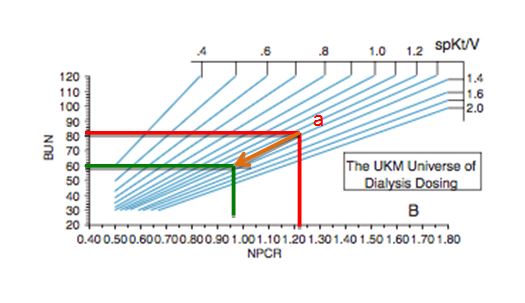
Los niños menores a tres años o aquellos con una talla por debajo del p3 requerirán una cantidad mayor de proteínas pudiendo ajustar el cálculo para la edad-talla en vez depara la edad cronológica. Además de la encuesta dietética, la ingesta proteica del niño en hemodiálisis puede ser valorada mediante el cálculo de la Tasa de Catabolismo Proteico Normalizada (Normalized protein Catabolic Rate, nPCR). Este parámetro es una medida objetiva de la ingesta proteica en pacientes estables en hemodiálisis, siempre que no exista un aumento del catabolismo endógeno asociado a infección, inflamación, malnutrición o tratamiento con esteroides. Se debe calcular de forma periódica en los niños en hemodiálisis, basándonos en el modelo cinético de la urea. Se calcula a partir de dos determinaciones de la concentración de urea (BUN), una al finalizar una sesión de hemodiálisis y la otra al principio de la siguiente. Los parámetros obtenidos se introducen en programas informáticos que hacen los cálculos. Uno de ellos es accesible a través de la red en la página “www.ureakinetics.org”. El cálculo de la nPCR añadido al BUN plasmático y el Kt/V nos permiten realizar una estimación objetiva de la situación nutricional del paciente (Figura 9).
Para saber si estamos haciendo las cosas bien los tres parámetros estarán bien correlacionados. Imaginemos por ejemplo como aparece en la gráfica que tenemos un paciente en hemodiálisis 6 meses. Inicialmente con una nPCR de 1.2, una Kt/V de 1.4 y un BUN de 80 mg/dl. Podemos ir dializando a este paciente a lo largo de 6 meses, pensando que estamos haciendo las cosas bien, con Kt/V por sesión de 1.3–1.4 y nuestro paciente presenta un buen aspecto, con un buen control y ganancia ponderal adecuada. Sin embargo, si hacemos las valoraciones adecuadas, con una representación gráfica correcta, veríamos que inadvertidamente nuestro paciente ha pasado da una situación a → b. Se ha ido desnutriendo y cambiando masa magra por agua, con una malnutrición y una inadecuada ingesta proteica.
La hemodiálisis frecuente se asocia con una mejor nutrición y velocidad de crecimiento. Así lo corrobora el grupo de Estrasburgo, con Fischbach [3] [4]. Aplica un programa de HDFOL frecuente corta en el centro. En su trabajo observacional prospectivo con 5 pacientes aprecia un incremento significativo en la velocidad de crecimiento, así como mejoría en el control de las cifras de tensión arterial, hipertrofia ventricular izquierda y un mejor control del fósforo.
El seguimiento de parámetros clínicos (presencia de anorexia y/o vómitos, encuesta dietética), somatométricos (peso, talla, velocidad de crecimiento, índice de masa corporal, pliegues cutáneos), bioeléctricos (agua corporal, agua extracelular y masas magra, grasa y celular) y bioquímicos (albúmina, prealbúmina leptina, transferrina, homocisteína y equivalente proteico de la dieta permite la detección precoz de alteraciones nutritivas. Por su simplicidad y gran valor clínico la determinación de estos parámetros en cada visita ayuda a prevenir la malnutrición, que podría condicionar por sí misma lesiones irreversibles.
Anemia y hemodiálisis
La corrección de la anemia mejora el riesgo cardiovascular, así como, la actividad física, la función cardíaca, el apetito, la asistencia escolar y la calidad de vida.
Las guías KDIGO de 2012, sobre la anemia en niños con ERC [28]; definen anemia cuando la hemoglobina es inferior a 11.0 g/dl en menores de 5 años y menor de 12.0 g/dl en mayores de 12 años. A partir de los 15 años se consideren valores como en adultos; es decir, en los varones hemoglobina menor de 13.0 g/dl y en mujeres menor de 12 g/dl. En cuanto al metabolismo del hierro para pacientes en dialisis se recomiendan valores de ferritina mayores de 200 ng/ml, siendo 100 ng/ml el límite inferior de lo normal en pacientes en ERC no en dialisis. En varias guías clínicas se ha establecido 500 ng/ml como límite superior de la normalidad que marcaría el riesgo de sobrecarga férrica/toxicidad sobre la cual el tratamiento con parenteral con hierro no se recomienda. De todas formas, esta recomendación no está basada en la evidencia. El índice de saturación de la transferrina (IST) del 20% es el umbral de ferropenia por debajo del cual se debe iniciar ferroterapia.
Con los hemogramas automatizados actuales, en la práctica clínica habitual, podemos encontrar dos parámetros que nos van a ayudar para detectar situaciones de ferropenia: el primero de ellos es el porcentaje de glóbulos rojos hipocromos, definido como el porcentaje de eritrocitos que tienen un VCM inferior a 28 g/dl, siendo los pacientes que tienen un porcentaje superior al 6% son los que se beneficiarán del tratamiento con hierro intravenoso. El segundo de los parámetros es el contenido de hemoglobina reticulocitaria. Una reducción en este parámetro es el indicador más sensible de deficiencia funcional de hierro. Se ha establecido el dintel de ferropenia en 29 pg/célula.
La combinación de ambos parámetros: un porcentaje de hematíes hipocromos > 6% junto con un contenido de hemoglobina reticulocitaria < 29 pg/célula es el mejor índice para detectar la deficiencia de hierro basado en la respuesta de hemoglobina al tratamiento con hierro intravenoso (Tabla 12).
Metabolismo del hierro y ferroterapia en hemodiálisis
La ferropenia es muy frecuente en los pacientes en hemodiálisis, tanto absoluta, con depósitos de hierro bajos en el organism0 como funcional, por mala utilización de los mismos. Las causas son:
Pérdidas por sangrado crónico por disfunción plaquetaria, flebotomías, pérdidas en filtro de diálisis.
Menor ingesta
Mayor demanda en pacientes tratados con agentes estimuladores de eritropoyesis.
Fármacos: captores de fósforo, antiácidos.
Elevación de Hepcidina: Péptido sintetizado en el hígado que juega un importante papel en la homeostasis del hierro. Está elevada en inflamación crónica y en insuficiencia renal produciendo una ferropenia funcional.
Los pacientes que llegan a hemodiálisis por deterioro progresivo de su ERC, reciben habitualmente tratamiento con hierro oral, habitualmente sales de hierro, principalmente en su forma ferrosa. En niños la dosis es 5 -6 mg/Kg. /día, según tolerancia, con un tope, la dosis de adultos de 200 mg al día, repartida cada 12 horas. Se absorben mal en los pacientes urémicos, con alta incidencia de efectos gastrointestinales (Tabla 13).
En la actualidad existe el consenso generalizado de que la ferroterapia oral es insuficiente para las de cubrir las necesidades de la eritropoyesis estimulada por EPO en los pacientes en hemodiálisis. Estudios de revisión sistemáticos y metaanálisis han mostrado que la respuesta en cuanto al ascenso de la hemoglobina es mucho más potente con la ferroterapia intravenosa que oral. Las guías KDIGO recomiendan la utilización de hierro intravenoso si queremos un incremento de la concentración de hemoglobina o una disminución de los requerimientos de EPO siempre y cuando la ferritina sea< 500 ng/ml e IST < 30%.Hay varias preparaciones de hierro para administración parenteral. La mayoría contienen hierro asociado a una capa envolvente de carbohidratos (Tabla 14)
La forma más frecuente de administrar hierro intravenoso es el hierro sacarosa. La dosis inicial de administración intravenosa se calcula por la fórmula de Ganzoni:
Déficit de hierro (mg) = peso (Kg.) x [hemoglobina diana (g/Dl.) – hemoglobina actual (g/Dl.)] x 2,4 + depósito de hierro (500 mg si peso > 35 Kg. o 15 mg/kg si menor).
Imaginemos un paciente con Peso 23 kg, hemoglobina 9.6 g/Dl. al que deseamos subir la hemoglobina a 11.5 g/dl y está ferropénico.
Aplicando la fórmula tendríamos: cantidad de hierro a administrar (mg) = 23 x [11.5 – 9.6] x 2.4 + [15 x 23] = 104.88 + 345 = 449.88 ¿ 450 mg.
Esta sería la dosis dotal a administrar. Una ampolla de hierro sacarosa, Feriv® o Venofer® tiene 5 ml con 100 mg de hierro elemento.
Por lo tanto, administraremos 0.15 ml/Kg. (3 mg/kg) y dosis = 0.15 ml x 23 kg = 3.45 ml ¿ 3.5 ml (70 mg). En total 450 mg / 70 mg = 6.4 = 6 administraciones. Se pueden inyectar una vez por semana hasta completar las 6 dosis. (Diluir 100 mg, una ampolla, hasta 100 ml de SF. Pasar como mínimo en 15 minutos)
Una vez realizada la administración de carga para rellenar depósitos, iniciaremos la dosis de mantenimiento, que ha sido valorada en estudios en hemodiálisis pediátrica, con dosis de 0.5, 1.0, o 2.0 mg/kg cada dos semanas.
Finalmente deberíamos llamar la atención en cuanto a que todas las preparaciones de hierro intravenoso presentan riesgo de reacción de hipersensibilidad inmediata, con hipotensión y nauseas. Normalmente son muy poco frecuentes si se tiene la precaución de una correcta administración, ya que son “infusión-dependientes”, dependientes de dosis total y de tiempo de administración; además el hierro dextrano, escasamente utilizado en la actualidad, tiene el riesgo de anafilaxia por la formación de anticuerpos. Otros efectos secundarios potenciales, la susceptibilidad incrementada a las infecciones y al estrés oxidativo.
Agentes estimulantes de la eritropoyesis (AEE)
Actualmente se utilizan la epoetina (EPO) alfa y beta con sus posteriores modificaciones para aumentar la vida media: darboepoetin alfa y metoxi-polietilenglicol epoetin beta, también llamada “continuous erythropoietin receptor activator” (CERA).
La EPO se puede administrar vía subcutánea o intravenosa. La biodisponibilidad de la EPO subcutánea es el 20 – 30% pero a cambio tiene una vida media prolongada (8 h intravenosa¿ 18 h subcutánea), que permite administrarla en menos pinchazos. La dosis requerida para mantener la misma hemoglobina es un 30% menor con administración subcutánea. La dosis inicial es de 100–150 UI/kg/semana, administrada 2 – 3 veces por semana. Se administrará iv al final de la sesión de hemodiálisis.
La Darboepoetin Alfa, modificación de la molécula EPO alfa hace que su vida media tras administración iv se triplique (8.5 horas a 25.3 horas). Si se administra subcutánea pasa a 43 horas. Se puede administrar cada semana o cada 2 semanas. La dosis requerida es la misma para la vía iv que la subcutánea. Para la conversión EPO en Darboepoetina se utiliza la regla 200:1, pero puede haber mucha variabilidad.
La Metoxi-polietilenglicol epoetin beta, también llamada “continuous erythropoietin receptor activator” (CERA). Tiene una vida media de 130 horas, tanto si es administrada vía iv o vía subcutánea. Se administra una vez al mes.
Aunque en general deberíamos conseguir la hemoglobina media correspondiente a la edad y sexo del paciente, algunas guías clínicas aconsejan no superar los 12 gramos/dl. Normalmente en pacientes con unos depósitos de hierro adecuados se produce un incremento de 1 – 2 g/dl al mes. Si no sucede, deberíamos incrementar la dosis un 25%.
Entre los efectos adversos de los AEE se puede observar un incremento moderado de la tensión arterial y una tasa incrementada de eventos tromboembólicos. Se debe utilizar siempre la mínima dosis eficaz.
Regulación del volumen extracelular mediante ultrafiltración. Hipertensión arterial y hemodiálisis
En este punto es importante tener en cuenta tres aspectos del paciente:
1) Edad del paciente. Lactante, preescolar, escolar, adolescente.
2) Función renal residual, diuresis residual.
3) Patología renal de base.
Hay dos diferentes poblaciones de niños en hemodiálisis con comportamiento distinto con respecto al manejo del agua y la sal: por un lado, tenemos al paciente pequeño, preescolar, con una nefropatía malformativa que suele conservar diuresis, con tendencia a la poliuria y con natriuresis incrementada. Por otro lado, el paciente escolar o adolescente que puede tener una glomerulopatía de base con escasa función renal residual y diuresis, con tendencia a la retención hidro salina e hipertensión arterial. Entre ambas poblaciones hay casos intermedios.
En el primer grupo, el paciente pequeño, preescolar, con diuresis residual correcta y natriuresis incrementada, las entradas en la dieta son más elevadas y permisivas hasta cierto punto. Suelen tener una alimentación mucho más líquida; padecen una poliuria-polidipsia “de siempre” y muchos han llevado suplementos de cloruro sódico para no entrar en balance negativo de sodio lo que impediría el correcto crecimiento. De todas formas, hay que tener en cuenta que en fases tan avanzadas de ERC las sobrecargas de sal dietéticas no se toleran como en fases más precoces de ERC y deberemos ajustarlas. Las “salidas” son principalmente por la diuresis residual con natriuresis incrementada. Es uno de nuestros objetivos que el paciente mantenga esta función residual en el tiempo de forma lo más prolongada posible. Ajustaremos la ultrafiltración con tendencia a la mínima necesaria o ninguna. Es más, alguno de estos pacientes pudiera necesitar inicialmente la adición de sueros salinos durante las primeras sesiones con objeto de mantener la tolerancia.
El segundo grupo de pacientes es el que ha entrado en diálisis con poca función y escasa diuresis residual; tiene tendencia a una mayor ganancia de peso interdialítica y está hipertenso si no cuida su ingesta. Para establecer el peso ideal del paciente tenemos varias aproximaciones. La primera y principal es por la clínica: edema, presencia de hipertensión arterial, uso de fármacos para el control de la misma nos orientan a una disminución del peso seco. Hipotensiones durante la sesión nos orienta a aumentar el peso seco. Cuanto mayor es un paciente, más difícil es valorar la sobrecarga hídrica desde el punto de vista clínico.
Para estimar el peso seco del paciente nos podemos ayudar de otras formas: una, mediante el uso de la bioimpedanciometría.; en ese sentido, actualmente disponemos de aparatos como el BCM “Body Composition Monitor” de Fresenius que nos proporciona 3 parámetros que son la Sobrehidratación, Cantidad de masa magra y Cantidad de masa adiposa; además disponemos del agua corporal total (ACT) que es equivalente al volumen de distribución de la urea (V). La segunda, valorando periódicamente la adecuación (cinética de la urea) de las sesiones de hemodiálisis y haciendo una gráfica con tres parámetros, nPCR – BUN – Kt/V de manera evolutiva. De esta forma podemos darnos cuenta si un paciente está perdiendo masa magra siendo sustituida por agua. En ocasiones hemos visto pacientes adolescentes o escolares mayores en hemodiálisis que pensábamos estaban correctamente nutridos e hidratados y que al ser trasplantados pierden toda el agua y la sal que les sobra evidenciando estado de nutrición.
Balance entradas y salidas de fluidos dependientes de la técnica
SALIDA: LA TASA DE ULTRAFILTRACIÓN ÓPTIMA
Sabemos que las Guías Europeas recomiendan una tasa de UF que no exceda el 1.5 + 0,5% del peso corporal por hora (en teoría no más del 5% del peso por sesión).Esto tiene un doble motivo: por un lado, el mantenimiento de la función renal residual de tal forma que cuanto más agresiva sea la pauta de UF, más riesgo tenemos de perder función residual y por otro, aunque el paciente tolere pautas agresivas de UF, se ha visto una relación directa entre tasas de UF elevadas y el desarrollo de patología cardiovascular, que sabemos es la causa de mortalidad más frecuente en los pacientes en hemodiálisis.
ENTRADAS: EL SODIO EN EL BAÑO DE DIÁLISIS
Hay que evitar que el sodio del baño de diálisis esté por encima del sodio del paciente. Si esto ocurre habrá una difusión hacia el paciente y un balance positivo del mismo en las horas de la técnica. Así el paciente incrementará su sensación de sed lo que producirá mayor ingesta de agua y ganancia de peso interdialítica. Si hacemos un perfil de sodio a lo largo de la sesión ajustado para el paciente, prescribiremos inicialmente un sodio base, un promedio de la concentración de sodio para dicha sesión. A partir de ahí se programa un perfil de sodio deseado, de más a menos en el tiempo, introduciendo el sodio máximo que deseamos al principio de la misma. Al tener una concentración de sodio base prefijada, automáticamente el software calculará el sodio mínimo a alcanzar al final de la sesión.
PAPEL DE LAS TÉCNICAS DE HEMODIÁLISIS INTENSIVA
Las pautas de hemodiálisis intensiva, tanto la hemodiálisis frecuente como la larga son muy eficaces a la hora de manejar al paciente con sobrecarga crónica de volumen. En los ensayos clínicos realizados ambas técnicas consiguen una mejoría evidente, influyendo de forma positiva en el control de la tensión arterial y de la hipertrofia ventricular izquierda.
Alteraciones del metabolismo mineral y óseo asociadas a la ERC
En la evaluación de estas anomalías y su tratamiento nos basamos en tres guías de práctica clínica, que ordenadas según el año de publicación son: guía de práctica clínica de KDOQI específica para CKD-MBD pediátrica de 2005 [29] guía europea específica para CKD-MBD de 2006 [30] guía de práctica clínica de KDIGO para CKD-MBD de 2017 [31].
Las guías KDOQI de 2005 sugieren que los niveles séricos de calcio, fósforo, CO2total, fosfatasa alcalina y PTH sean medidas en todos los pacientes con enfermedad renal crónica estadio 2-5. En los pacientes en hemodiálisis se deben evaluar de forma mensual los niveles séricos de calcio, fósforo y CO2total, y cada 3 meses fosfatasas alcalinas y PTH. Las guías europeas recomiendan que la monitorización de los 5 parámetros sea mensual.
Basándonos en la clínica –crecimiento, anomalías esqueléticas- y en las determinaciones analíticas de estos cinco parámetros descritos actuaremos para minimizar las complicaciones en el hueso y prevenir la calcificación extra esquelética. Intentaremos conseguir los siguientes objetivos [32]:
1) Mantener los niveles de calcio y fósforo séricos cerca de la normalidad.
2) Prevenir la hiperplasia de paratiroides y mantener la PTH en niveles apropiados.
3) Evitar el desarrollo de calcificaciones extra esqueléticas.
Fósforo y diálisis
En ERC 5 el fósforo sérico debe mantenerse entre 4–6 mg/dl en niños de 1 a 12 años y entre 3,5 – 5,5 mg/dl en adolescentes. Hay que valorar la ingesta de fósforo, y según las guías KDOQI de nutrición pediátrica en ERC, restringir los aportes. Si la PTH y el fósforo sérico están normales, seguiremos con el 100% del DRI para la edad (Tabla 15). Si la PTH y el fósforo sobrepasan el rango apropiado aportaremos el 80% de la DRI.
Los captores o quelantes del fósforo son necesarios casi de forma universal en los pacientes en hemodiálisis. Aún hoy día está controvertido cuál es el captor de fósforo ideal. Se deben tomar 10–15 minutos antes de las comidas. Todos los captores tienen la capacidad de aumentar la absorción de calcio al aumentar la disponibilidad de calcio que puede difundir a nivel de intestino. La capacidad de captar fósforo es limitada (1 g de carbonato cálcico 39 mg de fósforo, 400 mg de Sevelamer 32 mg de fósforo).
Los captores de fósforo de base cálcica son efectivos y relativamente baratos pero su administración con lleva un balance positivo de calcio y riesgo de hipercalcemia, especialmente cuando se administra junto con análogos de la vitamina D. Por este motivo se ha propuesto que la ingesta total cálcica al día incluyendo la fuente dietética y medicinal se limite a un máximo de dos veces el DRI de calcio para la edad y en el adulto 2500 mg.
Los captores de fósforo no cálcicos actualmente están fundamentalmente representados por el Sevelamer en su forma hidrocloruro o en su forma carbonato. El Sevelamer es captor de varios fármacos incluyendo furosemida, ciclosporina y tacrolimus. Asimismo, durante su tratamiento se ha visto que el colesterol total y el colesterol LDL disminuye un 20 a 30%, y a la vez el colesterol HDL tiende a aumentar.
En cuanto al papel de la hemodiálisis en el control de la fosforemia, hay que considerar que atodos los efectos el fósforo que es una molécula pequeña puede ser considerado como una molécula mediana ya que la transferencia desde los tejidos a la sangre es muy lenta y se encuentra en sangre en su forma hidratada. Debido a estas características la cinética del fósforo en hemodiálisis se parece más a la de las moléculas medianas que a las moléculas pequeñas. El aclaramiento de fósforo en hemodiálisis ocurre en dos fases. Durante la primera los niveles de fósforo en sangre caen. Tras 90 minutos aproximadamente tienden a estabilizarse e incluso pueden empezar a elevarse a lo largo del tratamiento, por la movilización desde otros pools. Como resultado se mantiene un gradiente de concentración importante a lo largo de toda la diálisis incluso en tratamientos prolongados. Esta es la causa del aclaramiento continuado de fósforo lo largo de la diálisis incluso cuando los niveles de urea en sangre han caído y el aclaramiento de urea es mínimo.
El mal control de la fosforemia en pacientes en hemodiálisis convencional es un criterio para el cambio a una modalidad de hemodiálisis intensiva. Los tres grupos que tienen programas de hemodiálisis intensiva en niños el de Berlín - hemodiálisis larga en el centro de diálisis, tres veces por semana-, el de Toronto - programa de hemodiálisis larga y frecuente, 8 horas, 6-7 días a la semana, en casa- y el de Estrasburgo - hemodiafiltración online frecuente corta en el centro- así lo corroboran.
Vitamina D y sus análogos y diálisis
En cuanto a la vitamina D las guías KDOQi recomiendan iniciar tratamiento con colecalciferol o ergocalciferol cuando los niveles bajan de 30 ng/ml (75 mol/l).
Hay discrepancia entre los valores óptimos de PTH que hay que mantener en niños en hemodiálisis; así mientras las guías pediátricas de 2005, KDOQI recomiendan un rango de 3 a 5 veces el superior de lo normal (que suele ser para los kits actuales de detección de PTH 65 pg/ml), por tanto 200 – 300 pg/ml; las europeas señalan que los valores idóneos serían de 2 a 3 veces superior, es decir: 130 – 190 pg/ml.
Los análogos de la vitamina D: Calcitriol y su precursor Alfacalcidol, y el sintético Paricalcitol deberían iniciarse como tratamiento en niños en hemodiálisis tras cumplir los pasos previos:
1) Niveles de 25 (OH) Vitamina D > 30 ng/ml.
2) PTH por encima de rango (>300 pg/ml).
3) Calcio sérico < 10 mg/dl.
4) Fósforo sérico < límite superior de lo normal para la edad.
Podemos iniciar tratamiento con Alfacalcidol (Etalpha gotas, 1 gota = 0,1 microgramo; 1 ml = 20 gotas = 2 microgramos) o Calcitriol (Rocaltrol, cápsulas de 0,25 y 0,50 microgramos). En teoría son equivalentes microgramo a microgramo. En cuanto al Paricalcitol (Zemplar, cápsulas de 1 microgramo) la equivalencia es calcitriol-paricalcitol = 0,5 mg–2 mg.
En pacientes mayores de 20 kg podemos iniciar tratamiento con cápsulas de Rocaltrol e ir titulando; en menores, iniciar con Etalpha gotas de más fácil cumplimentación y ajuste fino.
Una vez iniciado tratamiento con análogos de la vitamina D se debe monitorizar las concentraciones séricas de calcio, fósforo y PTH.
La dosis debe ser disminuida o incluso suspendida si hay hipercalcemia o disminución de la PTH por debajo del rango aconsejable (< 100 ng/ml). Por debajo de estas cifras existe el riesgo de enfermedad ósea adinámica, situación clínica indeseable a todas luces por la patología ósea que produce y el riesgo de calcificación extra esquelética. Asimismo, la hiperfosfatemia es indicación para disminuir la dosis e intensificar el uso de captores de fósforo, así como intensificar la restricción dietética de fósforo.
El Paricalcitol es un análogo de la vitamina D más selectivo, en teoría no produce hiperfosfatemia ni hipercalcemia como Alfacalcidol y Calcitriol.
Calcimiméticos y diálisis
El Cinacalcet es un calcimimético que suprime la secreción de la PTH y disminuye el disco de hipercalcemia asociado con calcitriol. Es muy efectivo en el tratamiento del hiperparatiroidismo secundario y ha hecho que la tasa de paratiroidectomías se haya reducido de forma drástica. Su uso está limitado en pediatría y debe ser utilizado con cautela previo consentimiento informado.
Calcio y diálisis
El calcio sérico total debe mantenerse en el rango normal para la edad, generalmente entre 8.8 y 9.7 miligramos decilitro. Si se produce hipercalcemia, con calcio mayor a 10.2 miligramos por decilitro, la dosis de captores cálcicos debería ser reducida/combinada/cambiada Sevelamer. La vitamina D nativa, así como los análogos de la vitamina D deberían ser paradas hasta que la calcemia retornara a la normalidad.
Concentración de calcio en el baño de diálisis
Las concentraciones de calcio del dializado varían de 1 a 3,5 mEq/l. La concentración 2,5 mEq/l (1,25 mMol/l) es la fisiológica y permite que el paciente dializado con este baño esté en un balance neutro de calcio durante la sesión. Mientras que por debajo de 2,5 mEq/l, el calcio se elimina del paciente, por encima de este valor el calcio difunde hacia el paciente. Aunque históricamente, los pacientes han sido dializados con una mayor concentración de calcio (3-3,5 mEq/l) para ayudar a controlar el hiperparatiroidismo y para prevenir el balance negativo de calcio, el reconocimiento del papel del calcio en la calcificación vascular ha hecho que el comité KDOQI recomiende una concentración de calcio de dializado de 2.5-2.6 mEq/l.
Prevención de la calcificación vascular en niños en diálisis
La enfermedad cardiovascular es la causa principal de mortalidad de niños y adultos con ERC. Se ha visto que pacientes jóvenes en diálisis (20 a 30 años) presentan la misma tasa de mortalidad por enfermedad cardiovascular que los pacientes de 80 años en la población general. Este proceso empieza en la niñez. Hay cambios en el grosor de la arteria carótida que aparecen en niños en estadios tempranos de ERC (ERC2). Desde el punto de vista patológico se caracteriza por la calcificación de la túnica media de las arterias. La normalización del metabolismo mineral (evitar hipercalcemia, hiperfosfatemia, disminuir la ingesta de calcio, evitar la enfermedad ósea adinámica) es efectiva para retrasar la progresión de la calcificación cardiovascular en pacientes con ERC y aquellos que están en hemodiálisis).
CRECIMIENTO Y HEMODIÁLISIS
Para lograr que los niños en hemodiálisis crezcan bien y alcancen una talla adulta adecuada, la actuación médica debe venir desde mucho antes, de los cuidados proporcionados desde la etapa inicial de ERC; efectivamente hay una fase de prevención de la pérdida de crecimiento potencial en las etapas iniciales que es básico para conseguir una talla final adecuada.
En los dos primeros años de vida, periodo de lactante un niño sano crece 30 – 35 cm; posteriormente, el periodo de crecimiento prepuberal 4 – 6 cm/año, y finalmente el periodo de crecimiento puberal en el cual el pico de velocidad de crecimiento alcanza 8 – 14 cm/año. Para que el crecimiento del niño con ERC sea correcto y no se pierda potencial de crecimiento aplicaremos las medidas que ya se han abordado en el curso con anterioridad “Módulo V, Enfermedad renal crónica. Tema 3, manifestaciones clínicas. Tratamiento conservador de la ERC, Tema 4, nutrición del niño con ERC y Tema 5, alteraciones del metabolismo mineral y óseo asociadas a la ERC”.
Los elementos presentes en la ERC que influyen el crecimiento y que, aunque también guardan una relación directa con la técnica deben estar ya presentes en el esquema terapéutico de la ERC son:
1. Vigilancia de los aportes nutritivos que proporcionen un aporte calórico y proteico adecuado. Es el factor más importante para la fase de crecimiento los dos primeros años de vida, pasando a ser un factor permisivo para el crecimiento en la fase de crecimiento prepuberal.
2. Corrección de las pérdidas de agua y sodio con suplemento a los niños con poliuria y pérdida salina.
3. Corrección de la acidosis metabólica.
4. Corrección de las alteraciones del metabolismo mineral y óseo asociadas a la ERC.
5. Corrección de la anemia.
Aun así, salvo con el enfoque agresivo nutricional en los dos primeros años de vida, ninguna de las medidas ha demostrado producir un “catch-up” importante en los niños con ERC.
Papel de la hemodiálisis en el crecimiento del niño con ERC
La hemodiálisis convencional no mejora el crecimiento en los pacientes urémicos. Más bien al contrario. Se ha visto que hay una pérdida de talla, que puede llegar a ser hasta 1 SDS por año. En un artículo en el cual se mide el crecimiento en 94 pacientes adolescentes en hemodiálisis seguidos durante 3 años se apreció un descenso del SDS para la talla desde -1.97 a –2.36. En otro realizado en lactantes en hemodiálisis que agrupaba un total de 9 niños, el SDS para la talla pasó de -0.61 a los 9 meses de edad, a -1.61 al finalizar su etapa en hemodiálisis 27 meses después. Los niños que mantienen función renal residual crecen mejor que los que no.
La hemodiálisis intensiva sí mejora el crecimiento de los niños en diálisis. Así lo ha demostrado Fischbach y su grupo en Estrasburgo. En el artículo publicado en el año 2010, relata como 15 pacientes que estaban en programa de hemodiálisis convencional tres días por semana y que recibían tratamiento con HGH fueron cambiados a un esquema de hemodiafiltración frecuente en el centro. Los resultados en cuanto al crecimiento fueron espectaculares, apreciando un incremento de la velocidad de crecimiento el primer año de 3.8 a 14.3 cm/año lo que produjo un completo catch-up, de -1.5 a + 0.2 en el Z score para la talla.
Tratamiento con hormona de crecimiento (GH) en hemodiálisis
En un informe del 2007 del “North American Pediatric Renal Trials and Collaborative Studies” (NAPRTCS) se apreció un beneficio del uso de GH en pacientes con ERC. En el análisis por grupos de pacientes, prepúberes vs púberes y ERC 2–4 vs ERC 5D vs trasplante, aprecian que el grupo que mejor fue es el de prepúberes, ERC II–IV [33].
En los artículos publicados por el grupo alemán (The German study group for growth hormone treatment in chronic renal failure) se refleja que, aunque la respuesta de estos niños era inferior a la de los niños en ERC 2- 5, se apreciaba un efecto positivo del tratamiento con un incremento en la velocidad de crecimiento de 2,6 a 3,5 cm/año durante el primer año de administración sobre la velocidad de crecimiento basal al inicio del tratamiento. Aunque la velocidad de crecimiento disminuyó en los años siguientes, pero permaneció por encima de la basal [34] [35] [36] [37].
En el informe de NAPRTCS del año 2011 los pacientes en diálisis tratados con GH fueron comparados con pacientes no tratados tras 12 meses de diálisis. Los niños que recibían GH en el grupo menor de seis años presentaron un incremento de 0,63 SDS en Z score frente a +0,01 en el grupo sin tratar. Los niños mayores de seis años un presentaron un incremento algo menor que en el otro grupo que fue de 0,26 frente a -0,1 SDS los no tratados.
Los efectos sobre el crecimiento que deberíamos esperar en niños en hemodiálisis tratados con GH serían los siguientes [38] [39] [40] [41]:
1. Un incremento en la velocidad de crecimiento, mayor en los primeros años del tratamiento.
2. Una mejor respuesta al tratamiento cuanto menor sea la edad al inicio, mejor sea la función renal residual y mejor sea la talla diana.
3. Un efecto positivo en la talla final, como se ha visto en cohortes de pacientes tratados durante 5 años. En su eficacia final se han mostrado influyentes los siguientes factores: de forma positiva, el Z score de la talla al inicio del tratamiento, la duración total del tratamiento con GH y de forma negativa el grado filtrado glomerular, la pubertad retrasada y la mayor edad al inicio del tratamiento.
La GH debe iniciarse lo más precozmente posible en el momento en que detectamos un retraso del crecimiento y después de corregir las alteraciones previamente descritas no se logra el objetivo de crecimiento deseado. La dosis de tratamiento es de 0,045 a 0,05 mg/kg/día (equivale a 4 UI/m2), administrado de forma subcutánea y diaria. El primer efecto observable es que la velocidad de crecimiento supera en 2 cm/año a la velocidad basal previa al inicio del tratamiento.
En cuanto a los efectos secundarios posibles, debemos vigilar la hipertensión intracraneal benigna o pseudo tumor cerebri, el deslizamiento de la epífisis femoral y el empeoramiento de escoliosis que tuviera previamente el paciente. Además, deberíamos continuar con los controles somatométricos, valoración del estado nutricional, estudio de fondo de ojo, y controles seriados de glucosa, electrolitos, calcio, fósforo, PTH y edad ósea.
COMPLICACIONES DURANTE LA SESIÓN DE HEMODIÁLISIS.
Hipotensión
Pese a una correcta valoración del peso seco y un adecuado perfil de ultrafiltración, la hipotensión es la complicación más frecuente de las sesiones de hemodiálisis. Las manifestaciones clínicas pueden ser difíciles de valorar en lactantes y niños pequeños, por lo que se recomienda monitorizar la presión arterial y la frecuencia cardíaca de forma continua. Durante la hipotensión debe interrumpir la ultrafiltración, poner al paciente en posición de seguridad, y Trendelemburg, y administrar la cantidad mínima necesaria de suero fisiológico para remontar la clínica.
Síndrome de desequilibrio
El cambio osmolar rápido que acompaña a las primeras sesiones puede producir el síndrome neurológico denominado de desequilibrio, caracterizado por náuseas, vómitos, cefalea, hipertensión, y en algunos casos convulsiones. Para minimizar el riesgo, durante las primeras sesiones de diálisis y en pacientes con valores de nitrógeno ureico en sangre (BUN) superiores a 100 mg/dl, se recomiendan aclaramientos de urea de 1.5 a 2 ml/kg (Kt/V por sesión 0.6 a 0.8) y la administración preventiva de manitol, 0,5 g/kg de peso.
Hemólisis
Puede manifestarse clínicamente con dolor precordial o dolor dorso lumbar. Ante esta clínica debemos descansar hemólisis porque si no es reconocida de forma precoz puede desencadenar una hiperpotasemia grave. Otros datos que sugieren hemólisis son el color como el vino de la sangre en la línea de retorno, caída del hematocrito y color rosa del plasma en una muestra de sangre. Si sospechamos hemólisis la diálisis debe ser parada inmediatamente, interrumpir el retorno sanguíneo al paciente y tratar la hiperpotasemia y la anemia que puede ser potencialmente graves. Además, el paciente debe ingresar para observación por riesgo de hiperpotasemia tardía.
Embolismo gaseoso
Es una complicación rara por la presencia de detectores de aire en los monitores. Desde el punto de vista clínico puede cursar con dolor torácico y disnea. Si el paciente está sentado la clínica puede ser neurológica porque el aire tiene tendencia a ir al sistema venoso cerebral. Si el paciente está tumbado el aire tiende a ir a los pulmones desde el corazón, con clínica de disnea y tos. El tratamiento consiste en clampaje inmediato de la línea venosa y parada inmediata de la bomba de sangre. El paciente se debe tumbar sobre su lado izquierdo en decúbito supino en Trendelemburg y se debe administrar oxígeno al 100 %.
Tablas
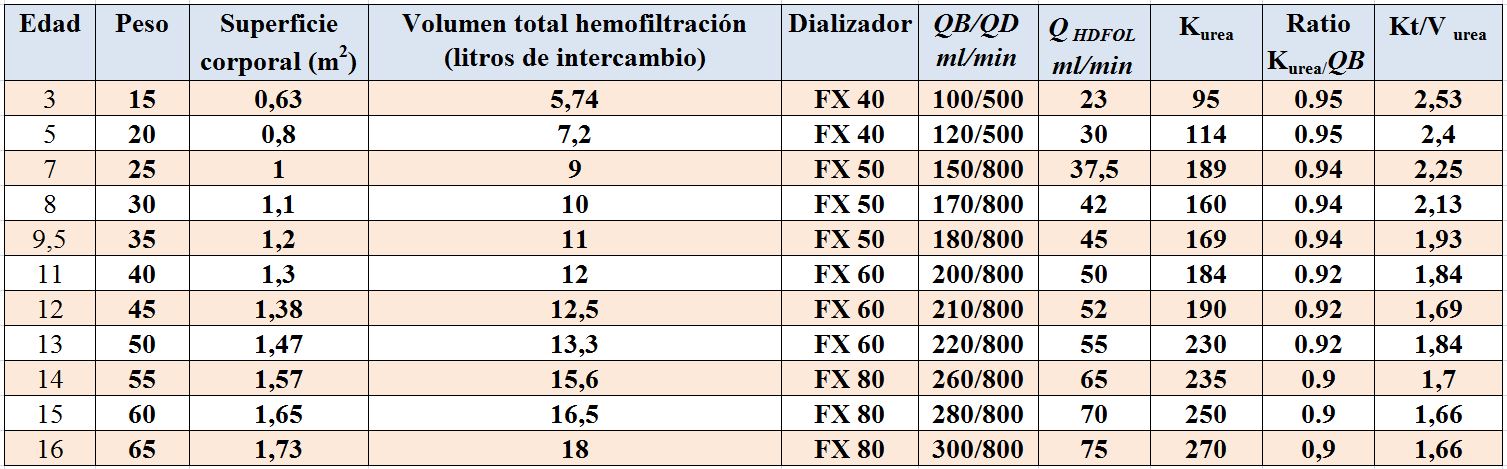
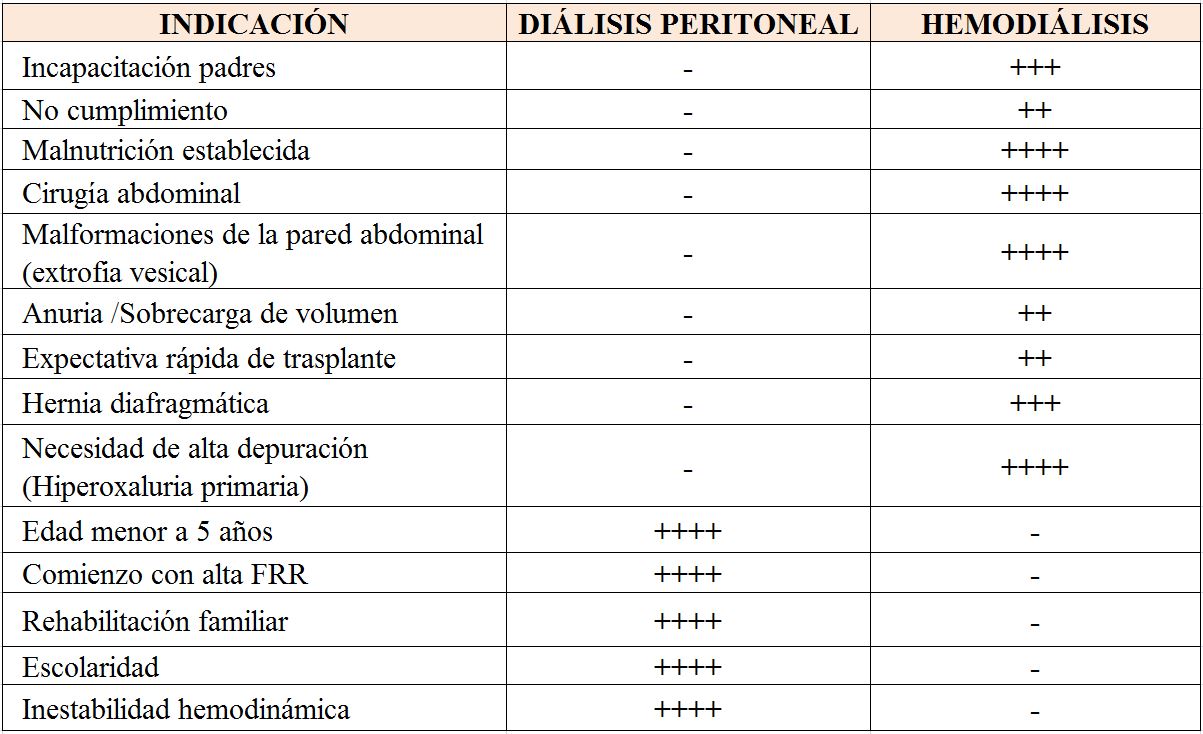
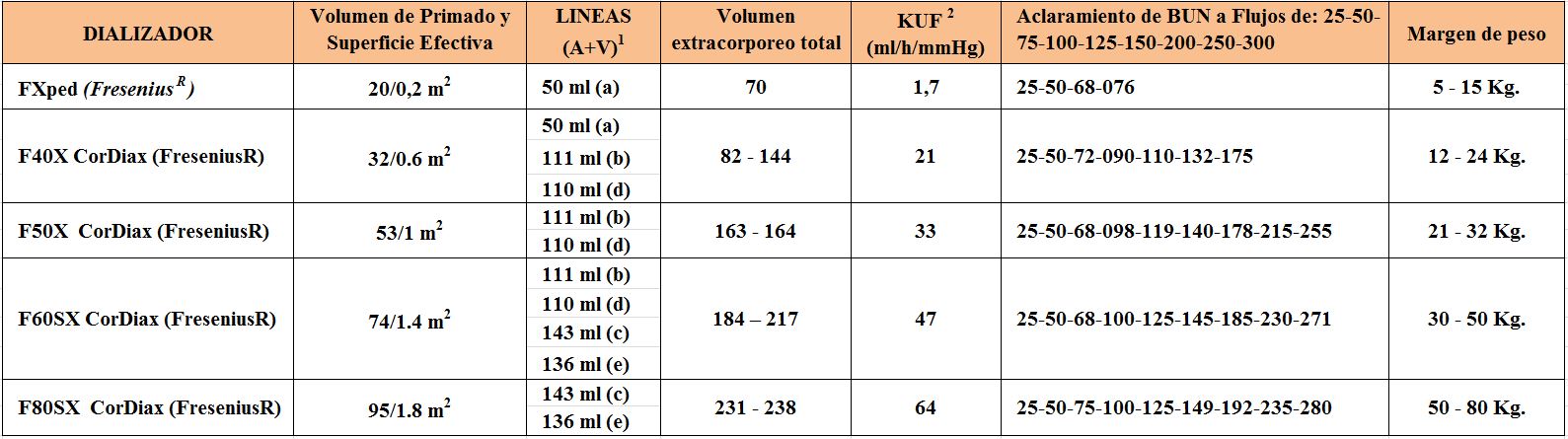
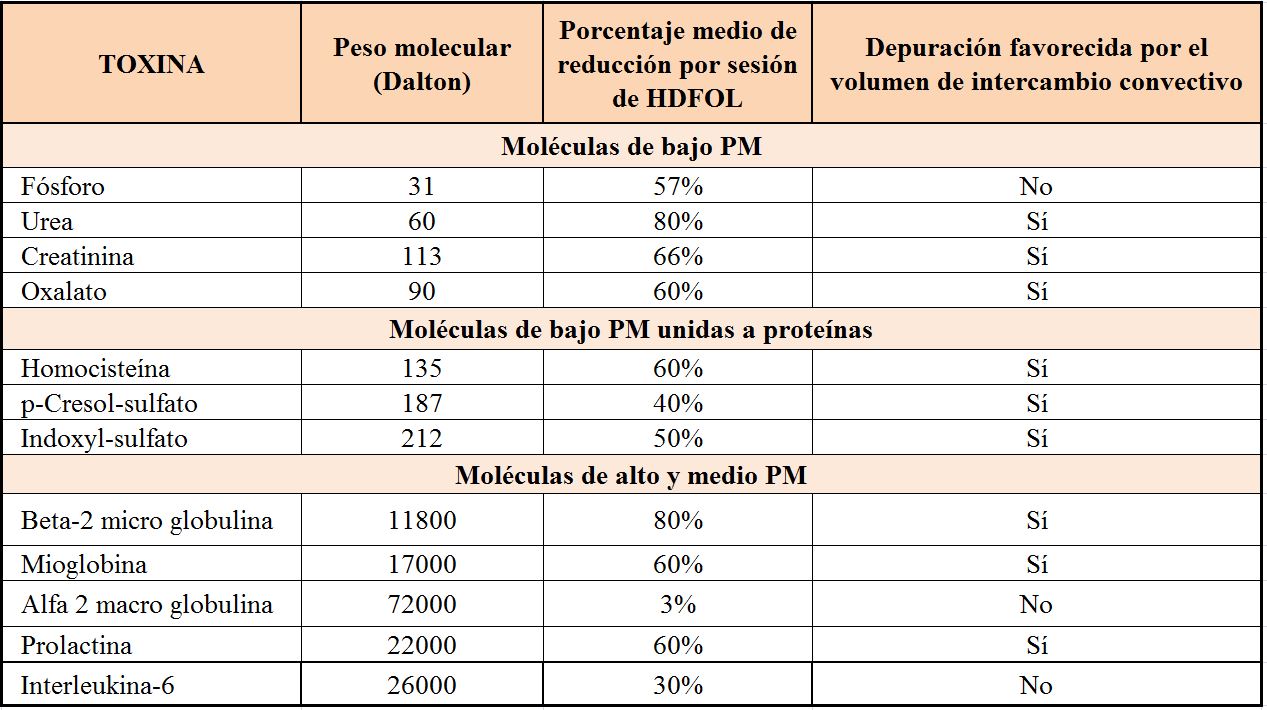
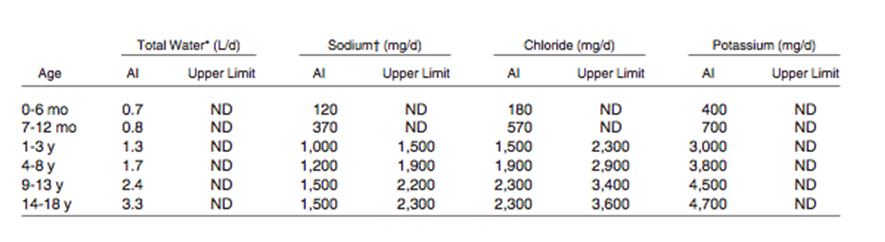
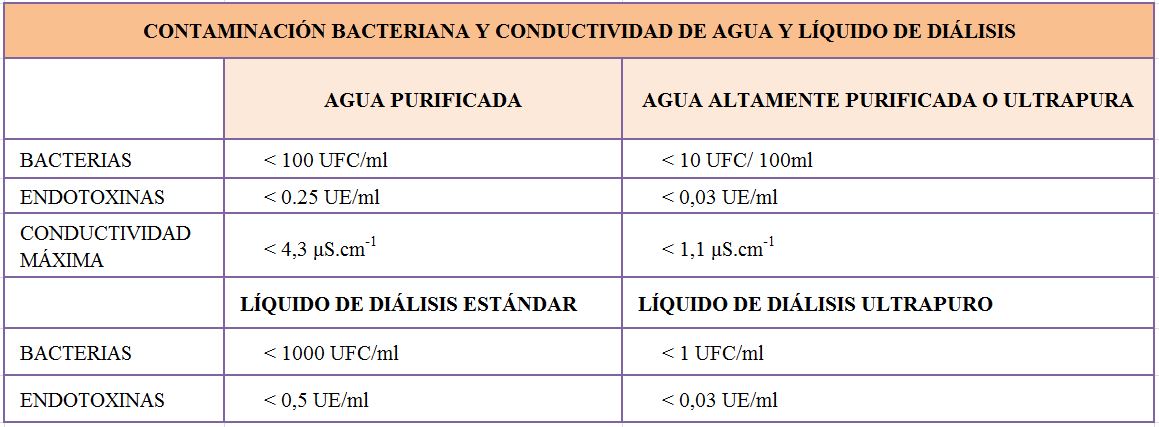
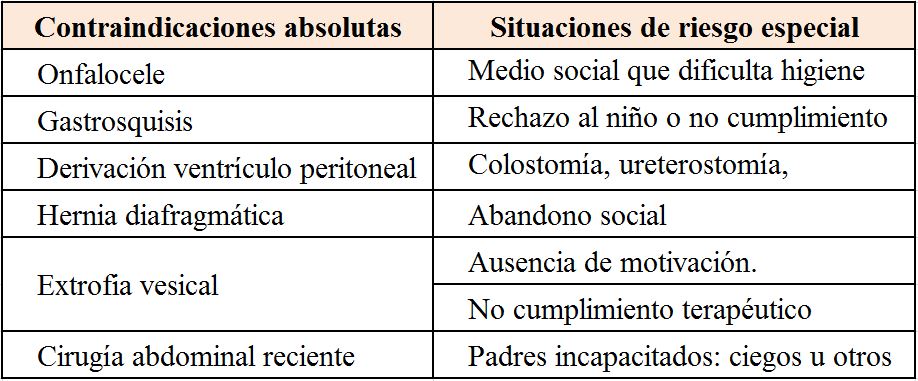
Figuras