Trasplante Renal Pediátrico con Donantes y/o Receptores límite
Introducción al donante y receptor límite en trasplante renal pediátrico
El trasplante renal es la forma ideal y universalmente aceptada de tratamiento de la enfermedad renal terminal del niño, ofreciendo un sinfín de ventajas reales sobre los otros tratamientos alternativos de reemplazo renal como son la hemodiálisis hospitalaria o domiciliaria y la diálisis peritoneal. En el momento actual la tendencia compartida por nefrólogos pediátricos es la realización de un trasplante anticipado que permita obviar el paso transitorio por diálisis; este hecho permite minimizar el impacto de la enfermedad renal y disminuir el gasto sanitario tanto de la institución como de la comunidad permitiendo además innumerables ventajas sociales y familiares.
Con todo ello, la realización de un trasplante renal anticipado en el estado español se consigue tan sólo en el 40% de los pacientes.
Es excepcional la exclusión definitiva de un niño de un programa de trasplante renal y cuando por motivos médicos, quirúrgicos o psicosociales se hace, es siempre de forma transitoria por un periodo corto de tiempo.
Por lo tanto, como norma general, podríamos definir que no hay receptores marginales en el trasplante renal pediátrico y sí situaciones comprometidas o de difícil abordaje.
No existe una definición universal de donante límite para receptor pediátrico. En este apartado el nivel de evidencia científica es menor y habitualmente descansa una vez más en la experiencia de los centros que aceptando continuos y nuevos desafíos amplían las características del donante pediátrico.
Consideraciones iniciales de la evidencia científica en trasplante renal en receptores pediátricos límite o con donantes marginales
En este grupo de estudio existen dificultades especiales para extraer conclusiones debido a la influencia del llamado efecto centro y a la ausencia de grandes estudios que podemos resumir en:
1. Ausencia de ensayos clínicos
2. Series cortas con resultados variables
3. Casos clínicos aislados
4. Recomendaciones de actuación basadas en opiniones de expertos
5. Protocolos de actuación y resultados influidos claramente por el nivel socio-económico del país [1].
Derivado de lo anterior el grupo pediátrico ha basado las líneas fundamentales para extraer conclusiones en:
1. Series amplias de grandes cohortes (registros colaborativos nacionales e internacionales: europeo, americano, japonés y australiano y neozelandés)
2. Amplio consenso de actuación en situaciones límites o marginales (actuaciones comunes consensuadas)
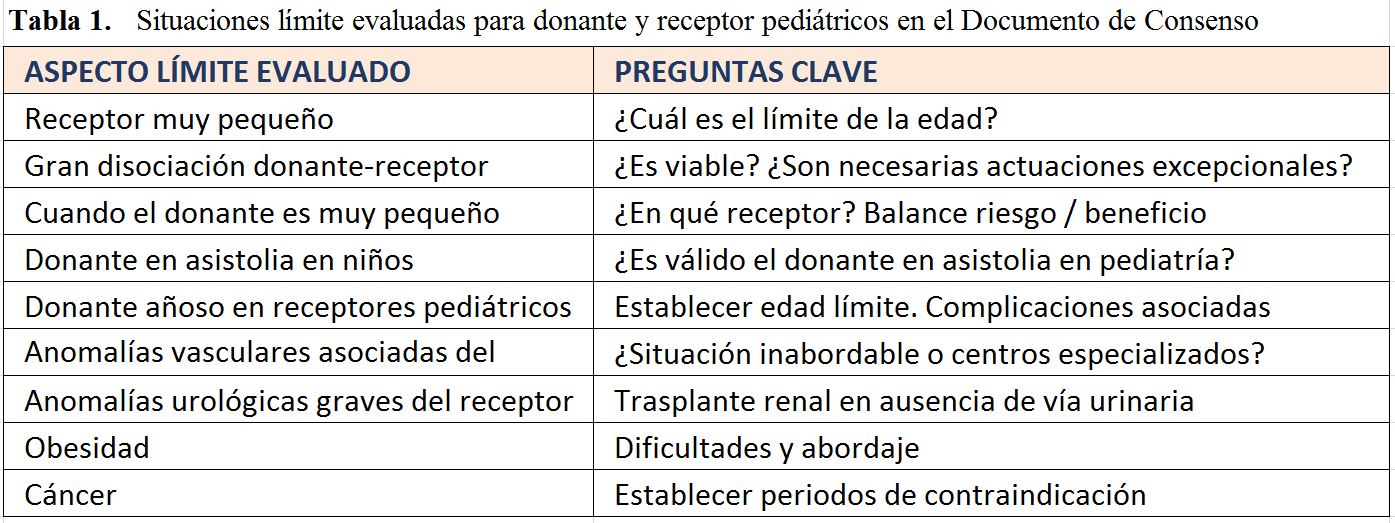
Situaciones límite evaluadas para donante y receptor pediátricos en el documento de consenso
Los aspectos evaluados en este documento de consenso y las preguntas que se han intentado resolver se pueden ver en la (Tabla 1)
Edad límite del receptor pediátrico
Los extremos de la edad pediátrica (lactantes y adolescentes) son los que de antemano presentan mayores dificultades para la realización de un trasplante constituyendo por sí mismos grupos de riesgo especial [1] [2] [3] (A).
Receptor de trasplante renal muy pequeño. edad y peso idóneos para el trasplante renal
El grupo de pacientes que presenta una mayor morbimortalidad en cualquier modalidad de tratamiento sustitutivo es el grupo de niños menores de 2 años (A) [1] [4].
El hecho de iniciar tratamiento sustitutivo durante el primer año de vida está asociado a un riesgo relativo independiente de mortalidad de 3 a 6 veces mayor que en otros grupos de edad (A) [1] [4].
En población pediátrica el inicio de tratamiento sustitutivo con trasplante tiene mejores resultados a corto y medio plazo que con diálisis, sin embargo, este hecho no está totalmente corroborado en menores de dos años [5] [6].
La realidad nos muestra que el trasplante renal en menores de 2 años y especialmente en menores de 1 año no es una práctica universal, lejos de ello el 99% de estos pacientes inician tratamiento con diálisis, especialmente diálisis peritoneal [1][4][5][6].
El inicio de los programas de trasplante renal en receptores extremadamente pequeños se asocian con mayor número de complicaciones vasculares; especialmente trombosis arterial y venosa (B), así como fallo primario del injerto; estas complicaciones son especialmente frecuentes cuando la edad del donante es asimismo extremadamente baja, siendo en muchos programas desestimado este tipo de donante para el receptor pequeño [7].
En la realización de un trasplante renal con una edad inferior a 2 años o peso inferior a 10 kilogramos son fundamentales las consideraciones quirúrgicas y el manejo perioperatorio y postoperatorio [6] [7] [8] [9] [10].
En esta población, aunque los datos son obtenidos en series cortas y con bajo nivel de evidencia, pero consensuadas de forma universal por la práctica clínica, una política adecuada de monitorización hemodinámica y de aporte adecuado de fluidos coloides y cristaloides se asocia con buenos resultados en receptores muy pequeños que reciben un trasplante renal, evitando pérdidas de injerto tempranas por causas técnicas como la trombosis vascular, la ausencia de función primaria o la necrosis tubular aguda [6] [7] [8] [9] [10].
Las aisladas experiencias cuando el peso del receptor es inferior a 6 kilogramos son en general negativas [7] [8].
Consenso de las unidades pediátricas españolas sobre el receptor pediátrico muy pequeño
Los integrantes del Grupo Prometeo Pediátrico de la Sociedad Española de Trasplante donde están representadas todas las unidades de referencia de trasplante renal pediátrico del estado español y con datos avalados por Registro Español Pediátrico de Tratamiento Sustitutivo (REPIR) y de otros registros europeos e internacionales acuerdan como grupo de expertos:
1. Se considera un peso aceptable límite de un receptor pediátrico 10 kilogramos, correspondiente a una edad de 2 años.
2. El tratamiento sustitutivo ideal inicial en el receptor con peso inferior a 10 kilogramos es la diálisis peritoneal y posponer el trasplante hasta que se haya alcanzado ese peso y/o edad si las circunstancias lo permiten.
3. De forma excepcional (fracaso peritoneal o de accesos vasculares u otros riesgos no definidos) se podría realizar un trasplante renal en receptores de 6 a 10 kilogramos de peso en centros con experiencia realizando un cuidadoso balance entre riesgos y beneficios.
4. Dado el importante riesgo de pérdida del injerto debería evitarse siempre la realización de un trasplante renal en receptores con peso inferior a 6 kilogramos.
5. El abordaje de un trasplante renal en receptores muy pequeños requiere un equipo multidisciplinar que incluya: cirujanos y/o urólogos con amplia experiencia; anestesiólogos, nefrólogos, intensivistas, nutricionistas y un amplio respaldo de otros especialistas pediátricos.
6. Por razones técnicas este tipo de trasplantes debe realizarse en centros pediátricos de referencia del estado español.
Receptor adolescente. ¿es un receptor límite?
La población pediátrica entre 12 y 18 años susceptible de recibir un trasplante convive con el proceso normalizado de la adquisición paulatina de autonomía y responsabilidades; este hecho, hace a esta población especialmente vulnerable al incumplimiento terapéutico y al riesgo permanente de rechazo [11] [12].
Los datos obtenidos de registros y de series muestran un incremento de pérdida del injerto por no adherencia al tratamiento con una incidencia máxima entre los 13 y los 21 años y una disminución en edades posteriores [11].
El tratamiento prolongado con diálisis no parece mitigar el riesgo posterior de incumplimiento terapéutico [12].
Aunque en líneas generales al adolescente no se le debe considerar un receptor límite, el proceso informativo antes, durante y después del trasplante y el apoyo mediante todas las armas de la institución (trabajadores sociales y psicólogos especialistas en adolescentes) es útil en la prevención de la no adherencia terapéutica [11] [12].
Es fundamental asegurar un proceso adecuado de transición a unidades de adultos.
Actitud perioperatoria en la disociación donante-receptor en receptores muy pequeños
El trasplante renal de donante adulto a un receptor muy pequeño requiere una mayor presión de perfusión inicial y puede condicionar un secuestro de la volemia del 33 al 50% siendo el manejo perioperatorio fundamental [7] [13] [14]. (A)
Para mantener una correcta presión de perfusión y disminuir el riesgo de trombosis vascular, el manejo perioperatorio debe incluir la administración de fluidos intravenosos (cristaloides y/o coloides) y fármacos inotrópicos junto con una correcta monitorización hemodinámica que incluye [14]:
1. Monitorización de la presión venosa central (PVC) mediante con catéter venoso central.
2. Monitorización directa arterial presión arterial (PA).
3. La presión arterial media (PAM) obtenida a los a los diez minutos de la re-perfusión del injerto no debe ser inferior a la del desclampaje (Riesgo de función retrasada del injerto).
4. La ratio PAM / peso: debería ser mayor de 4,3 en pacientes con peso de 13 a 21 Kilogramos (56 – 90 mmHg) mientras que la ratio PAM / peso: idealmente será mayor o igual de 2.5 en mayores de 22 kilogramos.
5. La PVC (parámetro de antemano asociado a mucha variabilidad determinada por muchos factores) debe situarse entre 12 y 18 cm H2O.
6. La monitorización del cociente entre la superficie corporal del donante y el receptor puede ser de utilidad; así un cociente > 0’8 predice una mejor función del injerto y una mayor supervivencia del injerto al año del trasplante.
Utilización de donantes pequeños. ¿existe un mayor impacto de trombosis venosa e hiperfiltración? ¿se asocia con peor supervivencia?
La utilización de donantes con peso de diez a veinte kilogramos (entre 3 y 5 años) en receptores pediátricos muestra una tasa baja de complicaciones quirúrgicas con una incidencia de trombosis venosas y supervivencia del injerto al año y al quinto año equiparable a los descritos en otros grupos de donantes [15] [16].
El registro norteamericano muestra buenos resultados de supervivencia del injerto a los cinco años (resultados equiparables a la utilización de donante adulto) pero, sin embargo, con peor supervivencia al año [17].
Los mejores resultados, observados en la actualidad con respecto a series históricas se debe fundamentalmente a la existencia de equipos quirúrgicos expertos y a la implantación de protocolos antitrombóticos junto a una cuidadosa selección del donante y receptor.
La utilización de donante pequeño ha demostrado un efecto real de crecimiento del órgano junto con la mejoría progresiva del filtrado glomerular; este hecho se acompaña de una sobreexpresión de marcadores de proliferación y de diferenciación podocitaria [18].
Sin embargo, y en contraste con los buenos resultados obtenidos con donantes de peso de 10 kilogramos, no hay suficiente evidencia para utilizar donantes con peso inferior en población pediátrica. Los resultados de análisis de cohortes con donantes de peso inferior a 10 kilogramos son peores y con mayor incidencia de complicaciones quirúrgicas y trombosis vasculares.
Utilización de donante añoso en receptores pediátricos. ¿cuál es el límite de edad?
En trasplante renal infantil se define donante añoso a aquel mayor de 50 años y tradicionalmente su utilización ha sido excepcional.
Sin embargo, en los últimos años en los registros de trasplante pediátrico internacionales se observa una mayor utilización de donantes vivos añosos (DVA) en población pediátrica; así por ejemplo, el registro UNOS [17] muestra un aumento del 3,6% en 1994 al 7,4% en el 2011. Por lo que debemos considerar que en el momento actual puede ser una opción considerable de donación si la edad no excede de forma importante los 50 años y si el estado de salud del posible donante permite la donación.
La supervivencia a los 5 años en los trasplantes renales de DVA es inferior a la de los trasplantes de donantes vivos jóvenes pero mejor que la de cualquier trasplante de donante cadáver, incluido los jóvenes [20] [21] [22] [23] [24], si bien, hay que tener en cuenta que el límite superior de la edad del DVA no está bien definida [21].
En el trasplante pediátrico con donante de cadáver añoso la supervivencia a largo plazo del injerto es peor a medida que aumenta la edad del donante por encima de los 50 años [21] [23] [24].
Donación en asistólica controlada en receptores pediátricos
Aunque la donación en asistolia controlada (datos de registros) en receptores pediátricos es sólo del 1,2 al 2,9%, en los últimos años va aumentando de forma progresiva.
En los dos estudios más importantes la mediana de edad del donante es de 21 años y ambos coinciden que pese a un mayor porcentaje de retraso en la función del injerto (19,7 y 25%), la supervivencia del injerto y paciente al tercer y cuarto año y medio es similar a la de aquellos receptores pediátricos que reciben un riñón en muerte cerebral [25]; si bien, con pocos datos de seguimiento a largo plazo, también se ha observado una peor supervivencia del injerto a partir del cuarto año de trasplante [26].
Derivado de los estudios anteriores concluimos que los injertos procedentes de donación en asistolia controlada en donantes seleccionados, representa una opción válida y adecuada para pacientes pediátricos y puede ampliar el número de donantes para esta población [27].
Anomalías urológicas complejas del receptor pediátrico
Hemos considerado anomalías urológicas complejas todas aquellas en las que se requiera un abordaje médico y quirúrgico especial antes de la realización de un trasplante renal, incluyendo:
a. Agenesia vesical,
b. Síndrome de la cloaca
c. Seno urogenital
d. Asociación VACTER
e. Atresia anorrectal
f. Extrofia vesical
g. Agenesia de sacro y/o regresión caudal.
En todas estas malformaciones congénitas se necesita un estudio pretrasplante detallado que incluye estudios ecográficos y urodinámicos, considerando la reparación o reconstrucción completa de la vía urinaria, así como la planificación de derivaciones continentes, la ampliación vesical o incluso la creación de una neovejiga [28] [29] [30].
Las anomalías del tracto urinario inferior deben ser estudiadas y preferentemente corregidas antes del trasplante (al menos entre 3-6 meses antes según los autores), siendo imprescindible el conseguir un reservorio urinario y un adecuado vaciado del mismo, incluso con aumento vesical si es necesario
Con frecuencia se precisa la realización de cateterismos vesicales intermitentes y en ocasiones la creación de una neouretra o derivación continente tipo Mitrofanoff.
Con mucho, la complicación más frecuente después del trasplante de todas estas malformaciones es la infección del tracto urinario, aunque no hay que olvidar el riesgo de malignidad en ampliaciones vesicales con intestino. Pese a todo, después de un abordaje pretrasplante adecuado, la supervivencia del injerto y del paciente es similar a otras patologías. Además, estos pacientes tendrán mayor riesgo de complicaciones con múltiples intervenciones y en algunos de ellos peor calidad de vida, pero ello nunca debe contraindicar el trasplante renal [28] [29] [30].
Es muy importante la existencia de un equipo multidisciplinar experimentado, con una buena planificación del tratamiento y de las intervenciones a seguir. El seguimiento urológico a largo plazo y el tratamiento de la vejiga neurógena son críticos para mantener un injerto sano.
El reflujo de alto grado está asociado con mayor morbilidad postrasplante y debe ser corregido previo al trasplante, siendo en ocasiones necesaria una nefrectomía previa de los riñones nativos.
Finalmente, y después de un tratamiento individualizado, el tipo de donante debería ser considerado previamente al trasplante.
Anomalías vasculares del receptor pediátrico
Las anomalías vasculares que comprometen al receptor pediátrico y deberían ser consideradas difíciles o especiales son:
Trombosis oclusiva de iliacas y/o cava inferior
Síndrome de aorta media
Síndrome de regresión caudal con vascularización infra abdominal alterada o hipodesarrollada
La que con más frecuencia compromete la realización de un trasplante renal es la trombosis total oclusiva de la vena cava inferior que requiere un procedimiento especial [31]; sin embargo, existen líneas comunes de actuación.
1. La exploración recomendada previa al trasplante es la RMN (Resonancia Magnética Nuclear o TAC (Tomografía Axial Computarizada) vascular.
2. Se debe garantizar el aporte vascular al nuevo órgano considerando el uso de colaterales incluso con cirugía exploradora y reparadora previa.
3. Hay que considerar el trasplante renal ortotópico como un recurso viable
4. Es muy importante la existencia de un equipo multidisciplinar experimentado que garantice una planificación del tratamiento e intervenciones a seguir, así como el mejor tipo de donante ajustado a las características del receptor.
Cáncer previo al trasplante. ¿qué tiempo de espera es necesario?
En los receptores que han tenido una neoplasia previa, no hay evidencia ni acuerdo en el tiempo de espera necesario para recibir un trasplante por lo que, en el momento actual, lo más aconsejable es valorar junto con los oncólogos, las probabilidades de recidiva, según el tipo, grado y extensión de la neoplasia, individualizando el tiempo de espera necesario [32].
Los estudios genéticos actuales son muy útiles ya que ayudan a distinguir entre los diferentes subtipos biológicos y, por tanto, a la toma de decisiones.
En la actualidad, tras la curación completa de un Tumor de Wilms, se aconseja un tiempo de espera corto, pudiendo ser considerado el posible receptor candidato a trasplante inmediatamente después del proceso de curación completa sin estar sujeto a una espera tradicional de 1-2 años [33].
Retraso psicomotor en el posible receptor de un trasplante renal pediátrico
Este documento de consenso elaborado por expertos de todas las unidades de trasplante renal pediátrico españoles no pretende en ningún momento ser dogmático sino que las recomendaciones emitidas tan sólo deberían ser una guía de ayuda a la toma de decisiones, en este sentido, la inclusión de un receptor pediátrico con retraso psicomotor grave en un programa de trasplante renal es una decisión difícil y siempre debe ser colegiada, incluyendo a todos los integrantes de los equipos multidisciplinares de trasplante y por supuesto a los padres.
En el momento actual no existe ningún consenso publicado para estos casos, tan sólo pequeñas guías con preguntas de ayuda para la toma de decisiones [34], y todas coinciden en la necesidad de basar la decisión en un consenso local del equipo trasplantador involucrando a los padres en el proceso.
Dada la supervivencia del paciente e injerto similar a los casos generales, hay autores que defienden la no contraindicación de un grave déficit intelectual para recibir un trasplante renal [35].
Las contraindicaciones absolutas para recibir un trasplante renal en un niño con grave déficit intelectual derivan de la asociación del retraso psicomotor con otras situaciones concomitantes y que por sí mismas representan ya una restricción total (véase más adelante) [33] [34] [35] [36] [37] [38].
Criterios absolutos de exclusión de trasplante del receptor pediátrico
En el proceso de trasplante renal pediátrico se consideran causas absolutas de exclusión las siguientes [33] [35] [36] [37] [38]:
1. Malignidad en los últimos 12 meses
2. Enfermedad pulmonar requiriendo tratamiento con oxígeno continuo.
3. Fallo cardíaco irreversible.
4. Infección activa.
5. Negativa para completar el calendario habitual de vacunas.
6. Inadecuado soporte social para realizar tratamiento post-trasplante
Obesidad en el receptor pediátrico
La decisión de realización de un trasplante renal a un receptor pediátrico con obesidad debe estar basado en decisiones del equipo, pero, en cualquier caso, receptores con un índice de masa corporal superior a 35 /Kg/m2 tienen un riesgo aumentado de pérdida del injerto a los 10 años [39] por lo que se debe estimular la pérdida de peso mediante hábitos que modifiquen el estilo de vida del receptor antes, y después del trasplante.