Hipofosfatemia en paciente joven
INTRODUCCIÓN:
La hipofosfatemia se define por una concentración baja de fósforo en suero o plasma, lo que no siempre implica una verdadera depleción corporal. Puede ser moderada, cuando la concentración sérica se sitúa entre 1-2,5 mg/dl, y es frecuentemente asintomática, pudiendo encontrarse hasta en un 5% de los pacientes ingresados. Los síntomas son más frecuentes cuando la hipofosfatemia es grave, con concentraciones séricas inferiores a 1 mg/dl, y se asocia en esos casos a mayor mortalidad.
En cuanto al manejo renal del fósforo, lo que se filtra se recupera en el túbulo proximal a través del cotransportador sodio-fosfato. De este modo, la respuesta renal normal frente a la depleción de fósforo es de aumentar la absorción reduciendo la excreción en la orina. Presentamos un caso en el que la respuesta a la hipofosfatemia no es la esperada.
CASO CLÍNICO:
Varón de 31 años sin antecedentes relevantes de interés, salvo otitis medias de repetición. Tampoco presenta antecedentes familiares de enfermedad renal.
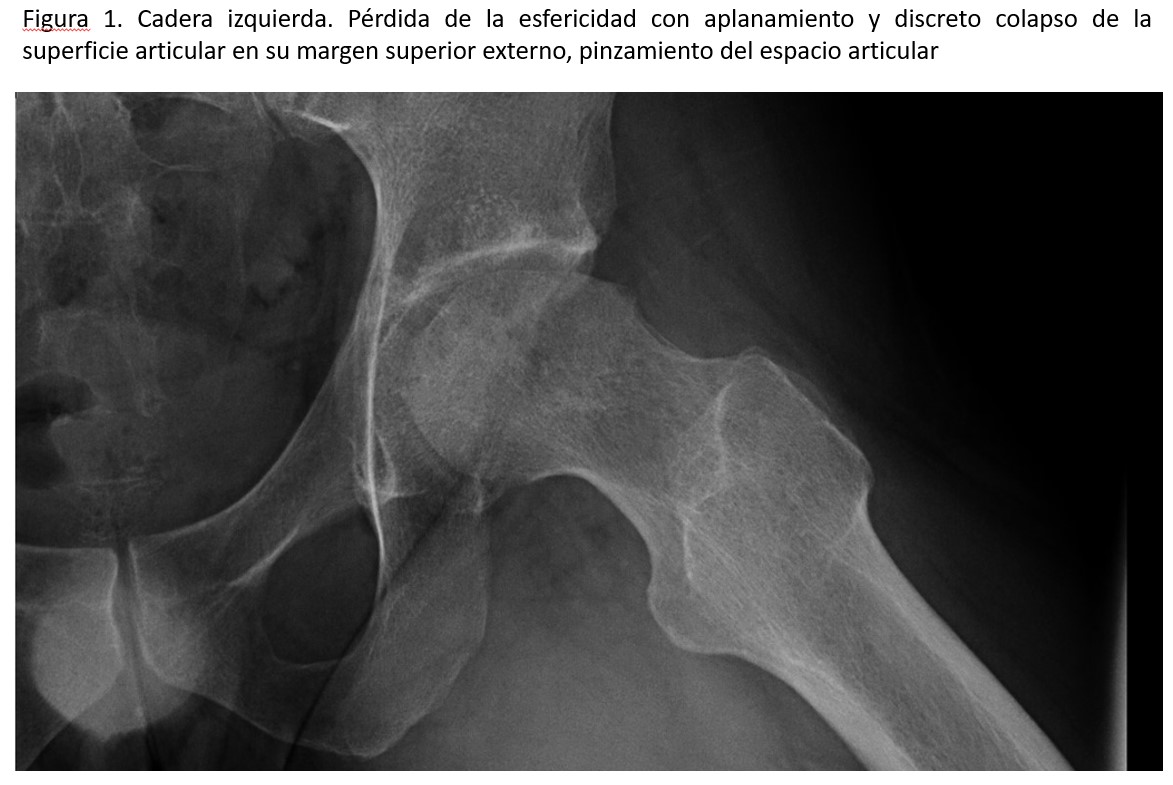
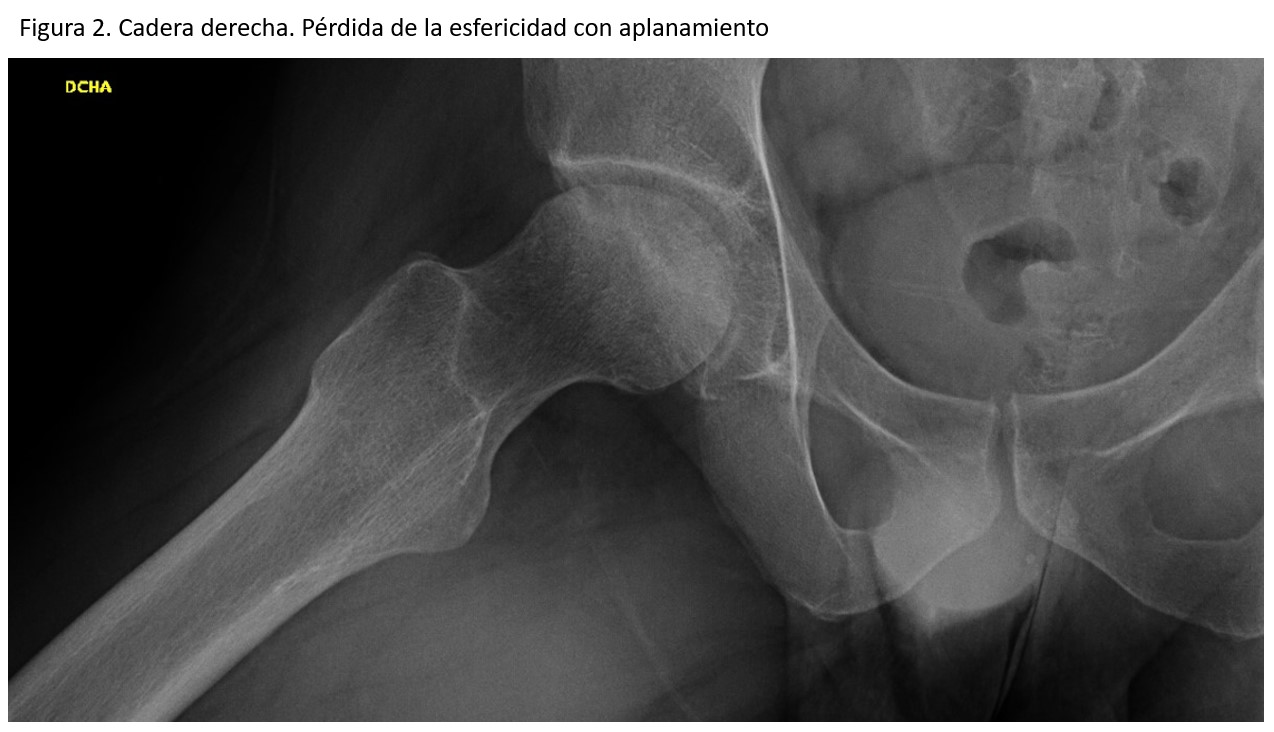
Acude a la consulta de atención primaria en enero de 2011 por dolor continuo en la pared costal y debilidad en miembros inferiores con dolor en la planta de los pies y dificultad para la marcha. La parrilla costal evidencia múltiples callos de fracturas costales sin traumatismos previos conocidos. Se inicia tratamiento con calcidiol mensual al encontrar niveles de 25-OH-vitamina D de 11,9 ng/ml y se remite a la consulta de neurología. Allí refiere aumento del dolor con la marcha y necesidad de toma de diclofenaco, además de rigidez al agacharse y levantarse desde sedestación. Se decide ingreso en noviembre de ese año para estudio de trastorno de la marcha progresivo con sospecha de triparesia con paraparesia proximal y distal flácida. Durante el ingreso, se realizan TC craneal, RM de columna y estudio de electromiografía descartando lesión medular y patología muscular. Se realiza también punción medular que es normal y con cultivos negativos. En los análisis llama la atención: P 1,1 mg/dl, Ca 9,8 mg/dl y Ca iónico 1,23 mmol/l. Por ausencia de patología de causa neurológica se remite a la consulta de reumatología en enero de 2012 donde se realiza radiografía de caderas evidenciando signos degenerativos bilaterales sin sacroileitis y deformidad de la cabeza femoral izquierda (Figura 1) (Figura 2). Por la persistencia de concentraciones bajas de P sérico con Ca y PTH normales lo remiten a consulta de nefrología para valoración en mayo de 2012.
En la anamnesis niega hábitos tóxicos, consumo de suplementos vitamínicos o fármacos fuera de diclofenaco. La ingesta y el tránsito intestinal son normales. Sin cambios ponderales en los últimos 6 meses. Persiste el dolor costal inespecífico y la dificultad para la marcha con fasciculaciones aisladas en ambos gastrocnemios. Refiere que cada vez que da un paso presenta dolor del tercio anterior de la planta del pie y también en región sacra.
Exploración física: TA 110/70 mmHg, FC 85 lpm, satO2 98%. Sin otros hallazgos.
Pruebas complementarias:
- Hemograma: Leucocitos 5040/microl, hemoglobina 16 g/dl, VCM 95 fl
- Bioquímica en sangre: Glucosa 91 mg/dl, urea 25 mg/dl, creatinina 0,78 mg/dl, calcio 9.5 mg/dl, fósforo 1,3 mg/dl, sodio 144 mmol/l, potasio 3,8 mmol/l, cloruro 104 mmol/L, magnesio 1.9 mg/dL, bilirrubina total 0,9 mg/dl, GPT 38 U/L, GOT 23 U/L, gamma-glutamiltransferasa 18 U/L, proteina C reactiva <1 mg/l, 25(OH)D: 25.1 ng/ml, 1-25-OH-VitD 45,7 pg/ml, PTH 31 pg/ml
- Gases venosos: pH 7.38 pCO2 48 mmHg, HCO3 27.3 mmol/l
- Orina elemental: pH 6.0, densidad 1020, nitritos, glucosa y proteínas negativos. Sedimento normal.
- Bioquímica en orina 24 h: Diuresis 1700ml/24h, creatinina 132 mg/dl, Na 137 mmol/24h, Ca/FG 0.08, P 155 mg/dl y 1556 mg/24h, excreción fraccional de fósforo (FPE) 71%, reabsorción tubular de fósforo (RTF) 48%. Ausencia de aminoaciduria.
- Ecografía renal: Normal.
Ante la presencia de una hipofosfatemia por pérdida renal y se mide factor FGF23 en plasma que está aumentado (290 pg/ml, normal <100 pg/ml). El PET-TAC fue normal. Se realiza primero estudio genético de FGF23 que es normal por lo que se indica estudio genético para otras alteraciones tubulares encontrando positividad para mutación del gen ENPP1 y se logra el diagnóstico final de raquitismo hipofosfatémico autosómico recesivo.
COMENTARIOS:
Nos enfrentamos al caso de paciente joven con una hipofostatemia, que por su concentración plasmática no se consideraría grave, pero que cursa con síntomas y deformaciones óseas, lo que nos lleva a buscar un obligado diagnóstico.
Frente a un valor disminuido de fósforo sérico tenemos que pensar en tres causas de hipofosfatemia: la disminución de la absorción intestinal, el desplazamiento del fósforo hacia el espacio intracelular y el aumento de las pérdidas urinarias (Ver. NAD: Trastornos del Calcio, Fósforo y Magnesio. Tabla 7 y Figura 6). Para diferenciarlas, si no se consigue por los datos clínicos, hay que ver la respuesta renal: si el riñón funciona normalmente la reabsorción renal de fósforo estaría elevada. Si esto no ocurre, como en nuestro caso, quiere decir que existe un defecto renal bien por hiperparatiroidismo o por una alteración en el transporte del fósforo.
Para calcular la eliminación de fósforo en orina, un valor > 100 mg en 24 h puede ser indicativo de pérdidas renales, pero es recomendable realizar el cálculo de la FPE o RTP:
FEP = [(Po x Crs) / (Ps x Cro)] x 100
RTP = (1- [(Po x Crs) / (Ps x Cro)])x 100
(Abreviaturas: Po: fósforo en orina, Ps: fósforo en sangre, Crs: creatinina en sangre, Cro: creatinina en orina)
Una FEP > 5% y una RTP disminuida (RTP < 80%) en un paciente con hipofosforemia confirman la pérdida renal inapropiada, como ocurría en nuestro caso. Descartamos el hiperparatiroidismo por presentar PTH y calcemias normales y la investigación se centró en los defectos en el transporte renal de fósforo.
Siempre hay que sospechar un defecto tubular frente a una hipofosfatemia persistente a pesar de corrección de déficit de vitamina D y que puede asociarse o no a otras alteraciones tubulares como glucosuria, aminoaciduria, hipouricemia y acidosis tubular renal. (ver NAD: Tubulopatías - Síndrome de De Toni-Debré-Fanconi). Nosotros nos centramos formas aisladas dada la ausencia de otras alteraciones tubulares y tenemos, por tanto:
1. Las formas hereditarias de raquitismo hipofosfatémico:
- el ligado al cromosoma X (gen PHEX)
- el autosómico dominante (genes FGF23, SGK3)
- el autosómico recesivo (genes DMP1, ENPP1, FAM20C)
- el asociado a hipercalciuria
2. La osteomalacia oncogénica (OO): suelen ser tumores pequeños, benignos, de crecimiento lento y se localizan frecuentemente en las extremidades, tanto en los huesos como en tejidos blandos.
Todas se caracterizan por un aumento de la síntesis o falta de degradación de fosfatoninas y en concreto el FGF23 que facilita la eliminación renal del fósforo. Así, el diagnóstico bioquímico se fundamenta en los datos descritos previamente más concentraciones bajas o inapropiadamente normales de calcitriol sérico y altas o inapropiadamente normales de FGF-23 plasmático. La determinación de FGF-23 sérico ayuda al diagnóstico clínico. El FGF-23 se expresa por los osteocitos, y regula el metabolismo del fósforo y vitamina D uniéndose al Klotho-FGF lo que en el riñón disminuye la RTP mediante una disminución de la expresión de los cotransportadores de sodio/fosfato tipo 2a y 2c e inhibe la actividad de la 1α-hidroxilasa renal. Estos mecanismos derivan en hipofosfatemia, hiperfosfaturia y niveles bajos de calcitriol.
Los síntomas y signos de la OO son similares a los de la osteomalacia hipofosfatémica familiar. Las principales manifestaciones clínicas en el adulto son el dolor óseo, la debilidad muscular proximal y las fracturas. Es difícil diferenciar las dos formas. En nuestro paciente se excluyó la posibilidad de OO tras realización de PET-TC. Se pensó, entonces, en una forma familiar, descartando mediante el estudio genético las alteraciones más frecuentes en los genes PHEX y FGF23, pero encontrando una mutación en ENPP1.
Un aspecto importante que queremos destacar es la gravedad de la sintomatología asociada a la hipofosforemia. Se ha descrito un amplio abanico de manifestaciones que se deben a la depleción de fosfato intracelular. Se pueden producir cambios en el sistema nervioso central (desde una leve irritabilidad y parestesias hasta encefalopatía metabólica, delirium, convulsiones generalizadas y coma) y en el músculo esquelético y liso (miopatía proximal, disfagia e íleo). En nuestro caso aparecían además de síntomas neurológicos y musculares aparecían alteraciones óseas costales y femorales que nos hablan de osteomalacia. El diagnóstico ahora es más accesible pero no siempre es fácil como demuestra el hecho de su paso por distintas consultas y el largo tiempo pasado hasta su diagnóstico.
Tratándose de una enfermedad rara los casos descritos en literatura son pocos y se han tratado con fosfato oral y calcitriol consiguiendo una mejoría del dolor óseo y estabilización de los valores de fósforo sérico [1].
El raquitismo hipofosfatémico es un trastorno poco usual que genera una importante comorbilidad para el que en el momento actual contamos con herramientas diagnósticas necesarias, aunque el tratamiento se basa en la sustitución de fósforo y vitamina D.
Bibliografía
1. Höppner J, Kornak U, Sinningen K, Rutsch F, Oheim R, Grasemann C. Autosomal recessive hypophosphatemic rickets type 2 (ARHR2) due to ENPP1-deficiency. Bone. 2021;153:116111. doi:10.1016/j.bone.2021.116111